Par Patrick Pla, Université Paris-Saclay

- L’ovocyte et son environnement
- Les réserves énergétiques
- Les réserves moléculaires
- Le contrôle de la progression de la méiose
Lors de la fécondation, le spermatozoïde n’apporte qu’un noyau, un centriole, quelques mitochondries (celles-ci sont ensuite impitoyablement détruites) et quelques protéines et microARN. Le cytoplasme du zygote est donc en immense majorité hérité de l’ovocyte. La quantité et la qualité des réserves énergétiques et des réserves moléculaires (ARN, protéines…) dans l’ovocyte a une influence considérable sur le développement embryonnaire, notamment sur la mise en place des axes de polarité.
L’ovocyte et son environnement
Chez la drosophile
Une femelle drosophile a deux ovaires composés d’environ 18 ovarioles, chacun pouvant être considéré comme une chaîne de production d’œufs.
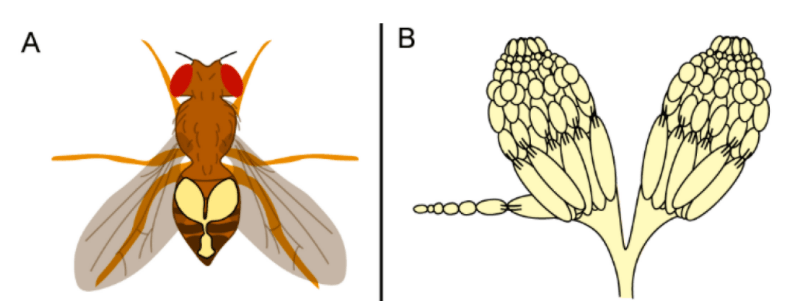
Vidéo d’une dissection d’ovaires de drosophile (en anglais) :
Le germarium, qui contient des cellules souches somatiques et germinales, se trouve à l’extrémité antérieure de l’ovariole. Il y a 2 à 3 cellules souches germinales par ovariole qui sont maintenues dans une niche particulière près des cellules de la coiffe qui leur envoient des signaux (notamment Dpp, l’orthologue chez la drosophile des BMP) qui inhibent leur différenciation (en inhibant l’expression du gène Bam) (Xie et al., 1998; Chen et al., 2003; Song et al., 2004). Les ovocytes et les cellules qui les entourent maturent au fur et à mesure qu’ils descendent l’ovariole, atteignant la partie postérieure avec des ovocytes compétents pour la fécondation. L’ovogenèse dure environ une semaine (Bastock et Saint Johnston, 2008).


L’ovocyte est entouré par :
- 15 cellules germinales appelées cellules nourricières avec qui il garde contact par des ponts cytoplasmiques. Les cellules nourricières deviennent polyploïdes et produisent des ARNm et des protéines qui sont transportées dans l’ovocyte.
- des cellules folliculaires qui appartiennent à la lignée somatique et qui forment une couche épithéliale autour de l’ensemble des 16 cellules germinales. L’ovocyte s’attache aux cellules folliculaires par des interactions médiées par la E-cadhérine. Les cellules folliculaires secrètent la membrane vitelline et le chorion qui protègent l’ovocyte et plus tard l’embryon.
Le développement des cellules germinales et des cellules folliculaires est interdépendant. L’ovocyte, qui est en position postérieure dans le germarium, induit via la voie Gurken/Torpedo (orthologue à EGFR des Vertébrés) les cellules folliculaires terminales adjacentes à adopter un destin postérieur plutôt qu’antérieur (González-Reyes et St. Johnston 1995 ; Roth et al. 1995). Ces cellules folliculaires postérieures signalent ensuite à l’ovocyte de polariser les microtubules le long d’un axe qui sera l’axe antéro-postérieur du futur embryon (pôle – du côté antérieur, pôle + du côté postérieur). Cette réorganisation nécessite l’activité de la PKA au pôle postérieur de l’ovocyte qui est activée par des signaux en provenance des cellules folliculaires postérieures (Lane et Kalderon, 1994). Toutes ces étapes très précoces sont donc déterminantes pour le développement du futur embryon.
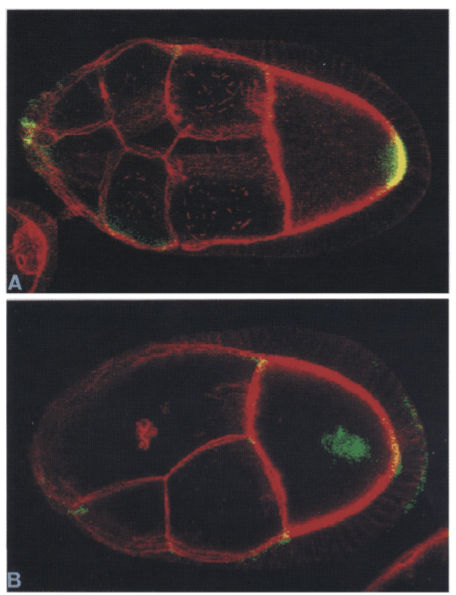
Un peu plus tôt, les cellules germinales exprimaient Delta à leur surface. Les cellules folliculaires exprimaient Notch et avaient ainsi activé la voie de signalisation correspondante (Roth, 2001, Lopez-Schier et St Johnston, 2001). Si on empêche cette interaction Delta-Notch, les cellules folliculaires ne sont pas assez différenciées et ne répondent pas correctement au signal inducteur Gurken. Il s’ensuit que les cellules folliculaires postérieures ne sont pas bien induites et qu’elles ne peuvent pas envoyer en retour le bon signal pour polariser l’ovocyte. L’axe antéro-postérieur de l’embryon est par la suite très altéré.
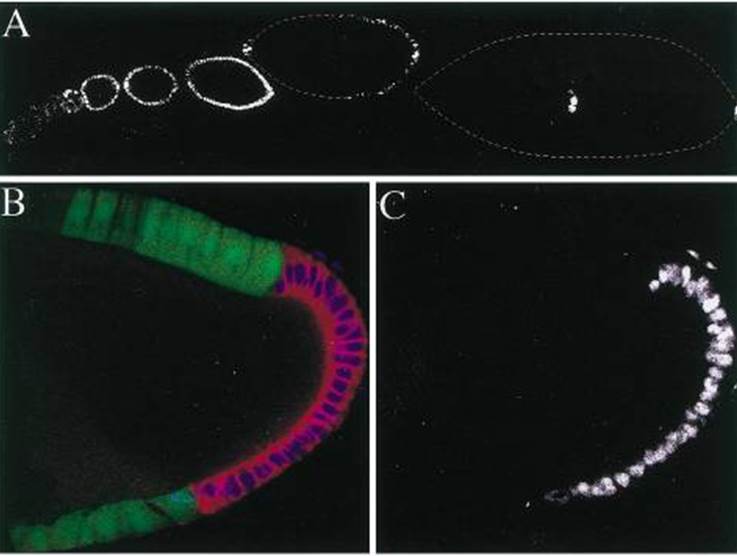
Les interactions entre l’ovocyte et les cellules folliculaires environnantes sont aussi essentielles pour établir l’axe dorso-ventral de l’embryon avant même la fécondation. Le noyau de l’ovocyte, localisé initialement en position antéro-dorsale, contrôle la localisation de la protéine Gurken qui se lie au récepteur Torpedo (EGFR) sur les cellules folliculaires dorsales adjacentes, inhibant ainsi l’expression du gène pipe dans cette région. À l’opposé, les cellules folliculaires ventrales expriment Pipe, une sulfotransférase qui modifie le protéoglycanne Vitelline Membrane Protein 2 (Vm32E), générant un signal ventral diffusible traversant la membrane vitelline ; ce signal active le récepteur Toll à la surface de l’ovocyte, déclenchant une cascade protéolytique (Spätzle, Snake, Easter) qui libère le facteur de transcription Dorsal du complexe inhibiteur Cactus. Ce gradient nucléaire de Dorsal (fort ventralement, faible dorsalement, rappelez vous que le nom des gènes de drosophile est donné d’après le phénotype du mutant perte-de-fonction !) détermine alors plus tard la différenciation cellulaire embryonnaire en activant des gènes ventralisateurs (comme short gastrulation, twist) ou dorsalisateurs (decapentaplegic (dpp)) selon sa concentration.
Chez les Mammifères
A partir de la puberté, régulièrement, une cohorte de follicules primordiaux se réveille et se développe pour passer au stade de follicule primaire puis secondaire puis de De Graaf.

Chez la femme, tout ce processus prend 190 jours avant d’arriver au cycle final où l’un des follicules de cette cohorte devient dominant et sera celui dont l’ovocyte sera ovulé (attention tout le processus dure bien plus longtemps que les 14 jours de la phase folliculaire comme on peut l’imaginer en regardant certains schémas trop simplifiés !). Les autres follicules entrent en atrésie et dégénèrent. Les premiers stades de cette maturation sont indépendants de la FSH produite par l’adénohypophyse mais à partir du stade follicule secondaire, les cellules de la granulosa expriment des récepteurs à la FSH et se mettent à produire des oestrogènes qui sont indispensables à la maturation des cellules folliculaires et de l’ovocyte.
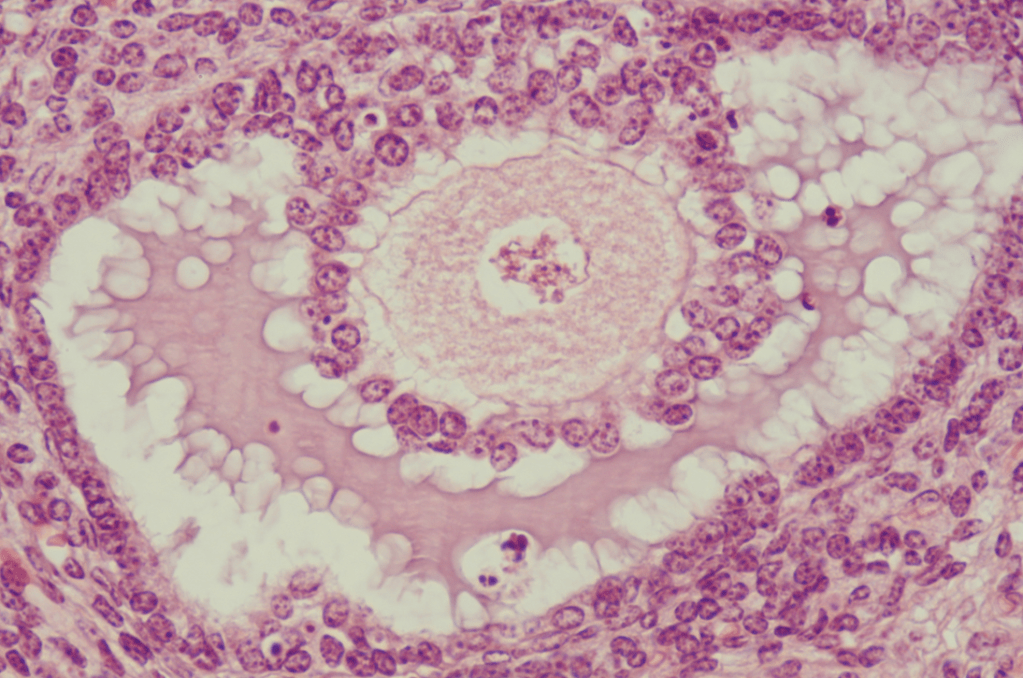
Durant l’ovogénèse des mammifères, l’ovocyte synthétise une matrice extracellulaire qui va notamment interagir avec les spermatozoïdes lors de la fécondation : la zone pellucide. Elle est composée de glycoprotéines nommées ZP1 à ZP4.

Malgré l’épaississement de la zone pellucide, l’ovocyte garde contact avec les cellules environnantes de la corona radiata par des projections cytoplasmiques transzonales. Les cellules communiquent par des jonctions gap impliquant la connexine 37 et l’absence de connexine 37 aboutit à une infertilité (Simon et al., 1997).

Les ovocytes ne peuvent pas métaboliser le glucose et les cellules environnantes lui envoient du pyruvate et du lactate par ces jonctions (Su et al., 2009). La présence des jonctions gap est diminuée au moment de l’ovulation et de la reprise de la méiose (qui était bloquée en prophase I). Cela permet de découpler les taux d’AMPc et de GMPc dans les deux types de cellules (baisse chez l’ovocyte, maintien chez les cellules environnantes), ce qui est nécessaire pour la reprise de la méiose (Okudaira et al., 2017, Thuratum et Sroyraya, 2017). Avant l’ovulation, l’ovocyte sécrète BMP-15 qui est nécessaire à la survie des cellules folliculaires (Hussein et al., 2015). Un nombre suffisant et une bonne santé des cellules de la corona radiata sont en retour nécessaires pour avoir des ovocytes qui ont de bons succès de fécondation.
Suivant le pic de LH qui provoque l’ovulation, les cellules de la corona radiata sécrètent de l’acide hyaluronique dans la matrice extracellulaire ce qui favorise l’ovulation (Zuo et Kimata, 2001).
La coopération existe donc bel et bien entre l’ovocyte et ses cellules somatiques environnantes chez les Mammifères tout comme chez la drosophile. Cependant, la mise en place des axes de l’embryon se fait bien plus tard et d’une autre manière chez les Mammifères.
Voir le chapitre « Développement des cellules germinales » pour plus d’informations.
Les réserves énergétiques
Chez les Vertébrés
Au cours de l’ovogénèse, il y a accumulation de réserves énergétiques dans l’ovocyte sous forme de vitellus. Elles se présentent en agrégats appelées plaquettes vitellines. Ce sont des réserves protéiques et surtout lipidiques (à poids égal les lipides permettent de stocker plus d’énergie que les glucides). Elles ne sont pas synthétisées dans l’ovocyte mais dans le foie sous le contrôle des œstrogènes (hormones sexuelles femelles produites dans les ovaires). La secrétion d’oestrogène par les cellules folliculaires de l’ovaire est contrôlée par l’axe hypothalamo-hypophysaire.
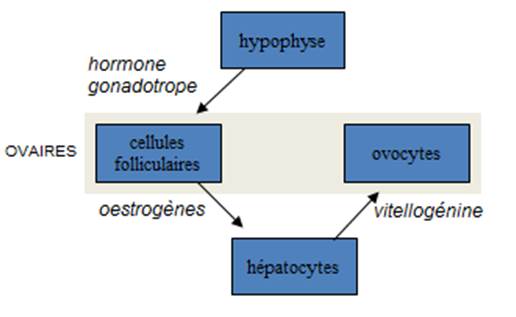
Les réserves sont acheminées vers l’ovaire par voie sanguine, notamment sous la forme d’une grande phosphoglycolipoprotéine appellée vitellogénine (470 kDa). Celle-ci est reconnue par un récepteur de la famille des récepteurs aux VLDL (Very Low Density Lipoprotein) à la membrane plasmique des ovocytes et le tout est internalisé par endocytose. Les endosomes fusionnent ensuite avec les lysosomes où la vitellogénine est clivée en différents fragments : phosvitine et lipovitelline. Les plaquettes vitellines sont dérivées des lysosomes et sont donc entourées par une membrane et contiennent la cathépsine D (une enzyme caractéristique des lysosomes).
Les composants majeurs du vitellus chez la poule sont :
- Les lipovitellines (a et b) : des lipoprotéines
- La phosvitine : une phosphoprotéine qui fixe le fer (réserve de fer)
- Les LDL (Low Density Lipoprotein)
- Les livetines dont certaines sont apparentées aux globulines sanguines
Les ovocytes sont classés selon la quantité de vitellus accumulée au cours de l’ovogénèse. Les ovocytes télolécithes (tels ceux des Sauropsidés ou des Téléostéens) ont des quantités très importantes de réserves qui s’accumulent progressivement dans l’ovocyte. Par exemple chez la poule, la croissance de l’ovocyte se déroule en 3 phases : 1) une phase dite « précoce » qui peut durer jusqu’à plusieurs années, 2) une phase de croissance lente de quelques mois, où s’accumulent des couches de vitellus dites « blanches », qui contiennent plus de protéines, et des couches dites « jaunes », comprenant plus de lipides, et enfin 3) une phase de croissance rapide, où sont transférées de grandes quantités de vitellus « jaune », 6 à 11 jours avant l’ovulation.
Les ovocytes télolécithes ont tellement de réserves que le vitellus empêche les divisions cellulaires au cours du développement embryonnaire. Ainsi, après la fécondation, seule une partie du volume de l’ovocyte se cellularise, le vitellus restant en dehors de l’embryon. L’embryon récupère les nutriments grâce à une annexe embryonnaire : la vésicule vitelline. Elle est formée d’endoderme qui sécrète des enzymes qui digèrent le vitellus et de mésoderme qui forme des vaisseaux sanguins capables de ramener les nutriments vers l’embryon.
Les ovocytes hétérolécithes (tels ceux des Amphibiens) ont suffisamment de réserves pour assurer tout le développement de l’embryon mais pas assez pour gêner les divisions cellulaires après la fécondation. Le vitellus se retrouve dans les cellules qui l’utilisent directement. Il n’y a pas besoin d’annexes embryonnaires. L’autre caractéristique d’un ovocyte hétérolécithe est la répartition inégale des réserves en vitellus. Dans l’ovocyte des amphibiens, le vitellus s’accumule autour du pôle végétatif. 75% du vitellus se retrouve ainsi dans l’hémisphère végétatif. Une pigmentation superficielle du cytoplasme (granules de mélanine) se répartit autour du pôle animal, dans ce qui forme l’hémisphère animal. On a donc un premier axe pôle animal-pôle végétatif.
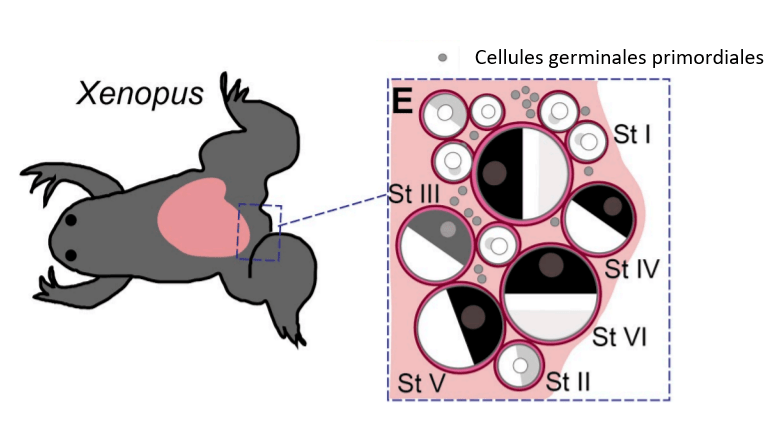
Chez les amphibiens, deux phases d’accumulation de vitellus se succèdent :
- la phase de petit accroissement ou prévitellogenèse qui dure de 2 à 3 ans
- la phase de vitellogenèse proprement dite qui dure 3 mois et voit l’essentiel de l’accroissement du volume de l’ovocyte

Une version commentée de cette figure est disponible en vidéo.
D’après Patten et Carlson, Foundations of Embryology (1958), McGrawHill
Les ovocytes alécithes tels que ceux de la plupart des Mammifères n’ont pas de réserves. Les Mammifères Monotrèmes tels que l’ornithorynque qui sont ovipares ont en revanche des ovocytes télolécithes. Le gène codant la vitellogénine n’est présent chez les Mammifères Métathériens (Marsupiaux) et les Euthériens (Primates, Rongeurs…) qu’à l’état vestigial de pseudogène. Avant son implantation dans la paroi de l’utérus, l’embryon vit libre dans la lumière des voies génitales femelles. Il est nourri par les sécrétions des glandes utérines qui se sont développées sous le contrôle de la progestérone produite au cours de la phase lutéinique du cycle ovarien (par le corps jaune).
Chez les Insectes
Au cours de la vitellogenèse des insectes, le précurseur des protéines du vitellus, la vitellogénine (Vg), est principalement synthétisé dans le corps adipeux et sécrété dans l’hémolymphe. À l’aide de la circulation de l’hémolymphe, Vg est transporté vers l’épithélium folliculaire qu’il traverse à travers des espaces intercellulaires et atteint la membrane ovocytaire, où a lieu une endocytose médiée par le récepteur Vg (VgR, classés dans la famille des récepteurs des lipoprotéines de basse densité (LDLR)) (Wu et al., 2021). En plus de transporter Vg pour l’absorption des ovocytes, signalons que VgR s’avère servir de cheval de Troie pour la transmission verticale des microbes pathogènes et des symbiotes Wolbachia. Lors de l’internalisation de Vg médiée par VgR, le complexe Vg/VgR sur la membrane de l’ovocyte se regroupe dans des fosses recouvertes de clathrine et s’invagine dans le cytoplasme. Le complexe se pince ensuite pour former des vésicules intracellulaires. Vg et VgR sont dissociés par acidification dépendante de l’ATP après avoir été transportés dans l’endosome. Par la suite, VgR retourne à la membrane de l’ovocyte, tandis que Vg est cristallisé et stocké sous forme de plaquette vitelline.
L’hormone juvénile (JH), une hormone sesquiterpénoïde produite dans les corps allates (ou corpora allata), stimule la vitellogenèse et le développement des ovocytes chez diverses espèces d’insectes. L’action moléculaire de JH repose sur son complexe de récepteurs intracellulaires comprenant deux facteurs de transcription bHLH-PAS, Methoprene-tolerant (Met) et Taiman (Tai).
Signalons que chez C. elegans, la vitellogénine est synthétisée dans les cellules intestinales et sécrétée dans la cavité générale (Kimble et Sharrock, 1983).
Les réserves moléculaires
La transcription est inhibée au cours des premières divisions du développement embryonnaire. Ainsi, le succès du développement précoce dépend des réserves moléculaires dans l’ovocyte. Elles comprennent des ARN (ARNm mais aussi ARNt et ARNr) et des protéines. Par exemple, dans un ovocyte de Xénope, il y a l’équivalent en histones pour 10.000 noyaux de cellules ordinaires. On peut inclure dans cette catégorie les mitochondries qui se divisent abondamment au cours de l’ovogénèse (il y a dans l’ovocyte d’une grenouille un nombre de mitochondries habituellement trouvé au total dans 100.000 cellules larvaires).
Chez les amphibiens, les gènes qui codent les précurseurs des ARN ribosomiques sont présents en 500 copies dans l’organisateur nucléolaire. Au stade pachytène de la méïose I, ces gènes sont activement répliqués (alors que l’on n’est pas dans la phase S du cycle où la réplication a habituellement lieu !) et environ 2000 copies sont produites. Elles forment des ADN circulaires extrachromosomiques ce qui va génère des milliers de nucléoles qui se répartissent à la périphérie du noyau. Celui-ci se dilate au stade diplotène et prend le nom de vésicule germinative. Cette amplification sélective permet de produire de très grandes quantités d’ARNr qui sont incorporés dans les ribosomes et permettent d’assurer la traduction durant tout le développement précoce de l’amphibien. Les ribosomes se concentrent autour du noyau créant un gradient ribonucléoprotéique qui est opposé au gradient vitellin.
L’activité transcriptionnelle est intense au cours de la vitellogenèse. Or l’ovocyte est bloqué en prophase I de méiose et donc les chromosomes sont déjà condensés. Les zones activement transcrites (marquées par de l’uracile tritiée par exemple) sont cependant décondensées formant des boucles : les chromosomes ainsi structurés sont appelés chromosomes en écouvillon. Ils ont été observés pour la première fois par Flemming en 1882 mais il a fallu attendre plusieurs décennies avant de comprendre leur fonction.

Les ARNm n’existent pas seuls dans le cytoplasme ; ils se lient à un certain nombre de protéines pour former des complexes ribonucléoprotéiques. Les protéines de liaison à l’ARN (RBP) et les moteurs moléculaires assurent le transport des ARNm le long du réseau de microtubules de l’ovocyte, ce qui entraîne une distribution asymétrique des ARN. En effet, les microtubules sont des structures polarisées et orientées de manière non aléatoire dans l’ovocyte (voir un exemple précis plus loin). Les RBP sont aussi capables de réguler la stabilité et la traduction des ARNm, ce qui a une importance considérable au début du développement embryonnaire où la transcription est inhibée.
De manière importante, la localisation des molécules d’ARNm et des protéines dans le cytoplasme de l’ovocyte a un rôle fondamental pour l’acquisition des axes de polarité de l’embryon. Par exemple, chez la drosophile, l’axe antéro-postérieur est déterminé par la localisation dépendante des microtubules des ARNm bicoid (bcd) et oskar (osk) respectivement aux pôles antérieur et postérieur de l’ovocyte. L’ARNm bcd n’est pas traduit pendant l’ovogenèse et n’est traduit que lorsque l’œuf fécondé, fournissant une source locale de protéine Bcd, qui diffuse pour former un gradient de morphogène qui modèle la moitié antérieure de l’embryon. En revanche, l’ARNm osk est traduit lorsqu’il atteint la partie postérieure de l’ovocyte pour produire des isoformes longues et courtes de la protéine Oskar. La forme longue d’Oskar ancre son propre ARNm, tandis que la forme courte d’Oskar agrège les granules polaires, conduisant au recrutement postérieur des déterminants de la lignée germinale et du déterminant abdominal, l’ARNm nanos.

Source : Roth et al., 1995.
Initialement, les ARNm bcd et osk sont transcrits dans les cellules nourricières associées à l’ovocyte et sont ensuite transportés par la dynéine le long des microtubules à travers des ponts cytoplasmiques vers l’ovocyte.
La localisation de l’ARNm osk à la partie postérieure de l’ovocyte nécessite la protéine motrice se déplaçant vers l’extrémité positive des microtubules, la Kinésine-1, les microtubules de l’ovocyte étant en majorité orientés avec le pôle positif vers la future région postérieure de l’embryon.

La localisation de l’ARNm bcd dépend en revanche de la protéine motrice se déplaçant vers le pôle opposé, l’extrémité négative des microtubules, la dynéine. La protéine Staufen reconnait un motif particulier dans le 3’UTR de l’ARNm de bicoid et fait la liaison de cet ARNm avec la dynéine (Ferrandon et al., 1994).
Chez les amphibiens, certains ARNm sont également concentrés dans des régions bien précises de l’ovocyte. Cela peut se faire en plusieurs phases : par exemple, les ARNm de Xwnt11 et Vg1 sont d’abord répartis dans tout le cytoplasme puis ils sont transportés vers le pôle végétatif le long des microtubules.

Une séquence de 340 nucléotides dans le 3’UTR de l’ARNm de Vg1 est nécessaire et suffisante pour expliquer la localisation de cet ARNm puisque si on enlève cette séquence les ARNm Vg1 restent répartis uniformément dans le cytoplasme et si on ajoute cette séquence sur un ARNm contrôle comme celui de la β-globine, cet ARNm se retrouve concentré autour du pôle végétatif alors que ce n’est pas du tout sa position habituelle. La protéine qui interagit avec la séquence de 340 nucléotide dans le 3’UTR de l’ARNm de Vg1 et l’arrime à un complexe avec des kinésines et les microtubules s’appelle Vera (Deshler et al., 1997; Messitt et al., 2008). Elle fait partie d’un complexe dans lequel on trouve un orthologue de Staufen (une protéine impliquée dans la localisation des ARNm dans l’ovocyte de drosophile) (Yoon et Mowry, 2004).

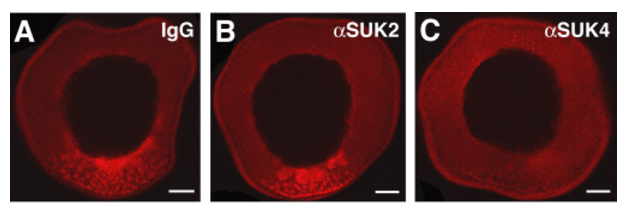
Source : https://www.cell.com/developmental-cell/fulltext/S1534-5807(08)00278-5
Une fois arrivé à destination près du pôle végétatif, l’ARNm est accroché aux microfilaments d’actine et se retrouve dans un complexe avec un ARN non traduit (Xlsirt) qui stabilise sa localisation (Kloc et Etkin, 1994).
Le transport de l’ARNm de Xwnt11 ou de l’ARNm de Xcat-2 qui est un composant du plasme germinal (qui va donner les cellules germinales) vers le pôle végétatif emprunte un autre mécanisme et est couplé au mouvement des mitochondries (Zhou et King, 1996). Cette voie de localisation est parfois appelée voie METRO. La localisation de Xcat-2 avec les mitochondries (dans ce qui est désigné par le « nuage mitochondrial ») dépend d’une séquence de 250 nucléotides dans le 3’UTR de cet ARNm.
L’organisme maternel accumule aussi dans les ovocytes des éléments pour protéger les futurs embryons. Par exemple, chez la drosophile, des piARN sont déposés avec pour fonction de protéger le génome des embryons contre le déplacement des transposons. Ces déplacements peuvent menacer l’intégrité du génome ce qui serait fâcheux lors du développement précoce, particulièrement si cela touche la lignée germinale (Luo et al., 2020). Le principal mécanisme de défense contre les transposons est la voie des ARN interagissant avec Piwi (piARN). Les piARN sont longs de 23 à 30 nucléotides et complémentaires des ARN dérivés des transposons. Ils dirigent les protéines Piwi associées vers les transposons actifs. Chez la drosophile, la répression guidée par Piwi provoque le clivage de l’ARNm cytoplasmique par Aubergine (Aub), Argonaute-3 (Ago3) et Piwi et induit la répression co-transcriptionnelle par formation d’hétérochromatine. En plus des piARN, toutes les protéines composantes de cette voie sont déposées par la mère dans l’ovocyte. La déplétion de Piwi d’origine maternelle aboutit à une augmentation de l’activité des transposons dans l’embryon précoce (Fabry et al., 2021).
Le contrôle de la progression de la méiose
En tant que gamète, l’ovocyte prêt à être fécondé est une cellule haploïde qui a subi la méiose quoique de manière incomplète et intermittente. En effet, les ovocytes dans l’ovaire sont bloqués en prophase I de méiose et ce sont les hormones qui déclenchent l’ovulation qui débloquent la méiose grâce à l’activation d’un complexe jusqu’à un nouvel arrêt en métaphase II. C’est la fécondation qui permet de surmonter ce nouveau blocage et de terminer la méiose.
Des expériences ont permis de mettre en évidence deux activités dans les cellules : l’activité MPF (Maturation Promoting Factor) et l’activité CSF (CytoStatic Factor).

Les molécules associées ont été identifiées : l’activité MPF est celle du complexe cycline B-Cdk1 tandis que l’activité CSF est celle de la kinase Mos ainsi que de Cdk2. Ces kinases inhibent le complexe APC/C qui est indispensable pour que les cellules quittent la métaphase (voir le chapitre sur le contrôle du cycle cellulaire).
> L’ovogénèse est suivie par la fécondation.
LA CARTE MENTALE
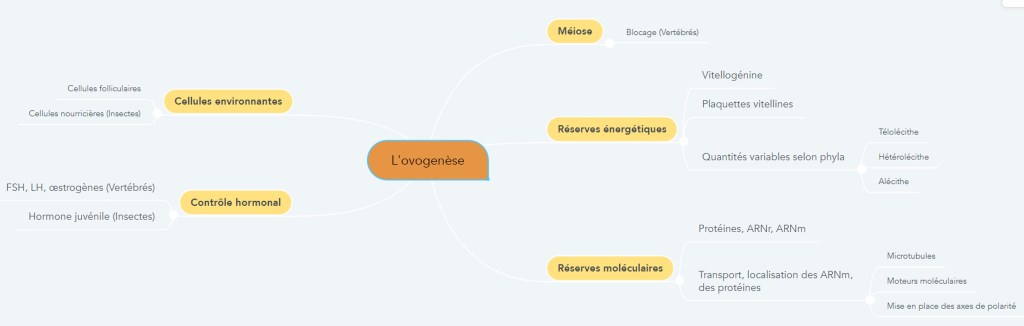
LES MOTS CROISES POUR REVISER :

QUIZZ :
Il peut y avoir plusieurs bonnes réponses par question. Les réponses se trouvent tout en bas de la page.
1* Quel organe des vertébrés est principalement responsable de la production de vitellogénine ?
A) Le foie
B) Les ovaires
C) L’utérus
D) Le pancréas
2* Chez les amphibiens, où se trouvent concentrés les granules de mélanine dans les ovocytes ?
A) Au pôle végétatif
B) Au pôle animal
C) Dans l’hémisphère végétatif
D) Dans l’hémisphère animal
3* Quelle(s) hormone(s) provoque(nt) l’ovulation chez les mammifères ?
A) Les oestrogènes
B) La LH
C) La progestérone
D) La FSH
4* Quelle protéine des jonctions gap est indispensable à la fertilité chez les mammifères en permettant la communication entre l’ovocyte et les cellules de la corona radiata ?
A) La E-cadhérine
B) La connexine 37
C) La connexine 43
D) La glycoprotéine ZP3
5* Comment appelle-t-on les ovocytes possédant une quantité massive de vitellus qui empêche la cellularisation complète lors du développement ?
A) Ovocytes hétérolécithes
B) Ovocytes télolécithes
C) Ovocytes oligolécithes
D) Ovocytes alécithes
QUESTION DE SYNTHESE :
Comment les interactions entre l’ovocyte et les cellules folliculaires influencent-elles le développement ?
La réponse se trouve tout en bas de la page.
QUELQUES EQUIPES FRANCOPHONES QUI TRAVAILLENT SUR LE SUJET :
Equipe « Evolution et développement des cellules germinales » – Collège de France, Paris
Vers le GLOSSAIRE
- Adhérences cellule-cellule
- Arabidopsis thaliana
- Axe antéro-postérieur chez la drosophile
- Biomécanique du développement
- Caenorhabditis elegans
- Concepts principaux
- Contrôle de la traduction
- Contrôle de la transcription
- Contrôle génétique et épigénétique
- Croissance du tube pollinique et double fécondation chez les Angiospermes
- Croissance et guidage axonal
- Des modèles animaux moins classiques
- Développement de l’oeil des Vertébrés
- Développement et évolution
- Et l’Humain ?
- Exercices sur l’ovogenèse, la spermatogenèse et la fécondation
- Exercices sur le contrôle de l’expression des gènes
- Exercices sur le développement des bourgeons de membre
- Exercices sur le développement des muscles striés squelettiques
- Exercices sur le développement des végétaux et les hormones végétales
- Exercices sur les cycles et les divisions cellulaires
- Exercices sur les étapes du développement, les inductions embryonnaires et la mise en place des axes de polarité
- Exercices sur les matrices extracellulaires, le cytosquelette et les adhérences cellule-cellule
- Exercices sur les voies de signalisation
- Glossaire
- Glossaire des termes liés à la génétique
- Glossaire des termes liés au cytosquelette, la matrice extracellulaire, l’adhérence et la migration cellulaire
- Hématopoïèse et développement des cellules du système immunitaire
- Histoire de la biologie cellulaire et de la biologie du développement
- L’acide rétinoïque
- L’apoptose
- L’autophagie
- L’organogenèse
- La drosophile
- La fécondation
- La formation des somites
- La gastrulation
- La gastrulation (version allégée)
- La métamorphose chez les Hexapodes et les Amphibiens
- La neurogénèse chez les mammifères adultes
- La neurulation
- La poule
- La signalisation calcique
- La souris
- La superfamille TGFβ et ses voies de signalisation
- La voie de signalisation de l’auxine et ses rôles
- La voie de signalisation Hedgehog
- La voie de signalisation Hippo et ses composants YAP/TAZ
- La voie de signalisation Notch
- Le clivage
- Le cytosquelette
- Le destin des cellules et les réseaux de régulation génique
- Le développement des bourgeons de membre
- Le développement des muscles striés squelettiques
- Le développement des organes génitaux et des cellules germinales
- Le développement du cortex
- Le méristème apical caulinaire en phase végétative et lors de la formation d’une fleur
- Le poisson zèbre
- Le xénope
- Les cellules des crêtes neurales
- Les cellules et les gènes en action dans le développement
- Les cellules souches
- Les cellules tumorales
- Les cycles et les divisions cellulaires
- Les étapes du développement
- Les étapes du développement embryonnaire d’Arabidopsis thaliana et leur contrôle
- Les inductions embryonnaires et les gradients de morphogène
- Les matrices extracellulaires animales
- Les organismes modèles
- Les outils pour étudier l’expression et la fonction des gènes
- Les parois des cellules végétales
- Les techniques et les outils pour la biologie cellulaire
- Les transitions épithélio-mésenchymateuses et les migrations cellulaires
- Les vésicules extracellulaires
- Les voies de signalisation
- Les voies de signalisation FGF
- Mise en place des axes chez les Vertébrés
- Structures et processus cellulaires
- Voies de signalisation WNT
REPONSES AU QUIZZ :
1A; 2D; 3B; 4B; 5B
REPONSE A LA QUESTION DE SYNTHESE :
Les interactions entre l’ovocyte et les cellules folliculaires sont marquées par une interdépendance étroite qui conditionne non seulement la maturation du gamète femelle, mais aussi la viabilité et l’organisation du futur embryon.
I) Soutien métabolique et survie cellulaire
Chez les mammifères, l’ovocyte et les cellules de la corona radiata maintiennent un contact physique étroit malgré l’épaisseur de la zone pellucide grâce à des projections cytoplasmiques transzonales et des jonctions gap.
Nutrition de l’ovocyte : Les ovocytes ne peuvent pas métaboliser le glucose par eux-mêmes. Les cellules folliculaires environnantes leur fournissent donc du pyruvate et du lactate via les jonctions gap (impliquant la connexine 37).
II) Maturation de l’ovocyte
Production d’œstrogènes : Sous l’influence de la FSH, les cellules de la granulosa produisent des œstrogènes nécessaires à la maturation de l’ovocyte.
Facilitation de l’ovulation : Suite au pic de LH, les cellules de la corona radiata sécrètent de l’acide hyaluronique pour favoriser l’expulsion de l’ovocyte
III) Contrôle du cycle cellulaire
Régulation de la méiose : Les jonctions gap permettent de réguler les taux d’AMPc et de GMPc entre les cellules. Au moment de l’ovulation, la diminution de ces jonctions permet la reprise de la méiose dans l’ovocyte lors de l’ovulation.
IV) Protection de l’ovocyte et de l’embryon
Les cellules folliculaires sécrètent des structures protectrices comme la membrane vitelline et le chorion chez les insectes, qui protègent l’ovocyte puis l’embryon. Chez les mammifères, elles participent à la formation de la zone pellucide, composée de glycoprotéines (ZP1 à ZP4), qui joue le rôle de matrice extracellulaire de l’ovocyte et interagit avec les spermatozoïdes. La zone pellucide modifiée par les enzymes des granules corticaux après leur exocytose devient la membrane de fécondation (ou membrane vitelline) qui protège l’embryon.
V) Mise en place des axes de polarité de l’embryon
Les interactions cellules folliculaires-ovocyte contrôlent les axes de polarité du futur embryon surtout chez la drosophile, mais pas chez les Mammifères.
Induction de l’axe antéro-postérieur : L’ovocyte, par la voie de signalisation Gurken/Torpedo, induit les cellules folliculaires adjacentes à adopter un destin postérieur.
Signal en retour : Ces cellules folliculaires postérieures envoient ensuite un signal à l’ovocyte pour polariser ses microtubules le long de ce qui deviendra l’axe antéro-postérieur de l’embryon. Cette réorganisation dépend de l’activité de la protéine kinase A (PKA).
Différenciation nécessaire : Pour que ce dialogue fonctionne, les cellules folliculaires doivent être correctement différenciées via l’interaction Delta-Notch ; si cette voie est altérée, l’axe de l’embryon est gravement perturbé.
D’une manière similaire, un dialogue moléculaire existe aussi entre les cellules folliculaires et l’ovocyte pour la mise en place de l’axe dorso-ventral de la drosophile par la mise en place du gradient d’expression de Dorsal (exprimé plus fortement dans la future région ventrale).
