Par Patrick Pla, Université Paris-Saclay
Comment et quand les cellules d’un organisme en développement savent ce qu’elles sont (identité) et où elles se trouvent (information de position), sont des questions les plus fondamentales en biologie du développement. Chez les organismes pluricellulaires, chaque cellule a une structure particulière associée à une fonction spécifique et occupe une position précise. Les cellules doivent donc interpréter les signaux positionnels qui les orientent vers leur destin. La structure des espèces a varié au cours de l’évolution et celle-ci a la possibilité d’agir à la fois sur les «signaux» et sur la machinerie qui exécute «l’interprétation» de ces signaux.
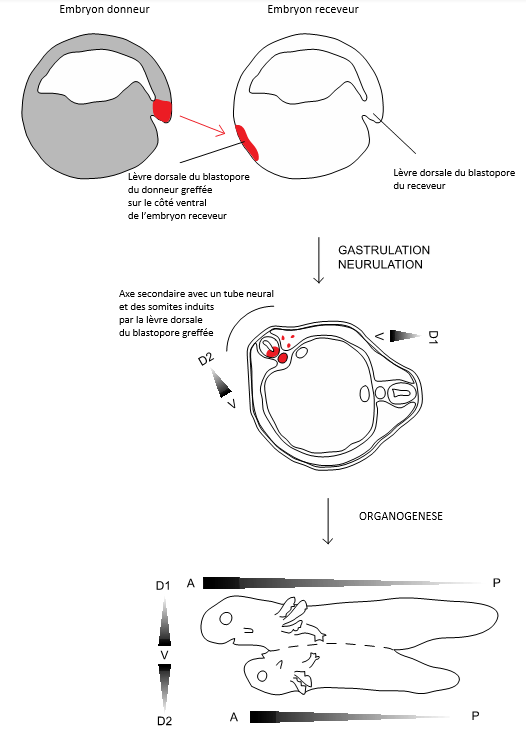
L’idée que les cellules adoptent des destins différents en détectant la présence ou l’absence de produits chimiques, appelés facteurs déterminants du destin ou «déterminants» remonte au début du XXème siècle. Cependant, l’expérience qui a permis de cimenter l’idée qu’une population de cellules peut contrôler le destin d’autres cellules est celle de Spemann et Mangold en 1924. La transplantation de la lèvre dorsale du blastopore d’un embryon d’amphibien sur la région ventrale d’un autre embryon induit la formation d’un nouveau tube neural et de nouvelles structures mésodermiques dorsales. Les cellules du greffon n’ont que marginalement participées à ces nouvelles structures : il s’agit bien d’une instruction envoyée par un groupe de cellules à un autre groupe de cellules qui a changé sa destinée. C’est une induction embryonnaire.

Les expériences de Boveri sur des embryons d’oursins en 1901 ont montré que les modèles de développement pourraient être déterminés par des gradients opposés, tandis que des expériences de régénération sur des planaires en 1904 postulaient l’existence de « substances formatrices » qui influencent le plan de développement de l’embryon. En 1952, Alan Turing a postulé que des concentrations de produits chimiques spécifiques, appelés « morphogènes », pourraient instruire le destin des cellules et donc l’organogenèse dans un organisme en développement.

Après avoir déchiffré le code de la machine allemande Enigma au cours de la seconde guerre mondiale, Turing s’est intéressé à en 1952 aux équations de réaction-diffusion, puis a élaboré un modèle biomathématique de la morphogenèse, applicable aux animaux ou aux végétaux. Il fait paraître un article à ce sujet, «The Chemical Basis of Morphogenesis» (Philosophical Transactions of the Royal Society, août 1952). Vous pouvez lire cet article ici : https://www.dna.caltech.edu/courses/cs191/paperscs191/turing.pdf
Dans les années 1990, des expériences de chimie confirment expérimentalement les modèles théoriques de Turing.
La prochaine étape épistémologique était l’inclusion de l’espace et la notion selon laquelle les gradients de produits chimiques conduisent à la structuration du développement et à la différenciation cellulaire. Le moment-clé associé à cette idée est constitué par un événement de rupture de la symétrie initiale, souvent déclenché par des facteurs asymétriquement localisés ou orientés (et ce sont souvent les microtubules et leur polarité +/- qui sont les déclencheurs). Par exemple, les morphogènes sont produits dans des cellules qui sont situées dans des régions spatialement restreintes et ils diffusent le long d’un axe d’un embryon ou d’un tissu, établissant ainsi un gradient. Il s’agit de communication paracrine, qui est le mode de communication intercellulaire principal dans les embryons précoces (les systèmes circulatoires et nerveux n’étant pas encore formés). En 1969, Lewis Wolpert a postulé que les cellules pouvaient déterminer leur destin en interprétant les concentrations locales de ces profils gradués, et il a inventé la notion abstraite selon laquelle ces profils contiennent des «informations de position». C’est ce qui a mené à son célèbre modèle du «drapeau français».
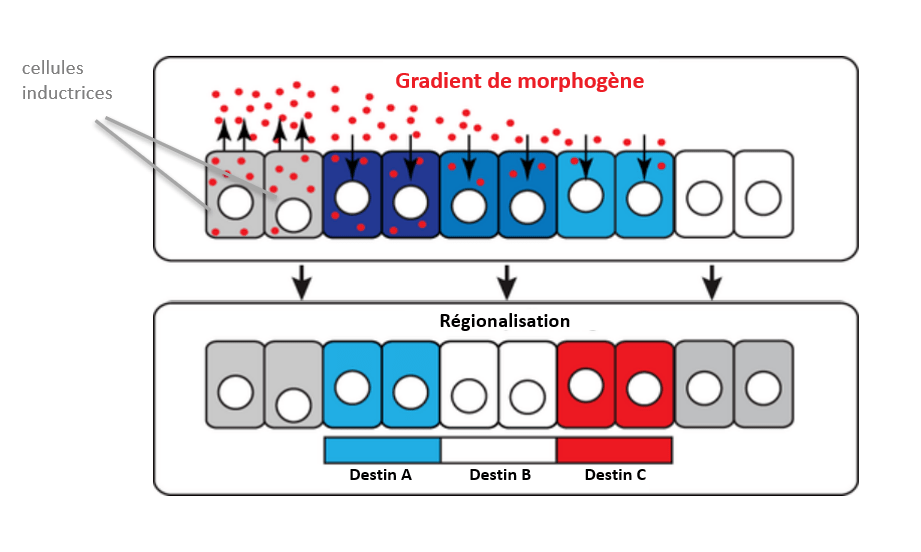
Ici, des groupes adjacents de cellules sont délimités par un seuil de concentration, qui définit une limite. La détermination du destin dans ce modèle est due à l’interprétation par les cellules de la concentration du morphogène. L’information est donc contenue dans la valeur de la concentration à une position donnée, et dans la cascade moléculaire qui transforme cette valeur en réponse cellulaire. Ainsi, les concentrations de morphogène de deux gradients orthogonaux agissent comme des coordonnées de position, définissant une carte de destin spatial bidimensionnelle comme pour les longitudes et les latitudes. Les cellules individuelles mesurent et interprètent la concentration locale de morphogène et déterminent le choix de destin approprié pour cette position.
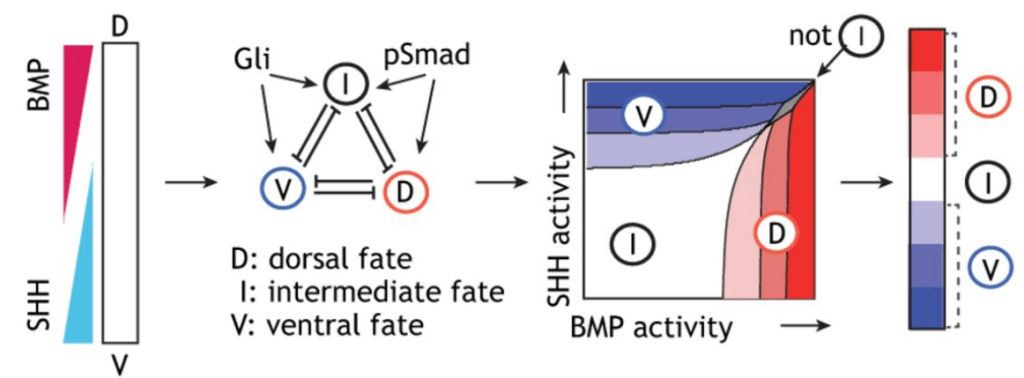
Egalement, il arrive souvent que deux gradients de morphogènes s’opposent le long d’un même axe permettant de raffiner la différenciation des destins le long de cet axe. Citons par exemple, les gradients opposés de SHH et de BMP le long de l’axe dorso-ventral du tube neural.
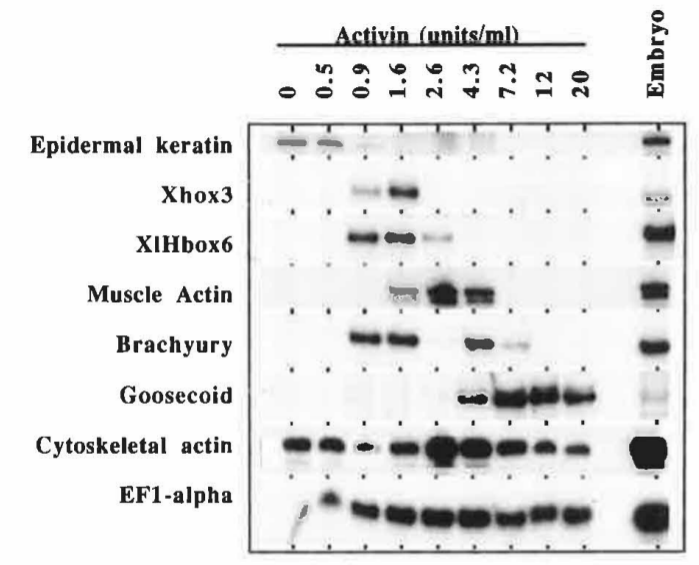
En 1989, soit 20 ans après le modèle de Wolpert, la première molécule de morphogène a finalement été découverte, la protéine Bicoid dans l’embryon de drosophile qui présentait toutes les caractéristiques du concept de Wolpert (Driever et Nüsslein-Volhard, 1988). Cette découverte a été immédiatement suivie par la démonstration qu’un ligand de la famille des TGFbeta, l’activine, détermine les destins différentiels des cellules en fonction des seuils de concentration (Green et al., 1992). Par la suite, de nombreux autres morphogènes porteurs d’information de position ont été découverts.
Les morphogènes sont donc des molécules distribuées de manière graduée qui fournissent des indices de position pour la spécification du destin cellulaire au cours du développement (Rogers et Schier, 2011). En général, les morphogènes sont des protéines excrétées, produites à partir de sources localisées et qui diffusent dans l’espace extracellulaire vers les cellules voisines. Signalons que l’acide rétinoïque (c’est un dérivé de la vitamine A) n’est pas une protéine mais agit souvent comme un morphogène.
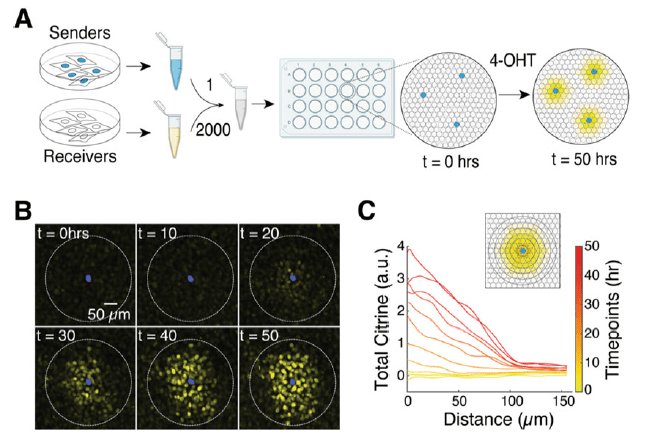
Une version commentée de cette figure est disponible en vidéo.
Source : https://doi.org/10.1007/978-1-0716-1174-6
Une fois que les gradients sont formés, les cellules réceptrices interprètent leur position respective dans le tissu en détectant la concentration de morphogènes. En réponse, les cellules activent différents ensembles de gènes cibles, initiant ainsi des processus de détermination et définissant finalement le destin des cellules. Chez les embryons de drosophile, deux morphogènes, dorsal (Dl) et bicoid (Bcd), contrôlent la mise en place de deux axes corporels: respectivement dorso-ventral et antéro-postérieur. Ces morphogènes spécifiques sont inhabituels car ce sont des facteurs de transcription et ils agissent directement dans les noyaux avant la cellularisation de l’embryon de drosophile; par conséquent, les réponses de leurs gènes cibles ne reposent pas sur de vastes cascades de signalisation intracellulaire, mais sur une action directe de ces morphogènes. Ils constituent ainsi un modèle d’étude de choix pour comprendre le couplage morphogène-régulation transcriptionnelle.
Voir le chapitre sur l’action de bicoid.
L’un des principaux problèmes étudiés en ce qui concerne les morphogènes est le mécanisme par lequel leurs diverses concentrations sont traduites en expressions géniques différentielles. L’un des premiers modèles a proposé que les différences dans les domaines d’expression spatiale des gènes cibles sont directement liées à la concentration de morphogène (Wolpert, 1969). Dans ce modèle, la transcription du gène cible est initiée uniquement lorsque la concentration de morphogène est au-dessus d’un certain seuil, alors que la transcription n’est pas initiée dans les domaines où la concentration de morphogène est présente en dessous. De cette manière, les gradients de morphogènes régulent la spécification dans un groupe de cellules en contrôlant de manière différentielle l’expression génique.
Ce modèle est enrichi en considérant l’importance du temps, à la fois le moment de commencement de l’exposition aux morphogènes et sa durée (Rogers et Schier, 2011; Sagner et Briscoe, 2017). L’expression du gène cible influencée par l’apport de morphogène dépend aussi de l’état d’expression génique des cellules réceptrices. Les réponses à un morphogène donné différeront entre les cellules réceptrices avec différents programmes d’expression génique pré-existants. On dira de ces cellules qu’elles ont des compétences différentes à répondre au morphogène. Par exemple, lors de la régionalisation dorsale-ventrale des embryons de poisson zèbre en gastrulation, le sort des cellules est spécifié de manière progressive dans le temps en raison des changements dans la sensibilité des tissus cibles au ligand BMP. La signalisation BMP pendant la gastrulation précoce active la mise en place des domaines ventrolatéraux antérieurs, tandis que plus tard, le même signal favorise la mise en place des domaines ventrolatéraux postérieurs (Tucker et al., 2008). Dans un autre exemple, le développement de l’œil est dépendant de l’expression de Pax6. Des expansions latérales du tube neural appelées vésicules optiques induisent l’ectoderme en surface à donner le cristallin. Or Pax6 est exprimé dans les deux tissus. Des expériences de recombinaison ont été réalisées entre vésicules optiques et ectoderme de surface provenant soit d’une souris sauvage, soit d’une souris Pax6-/-.

Ces résultats montrent que pour qu’il y ait induction du cristallin, il faut que le tissu cible de l’induction, l’ectoderme de surface exprime Pax6 et que l’expression de Pax6 n’est pas indispensable dans le tissu inducteur. Cela veut dire que Pax6 contrôle la compétence de l’ectoderme de surface à recevoir les signaux en provenance des vésicules optiques.
Au cœur de la notion de morphogène, se trouve le concept de gradient. Trois modalités générales de formation de gradient ont émergé : le transport actif, la diffusion libre et la diffusion régulée, dans lesquelles des molécules de liaison extracellulaire (les composants de la matrice extracellulaire par exemple) interagissent avec le ligand pour modifier sa distribution finale (Müller et al., 2013).
Il existe au moins deux mécanismes de transport actif: le transport basé sur les vésicules, notamment la transcytose et les migrasomes, dans lequel les ligands morphogènes naviguent à travers les tissus via des cycles répétés d’endo- et d’exocytose médiée par les récepteurs (González- Gaitán et Jäckle, 1999; Greco et al., 2001; Kicheva et al., 2007; Restrepo et al., 2014) et le transport médié par les cytonèmes, dans lequel de vastes réseaux de filopodes mis en place par les microfilaments d’actine agissent comme des conduits directs pour la transmission du morphogène aux cellules cibles (Ramírez-Weber et Kornberg, 1999). Il est également apparu que les cellules réceptrices peuvent envoyer des cytonèmes à la rencontre des cytonèmes qui sécrète le morphogène. C’est le cas lors de la mise en place de la polarité antéro-postérieure de l’aile de la drosophile qui dépend de Hedgehog (Gonzalez-Menendez et al., 2017). Ici, le mécanisme dominant d’action à distance n’est plus la diffusion du morphogène dans l’espace intercellulaire mais bien le transport dans les cytonèmes.
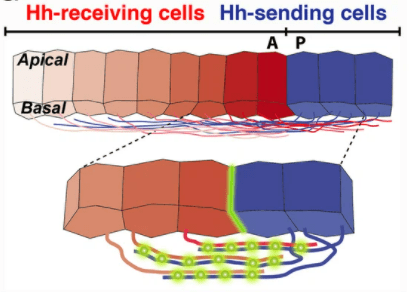
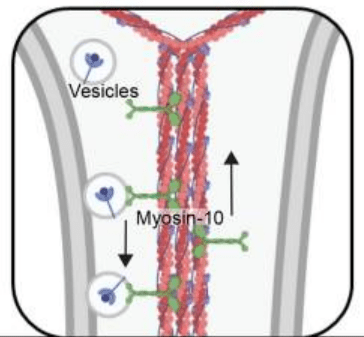
Pour la diffusion régulée et la diffusion libre, il est utile de faire la distinction entre la diffusion régulée par des facteurs immobiles, tels que les récepteurs et co-récepteurs, ainsi que les composants de la matrice extracellulaire et d’autres interactants mobiles avec les morphogènes qui ont un impact sur sa plage et sa vitesse de diffusion. La simulation de modèles mathématiques réaction-diffusion des étapes de transport et de réaction des molécules est de plus en plus utilisée pour mieux comprendre les mécanismes et les contributions relatives des facteurs mobiles et immobiles sur la formation des gradients, ce qui aurait beaucoup plu à Alan Turing.
Prenons l’exemple du gradient de BMP qui a une importance considérable pour la mise en place de l’axe dorso-ventral chez les animaux. Le principal régulateur de BMP est la protéine Chordine qui est produite à l’extrémité opposé de l’axe par rapport à la zone de production de BMP. Chordine se lie à BMP dans l’espace intercellulaire et l’empêche d’accéder à son récepteur. Dans le « modèle de navette », Chordine est très mobile et se lie avec une forte affinité à un dimère de ligand BMP peu diffusif et ainsi Chordine facilite la retour de BMP vers sa zone de production (Ben-Zvi et al., 2014). La métalloprotéase conservée Tolloid clive Chordine, libérant le ligand BMP qui peut se lier à son récepteur. Le gradient d’action de BMP est ainsi plus étroit et avec une pente plus raide. Signalons que Noggin et Follistatine, fonctionnent de manière similaire à Chordine en se liant directement aux ligands BMP (Little et Mullins, 2006). Cependant, ils ne sont pas clivés par le traitement Tolloid et fonctionnent principalement pour bloquer la signalisation BMP dans l’organisateur dorsal (Dal-Pra et al., 2006; Khokha et al., 2005).
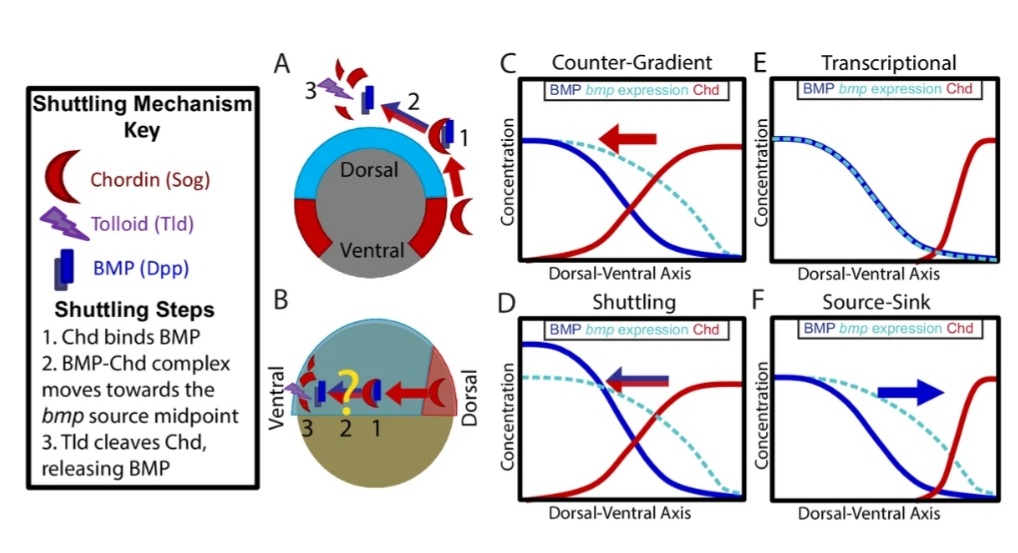
(A) Vue en coupe transversale de l’embryon de drosophile représentant la navette Sog pour Dpp (l’orthologue de BMP chez la drosophile). (B) Vue latérale d’un embryon de vertébré représentant Chordine (Chd) faisant la navette de BMP en direction de la région ventrale. (C) Contre-gradient : Chd diffuse ventralement pour former un contre-gradient réprimant le BMP. (D) Navette: BMP lié à Chd est transporté ventralement, où il est libéré par clivage Tolloid. (E) Transcriptionnel : BMP reste là où il est produit, reflétant le gradient d’expression bmp. (F) Source-puits : BMP diffuse de sa source de production ventrale à un puits de Chd dorsal. Source : https://elifesciences.org/articles/22199
Contrairement au xénope ou à la drosophile qui fonctionnent avec le modèle précédent, la formation d’un gradient de BMP dans l’embryon de poisson zèbre se produit par le biais d’un mécanisme «source-puits». Dans ce modèle, une Chordine exprimée dorsalement et à diffusion restreinte agit en liant et en séquestrant les ligands BMP dorsalement, fournissant les conditions d’un flux net de ligands BMP vers le « puits » Chordine et loin de la source BMP (Reversade et De Robertis, 2005; Zinski et al., 2017).
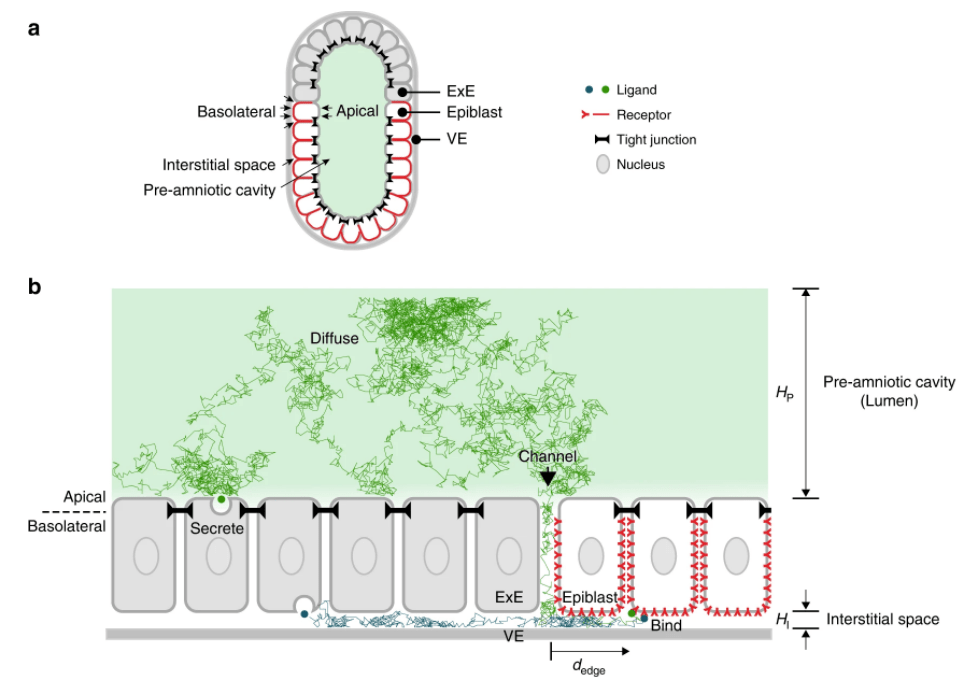
Des gradients de morphogène peuvent être également renforcés en créant un passage étroit pour le ligand. C’est le cas pour BMP lors de sa participation à l’induction du mésoderme dans l’épiblaste de souris. Il est secrété par l’ectoderme extraembryonnaire dans le liquide extracellulaire qui se trouve dans la cavité pré-amniotique. Ses récepteurs se trouvent sur le côté basolatéral de l’épithélium épiblastique. Les ligands BMP ne peuvent passer la barrière épithéliale qu’à la frontière entre l’ectoderme extraembryonnaire et l’épiblaste car il n’y a pas de jonctions serrées à cet endroit. Cela a pour conséquence de concentrer le ligand BMP sur les récepteurs des cellules de l’épiblaste près de cette frontière et de renforcer le gradient inducteur (Zhang et al., 2019).
Les motifs tissulaires, tels que les taches ou les rayures sur la peau, sont établis pendant le développement et maintenus tout au long de la vie adulte. Dans un tissu à motifs, les cellules reçoivent des signaux et acquièrent des identités en fonction de leur position. Différentes approches existent pour expliquer ces phénomènes. Premièrement, le système de structuration de Turing (Turing, 1952) propose la présence de cellules sources sécrétant des activateurs et des inhibiteurs avec différents coefficients de diffusion. En sécrétant des activateurs locaux et des inhibiteurs à longue portée, les tissus s’organisent selon un schéma dit de Turing. La peau du poisson zèbre se caractérise par une alternance de rayures dorées et argentées. Au cours du développement, les cellules pigmentées appelées mélanophores et xanthophores s’organisent selon un modèle de type Turing en ayant deux effets opposés l’un sur l’autre en fonction de la distance (Nakamasu et al., 2009). L’inhibition se produit localement, tandis que l’activation se produit sur une longue distance.
Un autre mécanisme qui peut créer des motifs est l’inhibition latérale. Un exemple bien étudié est l’inhibition latérale de Notch entre les cellules du neuroectoderme de la drosophile (Kunisch et al., 1994). Cette structuration est basée sur l’interaction du récepteur Notch et du ligand membranaire Delta sur les cellules voisines. La signalisation Notch réprime la capacité d’une cellule à devenir un neurone mais aussi à exprimer Delta, qui ne peut donc pas activer Notch dans les cellules voisines. Un modèle stable de type poivre-et-sel d’identité cellulaire apparaît dans le neuroectoderme, où les cellules pauvres en signalisation Notch (participent à la formation des neurones) sont entourées de cellules riches en signalisation Notch (ne participent pas à la formation des neurones). Voir ce chapitre sur la voie de signalisation Notch.
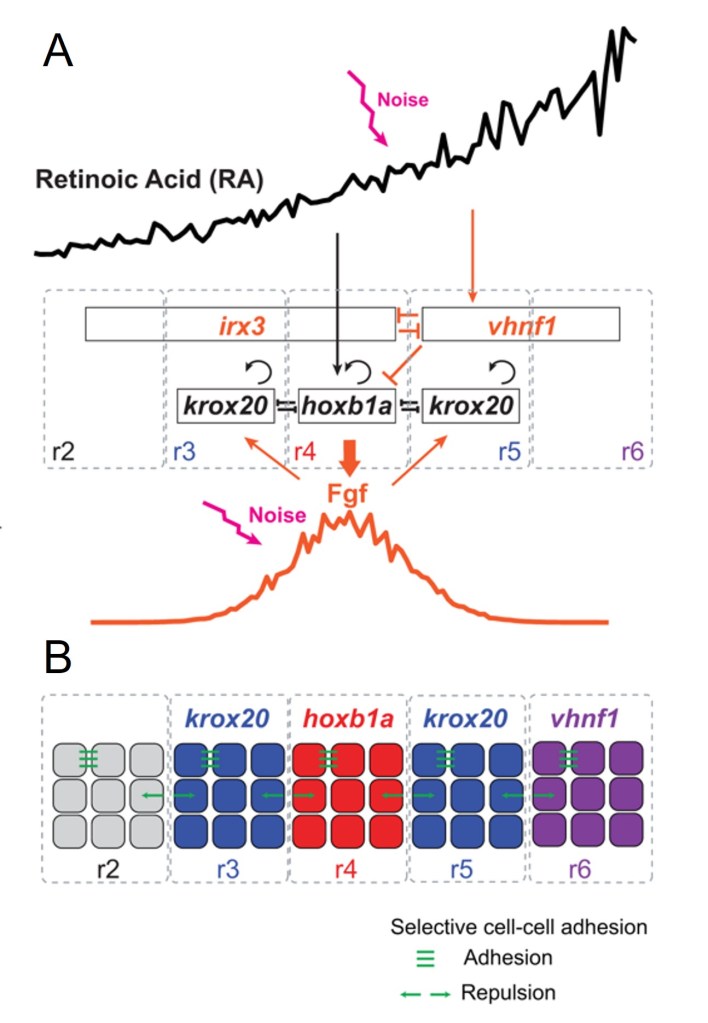
Les gradients de morphogènes activent des réseaux de régulation géniques de manière régionalisée. Ensuite, ces combinaisons de facteurs de transcription peuvent maintenir l’identité régionale même si le gradient a disparu. Des adhérences spécifiques peuvent se mettre en place à l’intérieur d’une même région et exclure un mélange des lignages par la suite. C’est ce que l’on observe par exemple lors de la régionalisation du rhombencéphale en rhombomères.
- Adhérences cellule-cellule
- Arabidopsis thaliana
- Axe antéro-postérieur chez la drosophile
- Biomécanique du développement
- Caenorhabditis elegans
- Concepts principaux
- Contrôle de la traduction
- Contrôle de la transcription
- Contrôle génétique et épigénétique
- Croissance du tube pollinique et double fécondation chez les Angiospermes
- Croissance et guidage axonal
- Des modèles animaux moins classiques
- Développement de l’oeil des Vertébrés
- Développement et évolution
- Et l’Humain ?
- Exercices sur l’ovogenèse, la spermatogenèse et la fécondation
- Exercices sur le contrôle de l’expression des gènes
- Exercices sur le développement des bourgeons de membre
- Exercices sur le développement des muscles striés squelettiques
- Exercices sur le développement des végétaux et les hormones végétales
- Exercices sur les cycles et les divisions cellulaires
- Exercices sur les étapes du développement, les inductions embryonnaires et la mise en place des axes de polarité
- Exercices sur les matrices extracellulaires, le cytosquelette et les adhérences cellule-cellule
- Exercices sur les voies de signalisation
- Glossaire
- Glossaire des termes liés à la génétique
- Glossaire des termes liés au cytosquelette, la matrice extracellulaire, l’adhérence et la migration cellulaire
- Hématopoïèse et développement des cellules du système immunitaire
- Histoire de la biologie cellulaire et de la biologie du développement
- L’acide rétinoïque
- L’apoptose
- L’autophagie
- L’organogenèse
- L’ovogénèse prépare le développement embryonnaire
- La drosophile
- La fécondation
- La formation des somites
- La gastrulation
- La gastrulation (version allégée)
- La métamorphose chez les Hexapodes et les Amphibiens
- La neurogénèse chez les mammifères adultes
- La neurulation
- La poule
- La signalisation calcique
- La souris
- La superfamille TGFβ et ses voies de signalisation
- La voie de signalisation de l’auxine et ses rôles
- La voie de signalisation Hedgehog
- La voie de signalisation Hippo et ses composants YAP/TAZ
- La voie de signalisation Notch
- Le clivage
- Le cytosquelette
- Le destin des cellules et les réseaux de régulation génique
- Le développement des bourgeons de membre
- Le développement des muscles striés squelettiques
- Le développement des organes génitaux et des cellules germinales
- Le développement du cortex
- Le méristème apical caulinaire en phase végétative et lors de la formation d’une fleur
- Le poisson zèbre
- Le xénope
- Les cellules des crêtes neurales
- Les cellules et les gènes en action dans le développement
- Les cellules souches
- Les cellules tumorales
- Les cycles et les divisions cellulaires
- Les étapes du développement
- Les étapes du développement embryonnaire d’Arabidopsis thaliana et leur contrôle
- Les matrices extracellulaires animales
- Les organismes modèles
- Les outils pour étudier l’expression et la fonction des gènes
- Les parois des cellules végétales
- Les techniques et les outils pour la biologie cellulaire
- Les transitions épithélio-mésenchymateuses et les migrations cellulaires
- Les vésicules extracellulaires
- Les voies de signalisation
- Les voies de signalisation FGF
- Mise en place des axes chez les Vertébrés
- Structures et processus cellulaires
- Voies de signalisation WNT
