Par Patrick Pla, Université Paris-Saclay

L’extraordinaire diversité des organismes y compris dans un même phylum (les Mammifères Euthériens de la chauve-souris à la baleine en passant par le pangolin) prend son origine dans le développement embryonnaire (et post-embryonnaire pour des espèces qui se métamorphosent). Cela tient aux propriétés des réseaux de régulation génique : ils présentent des degrés de liberté importants laissant la place à des innovations mutationnelles tout en restant robuste ce qui permet d’assurer la survie des « monstres prometteurs » qui seront sélectionnés dans un environnement adéquat.
Etudions un exemple (voir cet exemple présenté en vidéo) : l’épinoche de mer Gasterosteus aculeatus possède des nageoires pelviennes transformées en épines qui lui permettent de se protéger contre des prédateurs mais chez les populations d’épinoche d’eau douce ces nageoires pelviennes ont disparu (contre-sélection car pas de prédateurs et des parasites peuvent s’accrocher à ces nageoires). Il a été démontré qu’une des séquences régulatrices de l’expression du gène Pitx1 qui contrôle le développement des nageoires pelviennes a été délété chez la forme d’eau douce mais que les autres séquences régulatrices qui permettent à Pitx1 d’être exprimé dans d’autres tissus où il a un rôle primordial (thymus, fosses olfactives…) sont intacts. On voit donc qu’au cours de l’évolution, la modularité des séquences régulatrices d’un gène permettent de faire disparaître son expression d’une région de l’embryon (avec des conséquences importantes (disparition des nageoires pelviennes)) sans affecter son expression dans d’autres régions qui restent inchangées.
Les mutations peuvent ainsi concerner les séquences codantes ou les séquences régulatrices, voire même la topographie de la chromatine comme cela a été mis en évidence en comparant le génome de l’Homme et de la souris (Gibertson et al., 2022).

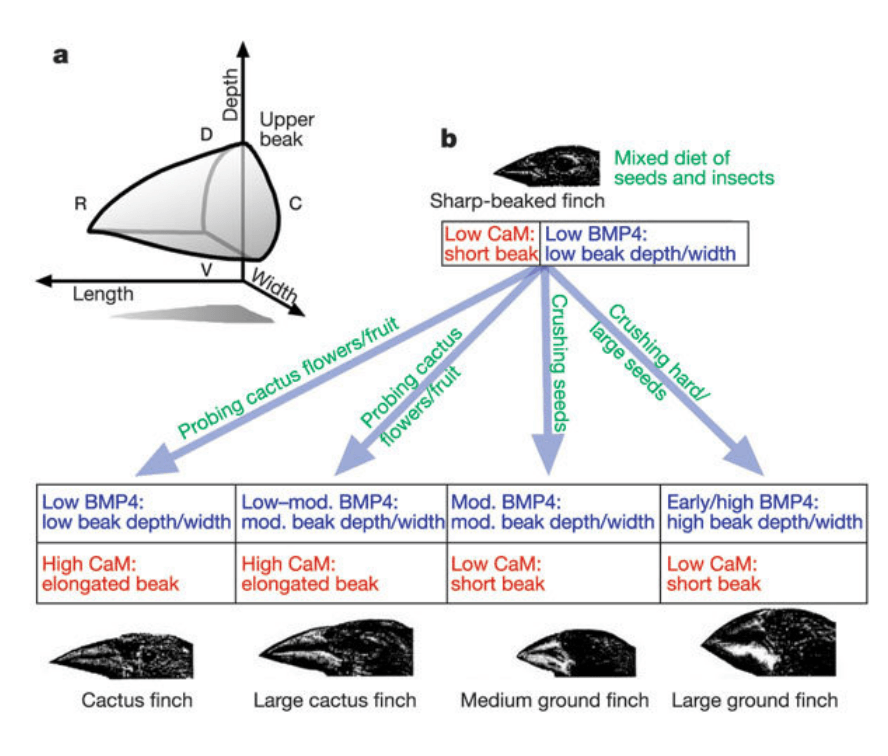
Les mutations sélectionnées peuvent modifier un réseau de régulation génique ou peuvent être plus subtiles telles des modifications quantitatives de l’expression des gènes. Par exemple, la diversité de la taille des becs des pinsons de Darwin des îles Galapagos dépend du niveau d’expression de BMP4. La manipulation du niveau d’activité de la voie BMP4 chez l’embryon de poulet aboutit à des modifications morphologiques du bec cohérentes avec ce modèle (plus BMP4 est exprimé, plus le bec est gros) (Abzhanov et al., 2004). Le niveau d’expression de la calmoduline est également impliqué dans le contrôle de la longueur du bec (Abzhanov et al., 2006).
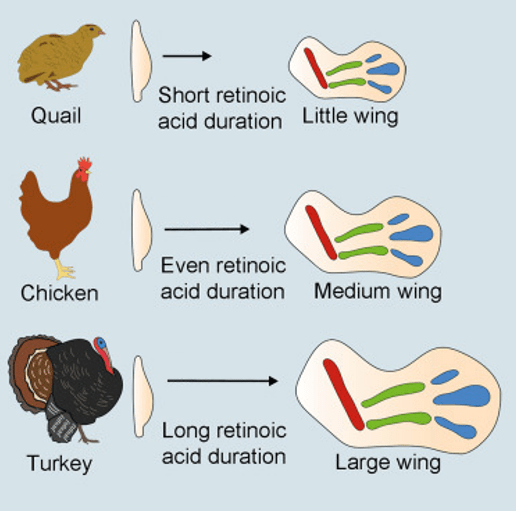
Le rythme de déroulement du programme génétique du développement peut aussi être un paramètre affecté au cours de l’évolution. Par exemple, la comparaison de la formation des somites chez l’embryon de poulet et chez l’embryon de python montre que le rythme de l’horloge interne du mésoderme présomitique est quatre fois plus rapide chez le python, expliquant le nombre très élevé de somites (et donc de vertèbres) produits (Gomez et al., 2008). Autre exemple, en comparant la formation de l’aile de la caille, du poulet et du dindon, on se rend compte que le temps d’action de l’acide rétinoïque qui stimule le développement des régions proximales est différent et corrélé à la taille de l’aile. La manipulation du temps d’exposition des cellules du bourgeon de membre à l’acide rétinoïque suffit à transformer la morphologie d’une aile de caille en celle approchant une aile de poulet et de même entre une aile de poulet et une aile de dindon (Stainton et Towers, 2022).
Il n’y a pas seulement des modifications d’expression des gènes Hox qui aboutissent à des modifications de l’organisation des animaux. La séquence est également importante. Par exemple, Ubx chez les Hexapodes possède une succession d’une dizaine d’alanines dans sa partie C-terminale, derrière l’homéodomaine, qui lui permet de réprimer l’expression de Distal-less dans l’abdomen et ainsi d’inhiber la formation de pattes. Chez les autres Arthropodes, Ubx ne possède pas cette succession d’alanines et Distal-less n’est pas reprimé (Ronshaugen et al., 2002). Ainsi, les Crustacés par exemple ont des (petites) pattes au niveau de l’abdomen. La séquence poly-alanine est une innovation évolutive partagée chez tous les Hexapodes (synapomorphie) qui a changé leur plan d’organisation par rapport au dernier ancêtre commun des Arthropodes.
Dans le même ordre d’idée, des mutations de Hoxa11 propres aux Mammifères à placenta (excluant les Monotrèmes) lui permettent de se fixer sur un enhancer régulant la transcription du gène codant la prolactine dans l’épithélium utérin (Lynch et al., 2008). Cette production de prolactine est nécessaire à l’implantation de l’embryon et la nouvelle fonction de Hoxa11 a été clairement un préalable nécessaire à l’évolution de la gestation intra-utérine chez les Mammifères.
Cependant, il existe des limites à la modularité lorsque la pléiotropie devient trop importante. Par exemple, tous les Mammifères ont 7 vertèbres cervicales (même la girafe). Le nombre de vertèbres cervicales est déterminé par les gènes Hox. Or chez les Mammifères, les gènes Hox interviennent également dans la régulation de la prolifération. Il existe une corrélation forte entre des anomalies du nombre de vertèbres cervicales et le déclenchement de tumeurs précoces chez l’enfant. Il existe très probablement une contre-sélection importante de la variation du nombre de vertèbres cervicales, car cela implique une mutation des gènes Hox qui provoque aussi des cancers (Gallis, 2002).
Malgré tout, des homologies profondes
Malgré des différences morphologiques très importantes, l’ensemble des Bilatériens et même parfois des Eumétazoaires (Bilatériens + Cnidaires) partagent un certain nombre de réseaux de régulation géniques qui signe leur parenté malgré des centaines de millions d’années d’évolution divergentes. Par exemple, dans tout le règne animal, le développement des organes photorécepteurs est dépendant du facteur de transcription Pax6 (qui s’appelle Eyeless chez la drosophile).

L’expression du Pax6 de souris par transgénèse dans la drosophile (ou même l’expression de Pax6 du calmar) aboutit à la formation d’un oeil ectopique, mais un oeil composé de drosophile, pas un oeil de souris ou de calmar ! Cela veut dire que le facteur de transcription Pax6 « donne l’ordre » de former un oeil mais la manière de répondre à cet ordre (c’est-à-dire les gènes activés en aval) dépend de l’organisme.

Signalons tout de même qu’en aval de Pax6, le tout début de la cascade menant à la formation d’un oeil est aussi conservé avec l’activation de l’expression de sine oculis (Six chez les Vertébrés), de eyes absent (Eya1-4 chez les Vertébrés) et de dachshund (Dach chez les Vertébrés).
De manière surprenante, Pax6 et Eyeless jouent aussi un rôle essentiel dans la différenciation des cellules productrices d’insuline, dans les cellules β des îlots de Langerhans du pancréas pour Pax6 chez les Vertébrés et dans un groupe de neurones du cerveau pour Eyeless chez la drosophile. Ces deux ensembles de cellules productrices d’insuline (ou de DILP qui sont ses orthologues chez la drosophile) n’ont rien à voir embryologiquement entre eux mais le module « Pax6 contrôle les gènes codant l’insuline » a été conservé (Clements et al., 2008).
La parenté entre tous les Eumétazoaires est évidente lorsque l’on compare les gènes Hox qui jouent également un rôle chez les Cnidaires pour la régionalisation le long de l’axe oral-aboral. Ce ne sont pas seulement des gènes homologues qui sont utilisés mais on retrouve aussi la règle de colinéarité entre la position des gènes dans le génome et leur expression spatiale et temporelle dans l’embryon.
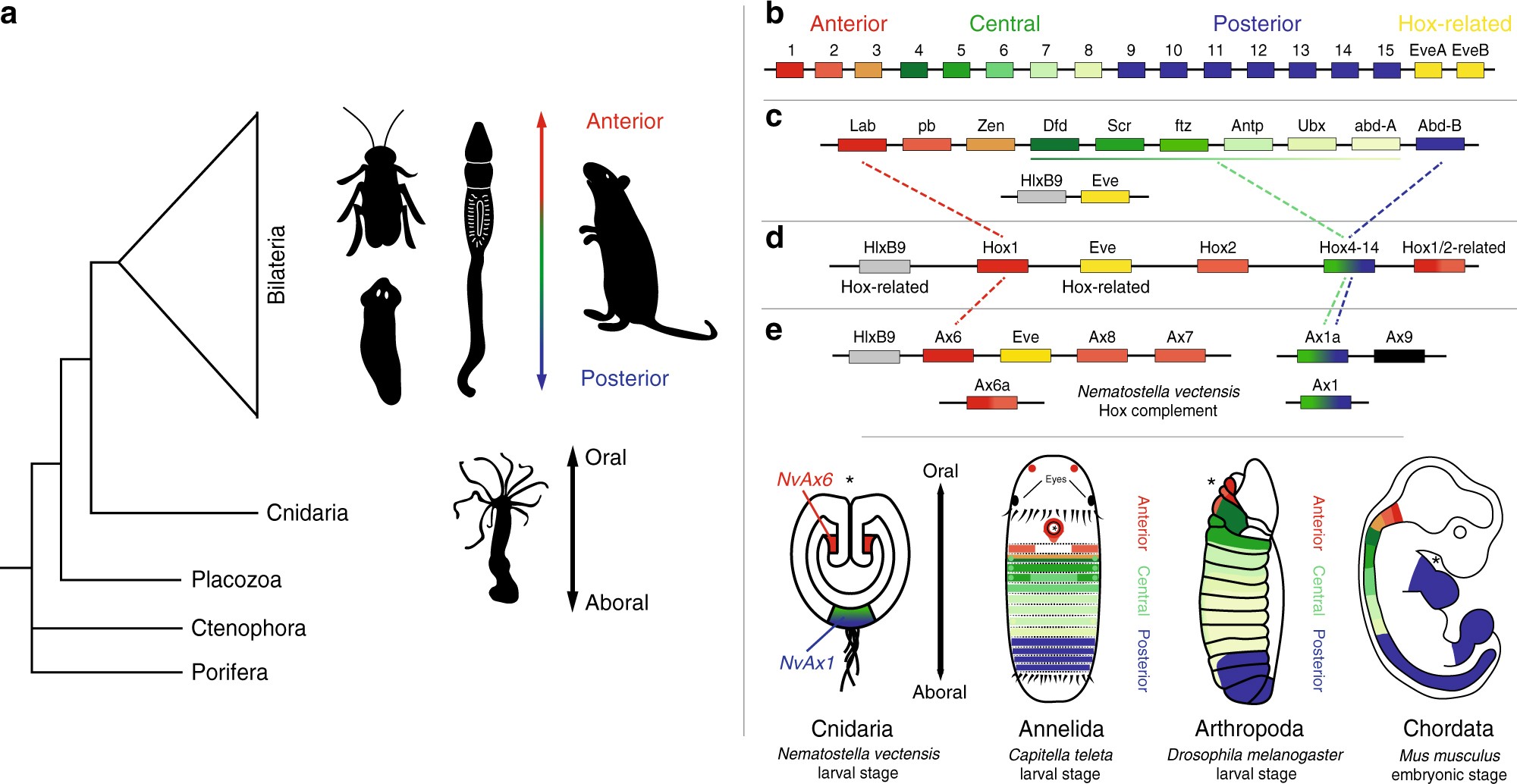
Les homologies profondes sont présentes également à des stades très précoces du développement lors de la mise en place des axes en amont des gènes Hox entre les Cnidaires et les Deutérostomiens.

Il y a aussi de fortes conservations en ce qui concerne l’axe dorso-ventral. Chordine des Vertébrés ou son orthologue Sog chez la drosophile participent à l’induction neurale en s’opposant à l’action de BMP4 des Vertébrés ou son orthologue Dpp chez la drosophile. La seule différence est une inversion dorso-ventrale : le système nerveux central est dorsal chez les Vertébrés et ventral chez les Arthropodes (à l’exception des ganglions cérébroïdes). Les patrons d’expression des différents gènes cités au-dessus sont inversés mais leur fonction demeure. On peut aussi émettre l’hypothèse que cette inversion n’est qu’apparente et que c’est plutôt la bouche, qui sert de référence pour désigner le côté ventral, qui a changé de côté.
La conservation des mécanismes au cours du développement se retrouve aussi dans les voies de signalisation qui forment des « boîtes à outils » très proches entre des phyla pourtant éloignés : voies Wnt, Hedgehog, Notch, Dpp/BMP comme nous l’avons vu et d’autres voies de signalisation.
En relation avec les stades de développement, il a été observé que le milieu du développement (correspondant à la fin de la gastrulation, à la neurulation et au début de l’organogenèse) est très conservé dans les différents phyla animaux avec des réseaux de régulation géniques assez similaires (Liu et al., 2020) et quelque fois des morphologies très semblables (chez les Vertébrés par exemple où on parle de stade phylotypique).


Il peut y avoir plusieurs origines à ce phénomène :
- toute modification dans cette période pourrait être très délétère car c’est la période où les différents signaux inducteurs sont le plus interdépendants.
- la sélection naturelle pourrait jouer plutôt au début et à la fin du développement à cause de l’adaptation aux différentes conditions du milieu.
La comparaison du transcriptome entre des embryons de drosophile à différents stades a montré que la robustesse des patrons d’expression face aux mutations est plus importante en milieu de développement (Liu et al., 2020). Ce résultat pourrait éclairé ce qu’il se passe chez les vertébrés pour le stade phylotypique.
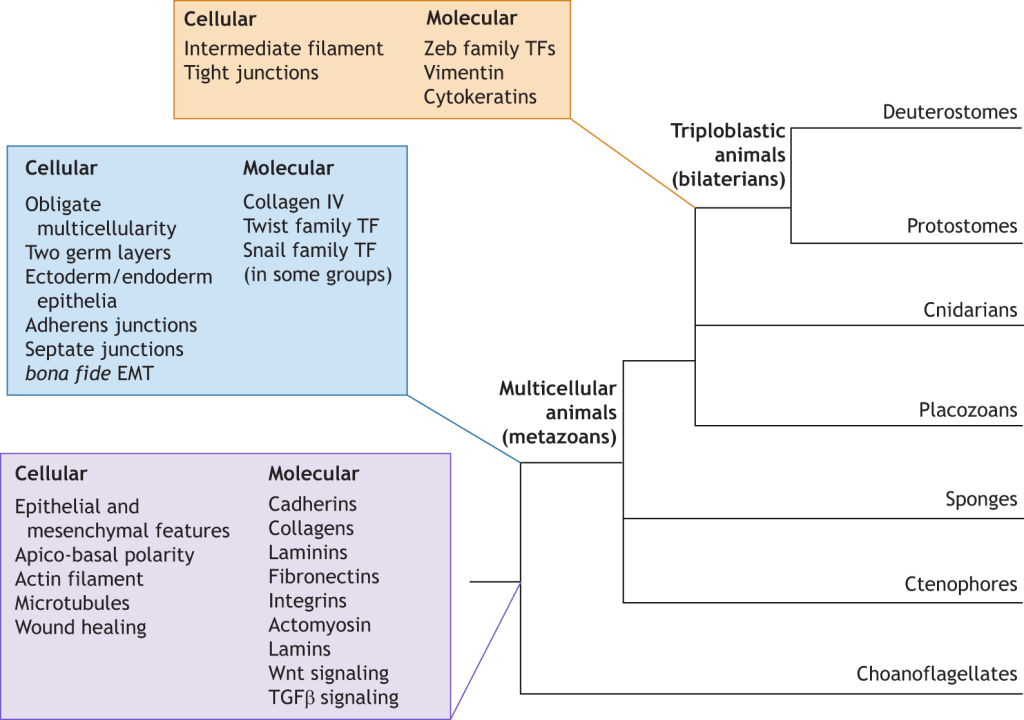
Les réseaux génétiques contrôlant les axes et la morphogénèse ont beaucoup été étudiés d’un point de vue évolutif mais l’étude de l’évolution des processus à l’achelle cellulaire est aussi un domaine très intéressant comme par exemple l’évolution de la transition épithélio-mésenchymateuse.
POUR ALLER PLUS LOIN
Vidéo de la leçon inaugurale de Denis Duboule au Collège de France :
Vidéo « parodique » expliquant les liens entre évolution et développement :
- Adhérences cellule-cellule
- Arabidopsis thaliana
- Axe antéro-postérieur chez la drosophile
- Biomécanique du développement
- Caenorhabditis elegans
- Concepts principaux
- Contrôle de la traduction
- Contrôle de la transcription
- Contrôle génétique et épigénétique
- Croissance du tube pollinique et double fécondation chez les Angiospermes
- Croissance et guidage axonal
- Des modèles animaux moins classiques
- Développement de l’oeil des Vertébrés
- Et l’Humain ?
- Exercices sur l’ovogenèse, la spermatogenèse et la fécondation
- Exercices sur le contrôle de l’expression des gènes
- Exercices sur le développement des bourgeons de membre
- Exercices sur le développement des muscles striés squelettiques
- Exercices sur le développement des végétaux et les hormones végétales
- Exercices sur les cycles et les divisions cellulaires
- Exercices sur les étapes du développement, les inductions embryonnaires et la mise en place des axes de polarité
- Exercices sur les matrices extracellulaires, le cytosquelette et les adhérences cellule-cellule
- Exercices sur les voies de signalisation
- Glossaire
- Glossaire des termes liés à la génétique
- Glossaire des termes liés au cytosquelette, la matrice extracellulaire, l’adhérence et la migration cellulaire
- Hématopoïèse et développement des cellules du système immunitaire
- Histoire de la biologie cellulaire et de la biologie du développement
- L’acide rétinoïque
- L’apoptose
- L’autophagie
- L’organogenèse
- L’ovogénèse prépare le développement embryonnaire
- La drosophile
- La fécondation
- La formation des somites
- La gastrulation
- La gastrulation (version allégée)
- La métamorphose chez les Hexapodes et les Amphibiens
- La neurogénèse chez les mammifères adultes
- La neurulation
- La poule
- La signalisation calcique
- La souris
- La superfamille TGFβ et ses voies de signalisation
- La voie de signalisation de l’auxine et ses rôles
- La voie de signalisation Hedgehog
- La voie de signalisation Hippo et ses composants YAP/TAZ
- La voie de signalisation Notch
- Le clivage
- Le cytosquelette
- Le destin des cellules et les réseaux de régulation génique
- Le développement des bourgeons de membre
- Le développement des muscles striés squelettiques
- Le développement des organes génitaux et des cellules germinales
- Le développement du cortex
- Le méristème apical caulinaire en phase végétative et lors de la formation d’une fleur
- Le poisson zèbre
- Le xénope
- Les cellules des crêtes neurales
- Les cellules et les gènes en action dans le développement
- Les cellules souches
- Les cellules tumorales
- Les cycles et les divisions cellulaires
- Les étapes du développement
- Les étapes du développement embryonnaire d’Arabidopsis thaliana et leur contrôle
- Les inductions embryonnaires et les gradients de morphogène
- Les matrices extracellulaires animales
- Les organismes modèles
- Les outils pour étudier l’expression et la fonction des gènes
- Les parois des cellules végétales
- Les techniques et les outils pour la biologie cellulaire
- Les transitions épithélio-mésenchymateuses et les migrations cellulaires
- Les vésicules extracellulaires
- Les voies de signalisation
- Les voies de signalisation FGF
- Mise en place des axes chez les Vertébrés
- Structures et processus cellulaires
- Voies de signalisation WNT
