Par Patrick Pla, Université Paris-Saclay
La neurogénèse chez l’adulte est chose courante chez les téléostéens comme le poisson-zèbre, et une douzaine de zones neurogéniques existent.
Chez les mammifères, la très grande majorité des neurones du système nerveux central est générée au cours du développement embryonnaire, et la neurogenèse postnatale est limitée à quelques régions cérébrales. C’est à la fin des années 1960 que Altman découvre qu’il existe de la neurogénèse dans la zone sous-granulaire (SGZ) du gyrus denté de l’hippocampe et dans la zone subventriculaire (SVZ) des ventricules latéraux chez les rats adultes (Kriegstein et Alvarez-Buylla, 2009). Cela correspond à la production de 30.000 neuroblastes par jour pour la zone subventriculaire et de 10.000 neuroblastes par jour pour le gyrus denté. D’autres régions sont suspectées d’abriter également de la neurogenèse chez l’adulte, par exemple les amygdales (Roeder et al., 2022).
SOMMAIRE :
Les cellules précurseurs des oligodendrocytes (OPC) sont des progéniteurs proliférants reconnaissables à leur expression de NG2, qui résident dans de vastes zones du SNC, avec une densité cellulaire d’environ 50% plus élevée dans la substance blanche par rapport à la substance grise (Dawson et al. 2003). En dehors des régions réduites de neurogenèse chez les Mammifères adultes, les OPC forment la principale population de cellules en division active dans le cerveau adulte. Les OPC de substance blanche ont des temps de cycle cellulaire plus rapides. La prolifération des OPC entraîne un auto-renouvellement ainsi que la production des cellules-filles donnant naissance à des oligodendrocytes myélinisants (Bergles and Richardson, 2016). La prolifération puis la différenciation des OPC et de leurs cellules-filles sont sous le contrôle de l’activité neurale locale, permettant d’avoir un niveau optimal de gaines de myéline (Hughes et al., 2018).
Neurogénèse adulte dans la SVZ
Pour étudier le développement du cortex chez l’embryon,
voir cette page.
Les cellules issues des cellules souches de la SVZ prolifèrent en tant que progéniteurs puis migrent dans le bulbe olfactif où ils se différencient essentiellement en neurones GABAergiques et aussi en neurones glutamatergiques (Brill et al., 2009; Tufo et al., 2022).
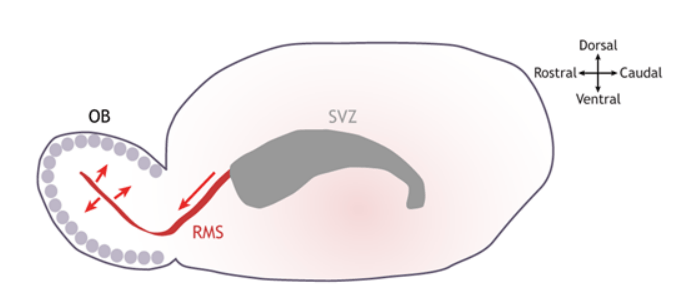
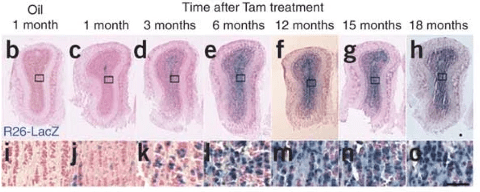
Une version commentée de cette figure est disponible en vidéo.
Source : https://www.nature.com/articles/nn.2185
Ces nouveaux neurones contribuent à la fois au maintien et au recâblage des circuits neuronaux existants, ainsi qu’aux fonctions cognitives et comportements innés associés (Imayoshi et al., 2008; Bond et al., 2015). Chez les jeunes animaux, des neuroblastes peuvent aussi migrer dans d’autres régions du cortex, dans le striatum et dans le noyau accumbens (Inta et al., 2008).
La plupart des cellules souches neurales adultes dans la paroi latérale de la SVZ sont dérivées d’une sous-population de cellules souches neurales embryonnaires en quiescence ou à division lente (tandis que la sous-population à division rapide donne naissance à des neurones et des cellules gliales qui peuplent le cerveau pendant le développement embryonnaire ou juste après la naissance) (Fuentealba et al., 2015). Une expression élevée de l’inhibiteur de CDK (CKI) p57 dans la sous-population à division lente inhibe la prolifération et la différenciation neurale et est nécessaire à la genèse des cellules souches neurales adultes (Furutachi et al., 2015). La voie Notch a été impliquée dans cette régulation (Harada et al., 2021).
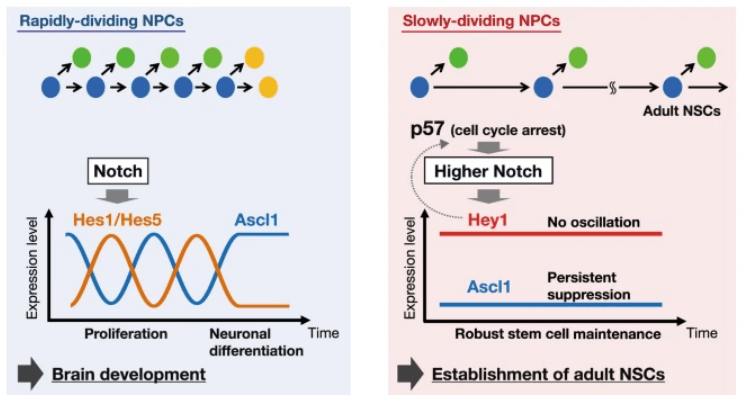
Les cellules souches neurales adultes dans la SVZ sont dites de type B. A division lente, elles produisent par division asymétrique des cellules de type C qui produisent à leur tour des neuroblastes de type A (exprimant la doublecortine (DCX)), et ceux-ci migrent en avant le long du flux migratoire rostral (RMS), se différenciant finalement en neurones qui s’intègrent dans les circuits du bulbe olfactif (Alvarez-Buylla et al., 2001).
La structure 3D de la niche des cellules souches neurales adultes (les cellules de type B) commence à être comprise. La zone germinale, qui n’a qu’environ 50 µm d’épaisseur, est prise en sandwich entre couches : du côté basal, la SVZ est délimitée par un vaste réseau planaire de vaisseaux sanguins, le plexus SVZ, et du côté apical (ventriculaire), par une couche de cellules épendymaires ciliées (Kazanis et al., 2008; Mirzadeh et al., 2008; Tavazoie et al., 2008). Une sous-population de cellules de type B a des prolongements apicaux qui pénètrent dans la couche épendymaire, et certains d’entre eux ont également un prolongement basal se projetant sur les vaisseaux sanguins du plexus SVZ (Mirzadeh et al., 2008). Ainsi, en interagissant avec la couche épendymaire, les prolongements apicaux des cellules de type B pourraient servir d’ancrage pour fournir une intégrité structurelle à la niche, et ils sont parfaitement positionnés pour détecter les changements de signaux dans le liquide céphalo-rachidien.
La protéine d’adhérence cellulaire VCAM-1 est impliqué dans le maintien des cellules souches neurales dans la zone sous-ventriculaire du télencéphale. Lorsqu’avec une micropompe, on injecte en continu pendant 6 jours des anticorps bloquant anti-VCAM dans la zone sous-ventriculaire d’une souris, la couche des cellules épendymaires qui constitue une partie de la niche des cellules souches neurales est désorganisée (Kokovay et al., 2012). Cela aboutit à augmenter la prolifération des cellules souches neurales dont une grande partie est habituellement quiescente. Dans ce système, VCAM-1 est exprimé par les cellules souches neurales. Son partenaire sur les cellules épendymales n’a pas été encore trouvé.
La voie BMP est produit par les cellules endothéliales dans la région basale de la niche alors que les cellules de l’épendyme dans la région apicale produisent Gremlin et Noggin.
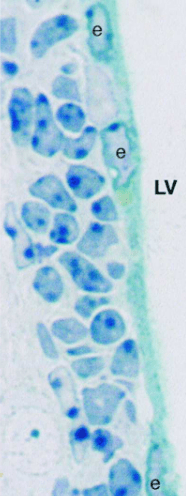
BMP pousse les cellules à perdre leur caractère de cellules souches et à devenir des cellules gliales. La niche des cellules souches neurales se trouve accolée aux cellules de l’épendyme donc elles sont protégées de l’influence de BMP par Gremlin et Noggin qui sont sécrétés localement (Lim et al., 2000). Cependant, si une cellule fille quitte la région apicale et se rapproche des cellules endothéliales de la région basale, elle subit l’influence des BMP et sera déterminée en cellule gliale.
Les précurseurs neuronaux en migration sécrètent la neurotransmetteur GABA ce qui leur permet d’activer une boucle rétroaction négative sur les cellules progénitrices en atténuant leurs taux de prolifération. En opposition à cette action, les cellules B sécrètent un inhibiteur du GABA, DBI (pour Diazepam Binding Inhibitor) pour augmenter la prolifération dans la niche (Alfonso et al. 2012).
Durant la migration dans le RMS (flux migratoire rostral) vers le bulbe olfactif, la protéine associée aux microtubules DCX (doublecortine) est importante pour maintenir la forme bipolaire des cellules et pour que la translocation nucléaire liée à la migration se réalise (Koizumi et al., 2006). Les neuroblastes sont entourés par des astrocytes particuliers qui forment des tubes gliaux indispensables à leur bonne migration (Sun et al., 2010). La migration de la SVZ vers le bulbe olfactif dure entre 2 et 6 jours (James et al., 2011).
Chez l’Homme, où l’olfaction a un rôle nettement moins important que chez les Rongeurs, il n’y a plus de neurogénèse dans la SVZ après 18 mois.
Il faut signaler que les cellules souches neurales de la SVZ de souris donnent aussi naissance à un petit nombre de cellules gliales : des oligodendrocytes du corps calleux et des progéniteurs d’oligodendrocytes qui restent à proximité (Delgado et al., 2021). L’expression du cluster de microARNs miR-17-92 dans les cellules souches neurales sorties de leur quiescence est nécessaire pour que la majorité des précurseurs générés donnent naissance à des neurones et pas à des cellules gliales (Favaloro et al., 2022).
Neurogénèse dans la SGZ de l’hippocampe
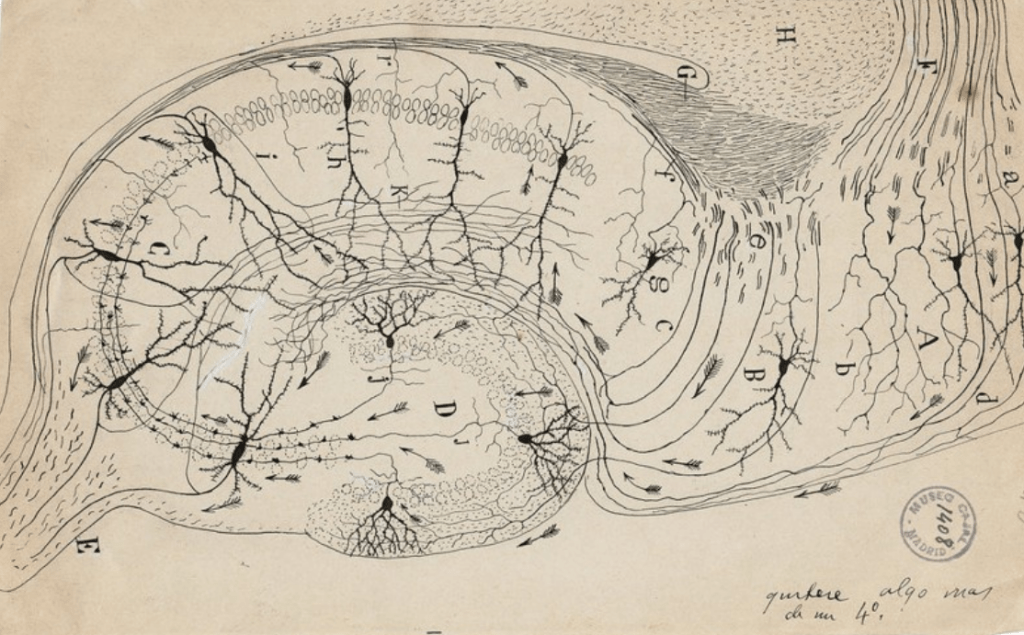

La neurogénèse se poursuit dans l’hippocampe durant toute la vie, y compris chez l’Homme (contrairement à dans la SVZ). Grâce à des mesures dans les neurones de l’hippocampe du 14C produit par les essais nucléaires et incorporés dans l’ADN au moment de la réplication des cellules souches, on a pu démontrer que 700 nouveaux neurones sont produits chaque jour dans l’hippocampe humain, mais leur durée de vie est 10 fois plus courte que celle des neurones qui sont déjà présents à la naissance.
Les cellules progénitrices neurales de la SGZ sont classées en différents stades de développement qui peuvent être identifiées par l’expression de marqueurs spécifiques. Les cellules souches neurales de type glie radiale de type 1 ont le potentiel de s’auto-renouveler et restent pour la plupart quiescentes. Ces cellules expriment la protéine de liaison aux lipides du cerveau (BLBP), la protéine acide fibrillaire gliale (GFAP) et la nestine. Un autre marqueur de cellules souches neurales largement utilisé est Sox2, un facteur de transcription essentiel au maintien de la pluripotence des cellules souches. Les cellules souches quiescentes de type 1 peuvent soit disposées radialement, soit horizontales.
Les cellules de type 1 subissent une division cellulaire asymétrique pour générer des cellules progénitrices neurales de type 2a hautement prolifératives, qui sont doublement positives pour Sox2 et Tbr2. Les cellules de type 2a génèrent ensuite des cellules progénitrices neurales de type 2b qui expriment Tbr2 et la doublecortine (DCX) (Gonçalves et al., 2016; Ming et Song, 2011 ; Spampanato et al., 2012). Les cellules de type 2b présentent un potentiel mitotique limité (Gonçalves et al., 2016), et après 2 à 5 cycles de mitose, ces cellules progénitrices se différencient en neurones immatures. Après maturation, ces nouveaux neurones granulaires s’intègrent dans les circuits.

Une version commentée de cette figure est disponible en vidéo.
Source : https://molecularneurodegeneration.biomedcentral.com/articles/10.1186/1750-1326-6-85
Dans la SGZ adulte, les neurones granulaires nouvellement générées contribuent à la formation de la mémoire (Sahay et al., 2011, Lazarov et Hollands, 2016), tout particulièrement la mémoire spatiale (Kee et al., 2007, Clelland et al., 2009) qui peut se tester chez la souris avec le dispositif de la piscine de Morris.
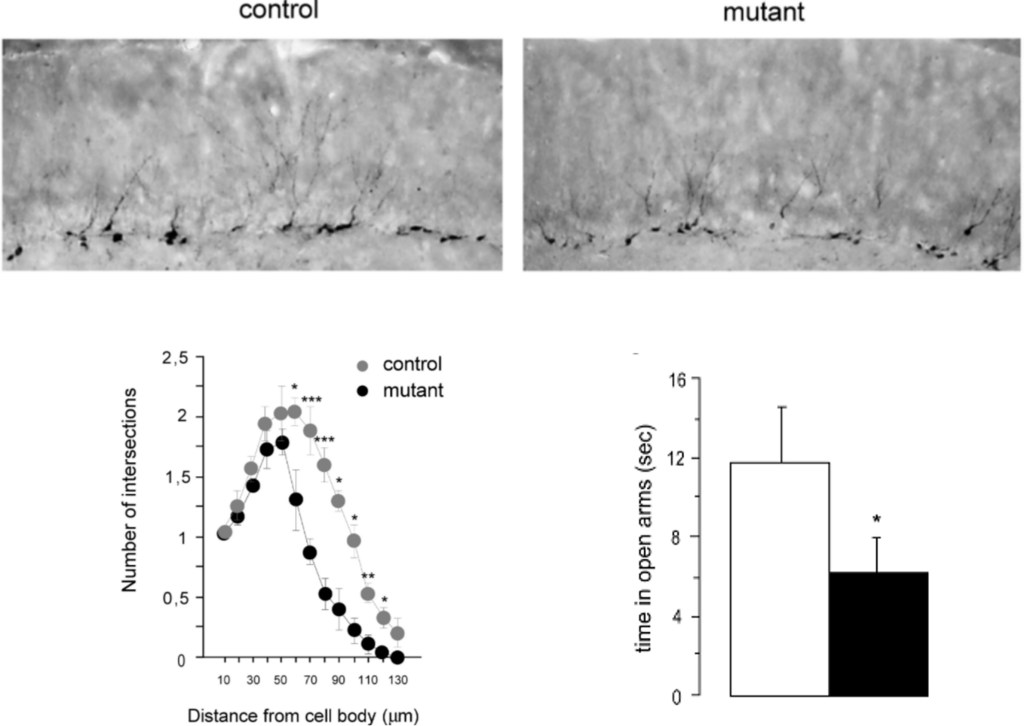
La neurogenèse dans la SGZ est également importante pour le contrôle de l’anxiété. Lorsque la maturation des nouveaux neurones est perturbée par une diminution de la sécrétion du facteur neurotrophique BDNF ou par une mutation perte-de-fonction dans le récepteur TrkB sur les nouveaux neurones, les souris sont plus anxieuses dans les tests comme le labyrinthe en croix surélevé (Bergami et al., 2008; Pla et al., 2013).
Contrairement aux précurseurs des cellules souches adultes dans la SVZ, les précurseurs des cellules souches adultes de la SGZ ne sont pas clairement « mis de côté », au repos pendant le développement embryonnaire/périnatal, mais semblent plutôt être actifs puis passer à un état de quiescence après la première postnatale où elles connaissent un pic d’activité. La suppression conditionnelle de Sufu (qui provoque une réduction de la signalisation Shh) altère la capacité des cellules souches à se développer au cours de la première semaine postnatale, ce qui entraîne l’entrée prématurée de ces cellules dans l’état de quiescence (Noguchi et al., 2019). Ces données montrent que la voie de signalisation Shh doit être maintenue en permanence pour favoriser l’expansion de cellules souches de la SGZ après la naissance. Sans cela, le pool de cellules souches est plus faible que la normale chez l’adulte.

Les inhibiteurs des CDK ont des rôles importants dans le maintien de la quiescence des cellules souches de la SGZ. Parmi eux, citons la famille Cip/Kip qui comprend p21Waf/Cip1 (appelée p21), p27Kip1 (appelée p27) et p57Kip2 (appelée p57). p27 est exprimé dans les cellules souches de type 1 et dans les souris mutantes perte-de-fonction p27 ou chez des animaux porteurs d’une perturbation dans le domaine d’interaction avec cycline-CDK de p27, il y a une augmentation de la prolifération des cellules souches adultes (Andreu et al., 2015). On ne sait pas cependant si cela entraîne l’épuisement des cellules souche avec le temps. De même, p57 est exprimé dans les cellules souches quiescentes et sa délétion spécifique dans ces cellules termine leur quiescence et active leur prolifération (Furatachi et al., 2013). Cela conduit à une augmentation du nombre de nouveaux neurones, mais à long terme (chez des animaux de 2 ans), cela conduit à une réduction excessive des cellules souches et de la neurogenèse dans l’hippocampe.
La première marque de sortie de quiescence des cellules souches neurales est l’augmentation de l’expression de gènes qui codent des protéines ribosomiques et qui participent donc à la biosynthèse des protéines. En effet, la surexpression lentivirale de certaines protéines ribosomiques est suffisante pour induire la prolifération des cellules souches adultes dans le SGZ (Mukherjee et al., 2016). L’augmentation de l’expression des gènes ribosomiques est suivie d’un changement des gènes du métabolisme énergétique de la glycolyse à la phosphorylation oxydative mitochondriale (Llorens-Bobadilla et al., 2015; Shin et al., 2015). Le métabolisme des acides gras est un régulateur important de l’activité des cellules souches et la lipogenèse de novo réalisée par l’acide gras synthase est nécessaire à leur prolifération (Knobloch et al., 2013).
L’analyse transcriptomique de Shin et al. (2015) a révélé environ 80 facteurs de transcription dont l’expression est modifiée au cours des premiers stades de la neurogenèse hippocampique adulte. Sox9, Id4 ou Id3 semblent associés à l’état de quiescence dans l’hippocampe, tandis que l’expression de Sox4 et Sox11 augmente pendant l’activation. Ce sont les mêmes profils que l’on retrouve dans la SVZ révélant la présence d’un programme génétique commun malgré les différences d’origine entre les cellules souches (Llorens-Bobadilla et al., 2015). Ascl1 est aussi un acteur majeur en commun présent dans les cellules en division (Andersen et al., 2014 ; Llorens-Bobadilla et al., 2015). Son activité est modulée par l’E3-ubiquitine ligase Huwe1 qui déstabilise la protéine Ascl1 empêchant l’accumulation de cyclines et ramenant les cellules à l’état de quiescence si besoin (Urban et al., 2016). Soutenant le rôle pivot d’Ascl1, les oscillations de son expression, qui à leur tour dépendent des oscillations de Hes1, régulent l’activation de cellules souches, tandis qu’une expression élevée de Hes1 et la suppression de Ascl1 qui en résulte favorisent la quiescence des cellules souches dans la SGZ (Sueda et al., 2019).
La neurogenèse dans l’hippocampe peut être influencée par les cytokines inflammatoires produites principalement par les cellules microgliales mais aussi par les cellules endothéliales. Par exemple, TNF-α exerce un effet régulateur complexe sur la neurogenèse hippocampique adulte via son interaction avec les récepteurs TNFR1 et TNFR2, qui exercent des fonctions opposées (Chen et Palmer, 2013). L’inactivation génétique de TNF-α (TNF−/−) ou du récepteur TNFR1 (TNFR1−/−) entraîne une augmentation de 50 % de la prolifération des cellules souches neurales (cellules BrdU+) et de 40 % de la neurogenèse (cellules DCX+) dans le gyrus denté de souris adultes, ce qui indique que la signalisation du TNFR1 supprime la différenciation neuronale, principalement en activant des voies pro-inflammatoires et apoptotiques. En revanche, les souris invalidées pour le gène codant le récepteur TNFR2 (TNFR2−/−) présentent une réduction de 30 % de la prolifération des cellules souches neurales (cellules BrdU+) et de 30 % de la neurogenèse (cellules DCX+/NeuN+) dans le gyrus denté, ce qui souligne le rôle de TNFR2 dans la promotion de la survie des cellules souches neurales et le soutien de la neurogenèse via des cascades de signalisation favorables à la croissance. Cet équilibre qui dépend des récepteurs TNFR est essentiel au maintien de l’homéostasie neurogénique dans le cerveau adulte.
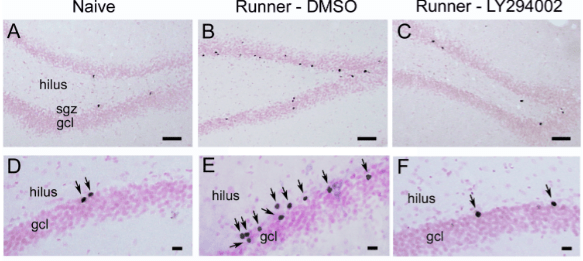
La neurogenèse dans l’hippocampe est modulée par le comportement et les pathologies d’un individu. L’exercice physique augmente cette neurogenèse tout comme les crises d’épilepsie (Lugert et al., 2010). Dans le cas de l’exercice physique, il y a une amélioration de la prolifération des cellules progénitrices et de la survie des nouveaux neurones qui dépend de la signalisation PI3kinase-Akt (Bruel-Jungerman et al., 2009).
Des facteurs circulants dans le sang comme GDF11 peuvent stimuler la neurogenèse dans l’hippocampe. Les taux de GDF11 diminuent avec l’âge mais leur supplémentation permet d’augmenter le niveau de neurogenèse chez des souris âgées et de limiter les pertes de mémoire et des diminuer les comportements de type dépressif (Moigneu et al., 2023).

La prise d’anti-dépresseur tel que le Prozac (fluoxétine) augmente la neurogenèse adulte dans l’hippocampe (Micheli et al., 2018) et celle-ci est indispensable pour que l’effet anti-dépresseur soit maximal. La fluoxétine inhibe la recapture de la sérotonine de la synapse et des neurones sérotonergiques projettent dans le gyrus dentelé de l’hippocampe où a lieu la neurogenèse adulte. Les neurones matures expriment les récepteurs 5-HT1A et 5-HT4 qui activent des voies de signalisation aboutissant à la stimulation de la neurogenèse des cellules voisines et aussi à une « dématuration » des neurones matures qui gagnent sans doute en plasticité neuronale (Segi-Nichida, 2017). Par ailleurs, les traitements anti-dépresseurs stimulent la production de BDNF et l’activation des voies de signalisation en aval du récepteur TrkB ce qui favorise la survie des nouveaux neurones dans la SGZ et contribue à l’amélioration des symptômes (Castren et al., 2010).
Lors du vieillissement, il y a une diminution de la production de nouveaux neurones par les cellules souches neurales et une proportion plus importante de cellules gliales qui est générée.

La neurogénèse dans l’hippocampe adulte est altérée de manière plus prononcée lors de la maladie d’Alzheimer. La formation de plaques amyloïdes caractéristiques de la maladie perturbe la prolifération des précurseurs et la différenciation des nouveaux neurones (Walgrave et al., 2021).
Par ailleurs, signalons que, bien que la neurogenèse du gyrus denté adulte soit principalement neuronale, les cellules souches neurales peuvent également générer des astrocytes, ce qui indique un potentiel gliogénique conservé pour ces cellules (Bonaguidi et al., 2012).
EN DIRECT DES LABOS :
QUELQUES LABOS FRANCOPHONES QUI TRAVAILLENT SUR LE SUJET :
Perception et action (Institut Pasteur, Paris)
AUTRES RESSOURCES SUR LE SUJET :
La neurogenèse adulte chez les Mammifères (Planet-Vie)
- Adhérences cellule-cellule
- Arabidopsis thaliana
- Axe antéro-postérieur chez la drosophile
- Biomécanique du développement
- Caenorhabditis elegans
- Concepts principaux
- Contrôle de la traduction
- Contrôle de la transcription
- Contrôle génétique et épigénétique
- Croissance du tube pollinique et double fécondation chez les Angiospermes
- Croissance et guidage axonal
- Des modèles animaux moins classiques
- Développement de l’oeil des Vertébrés
- Développement et évolution
- Et l’Humain ?
- Exercices sur l’ovogenèse, la spermatogenèse et la fécondation
- Exercices sur le contrôle de l’expression des gènes
- Exercices sur le développement des bourgeons de membre
- Exercices sur le développement des muscles striés squelettiques
- Exercices sur le développement des végétaux et les hormones végétales
- Exercices sur les cycles et les divisions cellulaires
- Exercices sur les étapes du développement, les inductions embryonnaires et la mise en place des axes de polarité
- Exercices sur les matrices extracellulaires, le cytosquelette et les adhérences cellule-cellule
- Exercices sur les voies de signalisation
- Glossaire
- Glossaire des termes liés à la génétique
- Glossaire des termes liés au cytosquelette, la matrice extracellulaire, l’adhérence et la migration cellulaire
- Hématopoïèse et développement des cellules du système immunitaire
- Histoire de la biologie cellulaire et de la biologie du développement
- L’acide rétinoïque
- L’apoptose
- L’autophagie
- L’organogenèse
- L’ovogénèse prépare le développement embryonnaire
- La drosophile
- La fécondation
- La formation des somites
- La gastrulation
- La gastrulation (version allégée)
- La métamorphose chez les Hexapodes et les Amphibiens
- La neurulation
- La poule
- La signalisation calcique
- La souris
- La superfamille TGFβ et ses voies de signalisation
- La voie de signalisation de l’auxine et ses rôles
- La voie de signalisation Hedgehog
- La voie de signalisation Hippo et ses composants YAP/TAZ
- La voie de signalisation Notch
- Le clivage
- Le cytosquelette
- Le destin des cellules et les réseaux de régulation génique
- Le développement des bourgeons de membre
- Le développement des muscles striés squelettiques
- Le développement des organes génitaux et des cellules germinales
- Le développement du cortex
- Le méristème apical caulinaire en phase végétative et lors de la formation d’une fleur
- Le poisson zèbre
- Le xénope
- Les cellules des crêtes neurales
- Les cellules et les gènes en action dans le développement
- Les cellules souches
- Les cellules tumorales
- Les cycles et les divisions cellulaires
- Les étapes du développement
- Les étapes du développement embryonnaire d’Arabidopsis thaliana et leur contrôle
- Les inductions embryonnaires et les gradients de morphogène
- Les matrices extracellulaires animales
- Les organismes modèles
- Les outils pour étudier l’expression et la fonction des gènes
- Les parois des cellules végétales
- Les techniques et les outils pour la biologie cellulaire
- Les transitions épithélio-mésenchymateuses et les migrations cellulaires
- Les vésicules extracellulaires
- Les voies de signalisation
- Les voies de signalisation FGF
- Mise en place des axes chez les Vertébrés
- Structures et processus cellulaires
- Voies de signalisation WNT
