Par Patrick Pla, Université Paris-Saclay

Chez les Métazoaires, les cellules se maintiennent ensemble par des adhérences intercellulaires et des adhérences avec la matrice extracellulaire. La matrice extracellulaire est traitée sur cette page.
L’adhérence intercellulaire peut être montrée par des expériences simples comme celle ci-dessous :
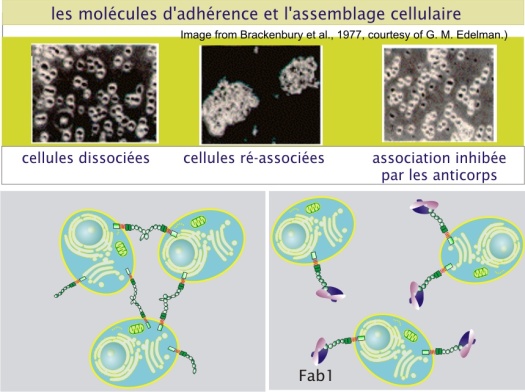
L’adhérence intercellulaire maintient la cohésion des tissus et permet de former des barrières entre deux milieux différents. Les cellules peuvent ainsi contrôler les échanges entre ces deux milieux. Au cours du développement, où les cellules peuvent être amenées à changer de position et donc de cellules voisines, les adhérences sont particulièrement dynamiques. Elles peuvent être aussi porteuses d’une information et à ce titre peuvent entrer dans la catégorie des communications juxtacrines (communication entre cellules voisines).
Les complexes d’adhérence
Ces complexes sont présents surtout dans les épithéliums.
Les adhérences jonctionnelles se présentent comme des complexes moléculaires protéiques. Parmi elles, les desmosomes sont composés d’une plaque de 100 à 500 nm de diamètre, constituée de protéines telles que la desmoplakine ou la desmoglobine et de cadhérines desmosomiales transmembranaires (desmogléines, desmocollines). Comme pour toutes les cadhérines, leurs parties extracellulaires se solidarisent en présence de Ca2+. La plaque interne est reliée à des filaments intermédiaires. Les desmosomes sont impliqués dans la résistance à la déformation et au stress mécanique des épithéliums (Green et al., 2019). Ils sont aussi présents dans les jonctions entre les cardiomyocytes et permettent de les maintenir solidaires lors de la contraction musculaire cardiaque.

La présence de desmosomes est un caractère dérivé partagé exclusif des Eumétazoaires (excluant les Spongiaires parmi les Métazoaires).
Autre adhérence jonctionnelle, les jonctions serrées forment la ceinture apicale des épithéliums (et ne sont présentes que chez les Eumétazoaires, excluant donc les Spongiaires parmi les Métazoaires). Elles sont formées de claudines et d’occludines (qui ont chacune 4 domaines transmembranaires) et de JAM (qui a un domaine transmembranaire, qui joue un rôle dans la stabilisation du complexe et aussi dans la polarité cellulaire). Les jonctions serrées sont reliées aux microfilaments d’actine via les protéines ZO-1/-2/-3.
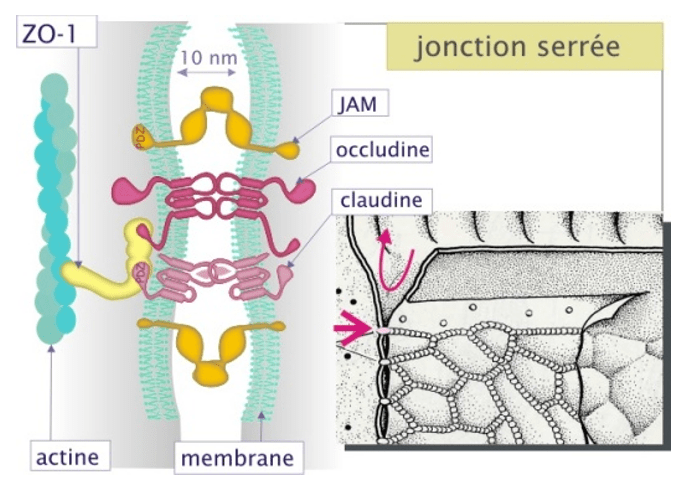
Ces jonctions serrées forment une barrière étanche qui bloque la circulation intercellulaire, assurant que les échanges de part et d’autre de l’épithélium se font à travers les cellules de manière contrôlée (perméabilité sélective de l’épithélium). Une brèche dans les jonctions serrées augmente la perméabilité entre les cellules et peut causer des pathologies (par exemple, des maladies chroniques inflammatoires de l’intestin) (Choi et al., 2017). Les jonctions serrées permettent aussi de restreindre la diffusion des protéines membranaires et donc d’assurer la spécificité de composition du domaine apical et du domaine basolatéral de la membrane plasmique des cellules épithéliales.
Les claudines forment une famille de 27 membres chez les Mammifères. Diverses combinaisons de claudines sont exprimées dans les différents cellules épithéliales et chaque claudine a des spécifités particulières qui participent aux propriétés spécifiques des différents épithélia (Kashihara et al., 2025). Par exemple, la perte de la claudine 11 dans des souris knock-out n’est pas compensable par d’autres claudines dans les cellules de Sertoli des testicules et aboutit à la perte de leur phénotype épithélial et à une stérilité (Mazaud-Guittot et al., 2010).
Dernière adhérence jonctionnelle, la ceinture d’adhérence ou zonula adherens. Elle est composée de cadhérines et de caténines qui sont reliées à des microfilaments d’actine. L’alternance microfilaments/zonula adherens forme une structure supracellulaire qui coordonne le comportement de la population de cellules. Par ce moyen, une pression ou un étirement à un endroit d’un épithélium sera « ressentie » par d’autres cellules assez loin.
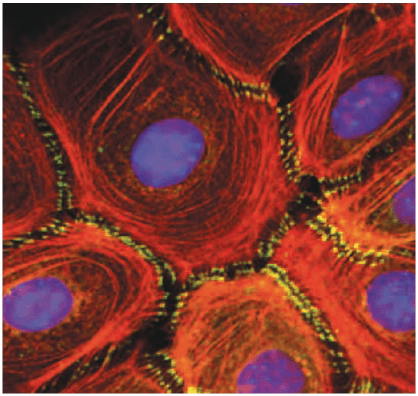

La mise en place des toutes ces zones d’adhérence est étroitement régulée lors de la formation d’un épithélium (par exemple lors d’une transition mésenchyme-épithélium ou lors du développement de structures acineuses comme les glandes mammaires). Le facteur de transcription TFAP2a est souvent impliqué dans l’activation de l’expression de la E-cadhérine qui est importante pour ces jonctions (voir plus loin) (Leask et al., 1991; Behrens et al., 1991; Hennig et al., 1996) et ERK3 est nécessaire pour que TFAP2a puisse bien activer ses cibles (Takahashi et al., 2018)

Les jonctions d’adhérence ne sont pas de simples zones qui « collent » les cellules les unes aux autres. Ce sont des centres de signalisation. Par exemple, lors de la formation du blastocyste de la souris, les cellules de la périphérie deviennent des cellules du trophectoderme (TE) et les cellules internes deviennent des cellules de la masse cellulaire interne (MCI). La protéine Angiomotine est associée aux jonctions d’adhérence dans les cellules internes et active la voie de signalisation Hippo qui réprime l’activité de YAP, un co-facteur de transcription. Dans les cellules en périphérie, Angiomotine est décrochée des jonctions adhérentes et se retrouve dans la partie apicale de la cellule. Dans ce cas, la voie Hippo n’est pas activée et YAP peut s’associer dans le noyau avec le facteur de transcription TEAD et active l’expression de Cdx2 qui spécifie les cellules en TE (Hirate et al., 2013).
Les cadhérines
Comme leur nom le suggère, les cadhérines sont des molécules d’adhérence cellulaire dépendantes des ions Ca2+. Ce sont des protéines transmembranaires qui interagissent avec les mêmes cadhérines sur les cellules adjacentes (interactions homophiles).
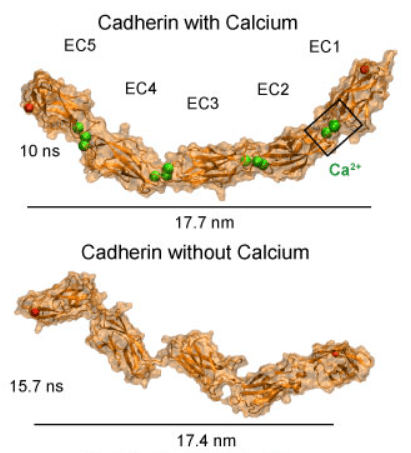
Une version commentée de cette figure est disponible en vidéo.
Source : https://www.ks.uiuc.edu/Research/cadherin/

Une version commentée de cette figure est disponible en vidéo.
Source : https://www.pnas.org/doi/full/10.1073/pnas.0905349106
Cependant, quelques cas d’interactions hétérophiliques ont été observés dans certains contextes cellulaires (Dash et al., 2022).
Les cadhérines sont ancrées à l’intérieur de la cellule par un complexe de protéines appelées caténines. Ce complexe se lie aux microfilaments d’actine de la cellule. Ce complexe permet également de regrouper plusieurs cadhérines en cluster ce qui permet une adhérence plus solide avec les cadhérines des cellules voisines que lorsque les cadhérines sont isolées (Yap et al., 1997).


L’interaction vinculine/α-caténine est particulièrement importante pour transmettre les forces de tension entre l’extérieur et l’intérieur de la cellule dans un épithélium (Seddiki et al., 2018). La tension intracellulaire induit des changements conformationnels dans l’α-caténine exposant son site cryptique de liaison à la vinculine (VBS pour Vinculin Binding Site) (Yonemura et al., 2010; Yao et al., 2014). Une fois liée à l’α-caténine, la vinculine réalise une transition vers une conformation ouverte capable de se lier au cytosquelette d’actine, permettant à son tour aux complexes d’adhésion de se renforcer et de résister à des forces plus élevées dans les cellules sous tension (le Duc et al., 2010; Dumbauld et al., 2013).

L’ensemble de ces interactions intègre les cellules épithéliales dans une unité mécanique. Le blocage de la fonction des cadhérines par une inhibition de leur expression ou par des anticorps bloquants peut empêcher la formation de tissus épithéliaux et provoque la désagrégation des cellules (Takeichi et al. 1979).
Les cadhérines interviennent précocement au cours du développement, par exemple dès le clivage lors de la compaction des embryons au stade 8 cellules chez les Mammifères. Initialement, les blastomères au stade 8 cellules sont lâchement attachés les uns aux autres mais lors de la compaction, l’adhérence cellule-cellule devient nettement plus forte. La compaction nécessite la présence d’ions Ca2+ extracellulaires ce qui a suggéré que des cadhérines sont impliqués. Des études plus poussées ont montré que la compaction est causée par l’exocytose de vésicules intracellulaires contenant de la E-cadhérine. Des embryons où les deux allèles du gène codant la E-cadhérine ont été délétés réalisent quand même la compaction ce qui montre que la E-cadhérine impliquée à cette étape est d’origine maternelle (Larue et al., 1994). Au cours de cette étape, les cellules acquièrent une polarité apico-basale comme dans un épithélium. Cette polarité est cruciale pour l’établissement du trophectoderme et de la masse cellulaire interne lors de la formation du blastocyste au cours de l’étape suivante du développement.
La E-cadhérine est la cadhérine la plus courante dans les tissus épithéliaux. D’elle dépend la stabilité de l’épithélium mais aussi son dynamisme. Par exemple, le mutant half-baked chez le poisson-zèbre possède des allèles mutés perte-de-fonction de la E-cadhérine et présente des défauts de gastrulation, notamment de l’intercalation radiaire qui est nécessaire à l’épibolie de l’épiblaste. Cette intercalation radiaire qui correspond au déplacement des cellules de la couche interne à la couche externe de l’épiblaste dépend des glissements des cellules les unes sur les autres et la E-cadhérine est essentielle dans ce processus (Kane et al., 2005).
Une classe de cadhérines appelées protocadhérines (Sano et al. 1993)
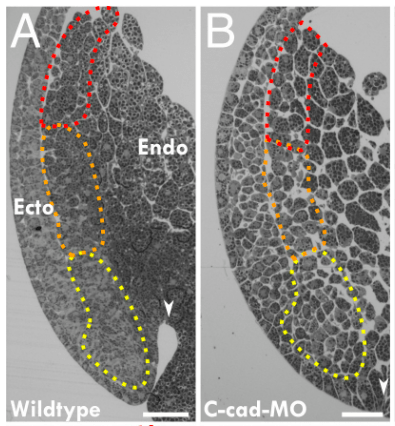
ne possède pas de domaine d’interaction avec les caténines et ne dépend pas du cytosquelette d’actine. L’expression de protocadhérines similaires permet de garder ensemble des cellules épithéliales durant une migration. L’expression de protocadhérines différentes provoque en revanche une séparation des tissus. C’est notamment le cas chez le xénope lorsque les cellules qui forment la corde expriment la protocadhérine AXPC et se séparent de celles qui forment les somites et qui expriment la protocadhérine PAPC (Chen et Gumbiner, 2006; Yoder et Gumbiner, 2011). AXPC semble avoir un rôle supplémentaire dans la spécification du destin des cellules de la corde que la simple adhérence différentielle. PAPC quant à elle, pourrait agir sur l’adhérence différentielle en diminuant l’expression de la C-cadhérine.
Certains protocadhérines dans des contextes cellulaires particuliers peuvent mettre en place des adhérences hétérophiles : lors de la mise en place des microvillosités des entérocytes, l’adhérence entre les microvillosités voisines contrôle leur disposition à la surface apicale de la cellule. Cette adhésion est médiée par une paire de protocadhérines : CDHR2 (également connu sous le nom de protocadhérine-24) et CDHR5 (également connue sous le nom de protocadhérine de type mucine). Ces protocadhérines sont présentes aux extrémités distales des microvillosités et interagissent d’une microvillosité à l’autre via une liaison hétérophile (Crawley et al., 2014).
Les changements d’expression des cadhérines accompagnent les changements de destinée des cellules. L’ectoderme de la souris exprime initialement la E-cadhérine mais au cours de la neurulation, la plaque neurale destinée à devenir le tube neural éteint l’expression de la E-cadhérine et exprime la N-cadhérine à la place. Si ce changement est bloqué, la séparation des deux tissus, ectoderme non neural et neurectoderme, se fait mal.
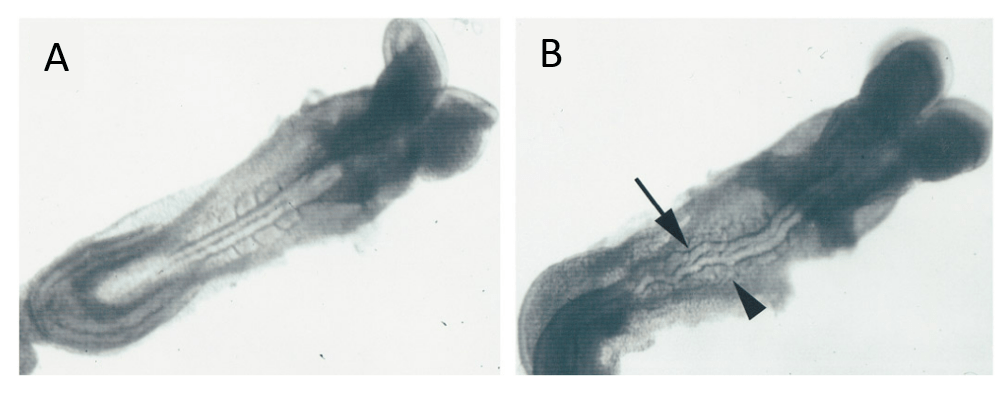
Il peut y avoir des différences entre espèces : la N-cadhérine ne semble pas jouer un rôle crucial dans l’architecture du neuroépithélium chez la souris mais elle joue un rôle important chez le poisson-zèbre.

Lors de la transition épithélio-mésenchymateuse (EMT) qui mène à l’émergence des cellules de crêtes neurales, il y a aussi des modifications importantes d’expression des cadhérines. Chez l’embryon de poulet, l’expression de la N-cadhérine et de la cadhérine 6B est remplacée par celle de Cadhérine-7 et de Cadhérine-11 (Chalpe et al., 2010 ; Nakagawa et Takeichi, 1998). Si on maintient artificiellement l’expression de la N-cadhérine, il n’y a pas de transition épithélio-mésenchymateuse et les cellules spécifiées en crêtes neurales restent dans le tube neural (Shoval et al., 2007). Au cours de cet EMT, ce sont les facteurs de transcription Snail2, Foxd3, Sox9 et Sox10 qui coopèrent pour provoquer les changements dans l’expression des cadhérines.

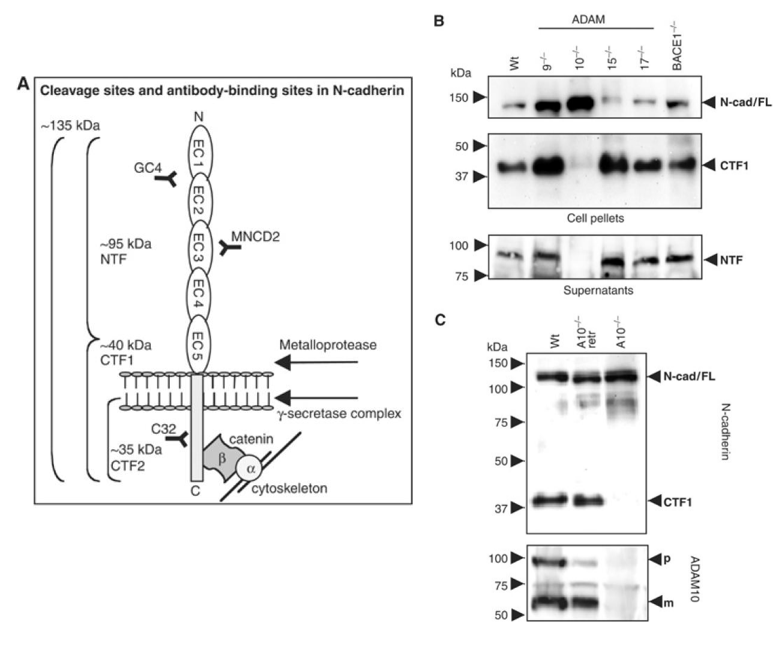
Durant la transition épithélio-mésenchymateuse des crêtes neurales, non seulement la transcription du gène codant la N-cadhérine est diminuée mais en plus la partie extracellulaire des protéines encore présentes est clivée par la métalloprotéinase ADAM10 (Shoval et al., 2007).
Cependant, une fois de plus, ce n’est pas un mécanisme général car chez le xénope, l’expression de la N-cadhérine est augmentée au cours de la transition épithélio-mésenchymateuse des cellules de crêtes neurales (Bahm et al., 2017). Dans ce modèle, la N-cadhérine permet aux cellules migrantes de mieux répondre au chémoattracteur Sdf1. De plus, les cellules de crêtes neurales céphaliques migratrices établissent des jonctions communicantes ou jonction-gaps qui leur permettent de répondre aux sémaphorines (Bannerman et al., 2000; Huang et al., 1998; Waldo et al., 1999; Xu et al., 2006). On voit particulièrement bien dans cet exemple qu’il ne faut pas imaginer l’adhérence cellule-cellule comme un frein absolu à la migration cellulaire.
Dans un autre système comme la cicatrisation de l’épiderme de l’embryon de drosophile, la transition épithélio-mésenchymateuse est réalisée en partie par endocytose de la E-cadhérine (Hunter et al., 2015).
Les interactions médiées par les cadhérines peuvent être essentielles entre des cellules souches et les cellules de leur niche pour que les cellules souches conservent leurs propriétés. C’est le cas dans les ovarioles de drosophile. Les cellules souches germinales sont en contact avec les cellules de la coiffe dans la partie la plus antérieure des ovarioles. Les interactions E-cadhérine/E-cadhérine assurent que les cellules souches germinales ne se différencient pas. Lorsqu’au cours d’une division cellulaire, une des deux cellules filles de la cellule souche perd le contact avec les cellules de la coiffe, elle commence à se différencier en cystoblaste qui va subir la méiose.
Autres molécules d’adhérences cellulaires

Contrairement à ce que l’on pourrait penser les intégrines peuvent également être impliquées dans l’adhérence cellule-cellule en plus de leur fonction plus classique d’adhérence à la matrice extracellulaire. Par exemple, les cellules souches hématopoïétiques restent dans leur niche, accrochées aux cellules stromales voisines et les intégrines participent à ces jonctions.

Si on utilise des anticorps bloquant l’interaction intégrine α4β1/VCAM-1, les cellules souches hématopoïétiques finissent par s’échapper dans la circulation sanguine (Papayonnoupoulou et al., 1995). L’interaction entre l’intégrine α4β7 et MadCam-1 est essentielle pour le recrutement des cellules souches hématopoïétiques dans la moelle osseuse soit au cours du développement, soit au cours de transfusions (Katayama et al., 2004). Chez les patients atteints de leucémie myéloïde aigue, l’interaction intégrine α4β1/VCAM-1 est un élément important de la résistance à la chimiothérapie parce que cette interaction active la signalisation NF-kB dans les cellules stromales qui en retour envoient des signaux favorisant la survie des cellules tumorales (Jacamo et al., 2014).
VCAM-1 est aussi impliqué dans le maintien des cellules souches neurales dans la zone sous-ventriculaire du télencéphale où de la neurogénèse se déroule chez les Mammifères adultes. Lorsqu’avec une micropompe, on injecte en continu pendant 6 jours des anticorps bloquant anti-VCAM dans la zone sous-ventriculaire d’une souris, la couche des cellules épendymaires qui constitue une partie de la niche des cellules souches neurales est désorganisée (Kokovay et al., 2012). Cela aboutit à augmenter la prolifération des cellules souches neurales dont une grande partie est habituellement quiescente. Dans ce système, VCAM-1 est exprimé par les cellules souches neurales. Son partenaire sur les cellules épendymales n’a pas été encore trouvé.
L’adhérence cellulaire médiée par les intégrines et les molécules qui s’y lient peut être contrôlée. Par exemple, lors d’une inflammation, les cellules endothéliales produisent des chimiokines en direction des leucocytes qui activent des voies de signalisation intracellulaires qui activent les intégrines à la surface en leur faisant changer de conformation et qui permet de les faire interagir avec ICAM-1 qui est présente à la surface des cellules endothéliales. Cette interaction permet de ralentir puis d’arrêter les leucocytes, préalable à leur traversée de l’endothelium vers le site de l’inflammation.

Les protéines Dscam chez la drosophile appartiennent à la famille des molécules d’adhérence cellulaire et jouent un rôle important dans l’immunité et dans la mise en place en place des circuits nerveux. Ces protéines sont très diversifiées mais elles proviennent d’un seul gène qui contient 115 exons. La diversité est générée par épissage alternatif : 20 exons sont toujours présents mais 95 sont « optionnels » et de multiples combinaisons sont générées. Les interactions homophiliques n’ont lieu qu’entre protéines identiques mais pas entre protéines même très proches (Wojtowicz et al., 2009). Cela suggère que le rôle de Dscam dans le guidage axonal et la mise en place des réseaux neuronaux chez la drosophile est lié à des reconnaissances et des adhérences très précises entre cellules.
LA CARTE MENTALE

LIEN VERS LE GLOSSAIRE DES TERMES SPECIFIQUES A L’ADHERENCE CELLULE-CELLULE
(et cytosquelette et matrices extracellulaires)
LIEN VERS LE GLOSSAIRE GENERAL
- Arabidopsis thaliana
- Axe antéro-postérieur chez la drosophile
- Biomécanique du développement
- Caenorhabditis elegans
- Concepts principaux
- Contrôle de la traduction
- Contrôle de la transcription
- Contrôle génétique et épigénétique
- Croissance du tube pollinique et double fécondation chez les Angiospermes
- Croissance et guidage axonal
- Des modèles animaux moins classiques
- Développement de l’oeil des Vertébrés
- Développement et évolution
- Et l’Humain ?
- Exercices sur l’ovogenèse, la spermatogenèse et la fécondation
- Exercices sur le contrôle de l’expression des gènes
- Exercices sur le développement des bourgeons de membre
- Exercices sur le développement des muscles striés squelettiques
- Exercices sur le développement des végétaux et les hormones végétales
- Exercices sur les cycles et les divisions cellulaires
- Exercices sur les étapes du développement, les inductions embryonnaires et la mise en place des axes de polarité
- Exercices sur les matrices extracellulaires, le cytosquelette et les adhérences cellule-cellule
- Exercices sur les voies de signalisation
- Glossaire
- Glossaire des termes liés à la génétique
- Glossaire des termes liés au cytosquelette, la matrice extracellulaire, l’adhérence et la migration cellulaire
- Hématopoïèse et développement des cellules du système immunitaire
- Histoire de la biologie cellulaire et de la biologie du développement
- L’acide rétinoïque
- L’apoptose
- L’autophagie
- L’organogenèse
- L’ovogénèse prépare le développement embryonnaire
- La drosophile
- La fécondation
- La formation des somites
- La gastrulation
- La gastrulation (version allégée)
- La métamorphose chez les Hexapodes et les Amphibiens
- La neurogénèse chez les mammifères adultes
- La neurulation
- La poule
- La signalisation calcique
- La souris
- La superfamille TGFβ et ses voies de signalisation
- La voie de signalisation de l’auxine et ses rôles
- La voie de signalisation Hedgehog
- La voie de signalisation Hippo et ses composants YAP/TAZ
- La voie de signalisation Notch
- Le clivage
- Le cytosquelette
- Le destin des cellules et les réseaux de régulation génique
- Le développement des bourgeons de membre
- Le développement des muscles striés squelettiques
- Le développement des organes génitaux et des cellules germinales
- Le développement du cortex
- Le méristème apical caulinaire en phase végétative et lors de la formation d’une fleur
- Le poisson zèbre
- Le xénope
- Les cellules des crêtes neurales
- Les cellules et les gènes en action dans le développement
- Les cellules souches
- Les cellules tumorales
- Les cycles et les divisions cellulaires
- Les étapes du développement
- Les étapes du développement embryonnaire d’Arabidopsis thaliana et leur contrôle
- Les inductions embryonnaires et les gradients de morphogène
- Les matrices extracellulaires animales
- Les organismes modèles
- Les outils pour étudier l’expression et la fonction des gènes
- Les parois des cellules végétales
- Les techniques et les outils pour la biologie cellulaire
- Les transitions épithélio-mésenchymateuses et les migrations cellulaires
- Les vésicules extracellulaires
- Les voies de signalisation
- Les voies de signalisation FGF
- Mise en place des axes chez les Vertébrés
- Structures et processus cellulaires
- Voies de signalisation WNT
