Par Patrick Pla, Université Paris-Saclay
La biologie du développement est une discipline très ancienne dont on trouve les premières traces dans l’Antiquité avec Aristote (384-322 av. JC). Il observe le développement d’embryons de poulet à différents stades. Il classe les animaux en ovipares, vivipares et ovovivipares et pose la question fondamentale de la biologie du développement : comment sont formées les différentes parties de l’embryon ?
- La biologie du développement à la croisée des chemins entre la biologie cellulaire, la génétique et l’évolution
- Progrès dans la compréhension des modalités du développement embryonnaire
- Histoire de l’étude et de la production des cellules souches
La biologie du développement à la croisée des chemins entre la biologie cellulaire, la génétique et l’évolution
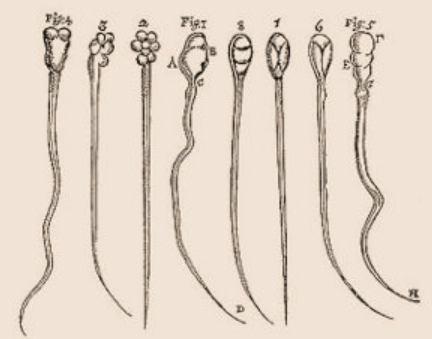
L’idée dominante de l’Antiquité d’Aristote à la Renaissance est celle de la génération spontanée : les petits organismes naissent continument à partir de matière inanimée. William Harvey pose en 1651 les bases de la réfutation de la génération spontanée avec son « Ex ovo omnia » (tout provient d’un oeuf). C’est dans ce contexte qu’a lieu le débat entre préformation (des embryons pré-formés emboités comme des poupées russes à travers les générations) et épigenèse (formation d’un nouvel embryon à chaque génération). Le principal propagateur de la préformation est Nicolaas Hartsoeker (1656-1725) : « Chacun des animaux mâles (les spermatozoïdes) renferme une infinité d’autres embryons ».
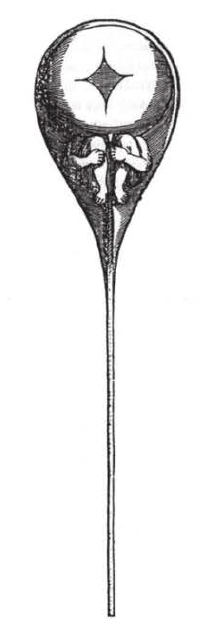
Des données expérimentales mal interprétées vont dans le sens de la préformation : Charles Bonnet (1720-1793) isole une femelle puceron et elle est capable de donner une progéniture. Il en conclut que la préformation existe mais il ne peut se douter que c’est en fait de la parthénogenèse qui a eu lieu (cas particulier du développement d’un ovocyte en embryon sans fécondation avec un gamète mâle). La préformation commencera à être réfutée par Pierre-Louis Moreau de Maupertuis (1698-1759) qui ne comprend pas comme elle peut rendre compte des croisements humains inter-ethniques qui donnent des métisses. Il propose alors que les embryons se forment par le mélange d’une semence maternelle et d’une semence paternelle. Caspar Friedrich Wolff (1734-1794), à partir de ses observations d’embryons de poulet, va poursuivre la réfutation de la préformation et renforcer la notion d’épigenèse. Dans son sillage, Christian Heinrich Pander (1794-1865) énonce la théorie des feuillets embryonnaires (les tissus des animaux se forment à partir de 3 feuillets : ectoderme, mésoderme et endoderme) et qui est toujours utilisée aujourd’hui.
Comment l’information circule-t-elle entre le soma (corps) et les gamètes qui contribuent à la génération suivante ? Selon la théorie de la pangenèse (dont Charles Darwin était un adepte), les cellules somatiques transmettent de l’information vers le « plasma germinatif » ou « germinal ». Dans son traité de 1892, Das Keimplasma: eine Theorie der Vererbung (Le plasma germinatif: une théorie de l’hérédité), August Weismann a proposé que l’information ne circule que du plasma germinal vers le soma et non l’inverse. Ainsi, alors que le soma vieillit et finit par mourir, les cellules germinales sont en quelque sorte épargnées des effets ruineux du vieillissement, conduisant à l’immortalité théorique d’une espèce.
Quant à la théorie de la génération spontanée, elle ne sera définitivement réfutée pour tous les êtres vivants, y compris les « microbes » qu’au XIXème siècle par Louis Pasteur avec son expérience avec des ballons en col de cygne.

Les progrès techniques vont amener progressivement des changements conceptuels avec le développement des premiers microscopes et l’observation des premières cellules (Robert Hooke en 1665 qui a utilisé pour la première fois le terme « cellule » appliqué aux êtres vivants et Antoine Von Leeuwenhoek en 1675), ce qui n’empêche pas, comme nous l’avons vu plus haut, certaines théories erronées (comme celle de la préformation) de continuer à prospérer pendant un moment.
Voir une page interactive qui explore l’histoire de la théorie cellulaire
Une fois la théorie cellulaire acceptée (grâce à la synthèse réalisée par le botaniste Schleiden et le zoologiste Schwann en 1838) et la contribution des processus cellulaires bien observée dans les embryons (avec Wilhelm His par exemple qui observe la migration des cellules de crêtes neurales en 1868), la biologie du développement se retrouve à devoir répondre à deux questions : la question quantitative (comment produire un nombre de cellules suffisant ?) et la question qualitative (comment produire des cellules différentes au bon endroit ?). Ces deux questions doivent avoir des mécanismes coordonnés dans l’embryon bien entendu.
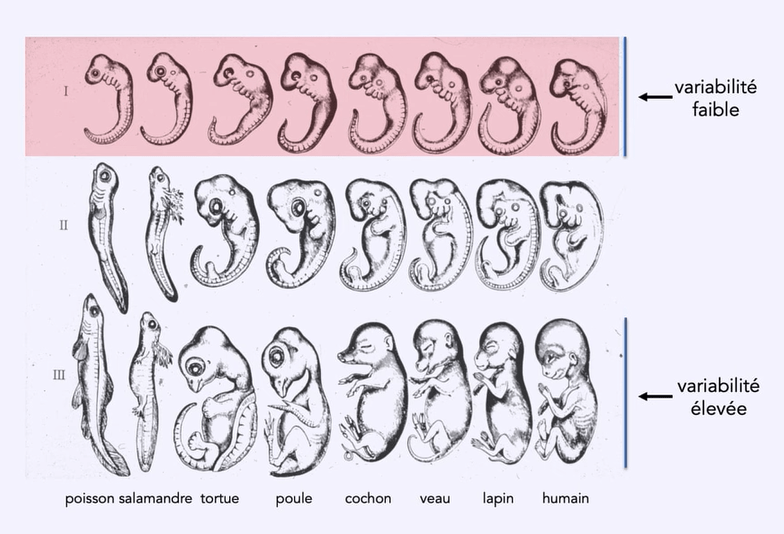
La question de nos origines en tant qu’individu (ontogenèse) est aussi liée à la question de nos origines dans un sens plus large (l’origine de notre espèce et ses parentés avec les autres espèces, la phylogenèse). Ces deux questions ont des relations différentes avec la notion de temps : le développement embryonnaire revient de manière cyclique à chaque nouvelle génération de manière quasi-identique alors que l’évolution est un processus historique sur une échelle de temps plus grande et avec une dimension linéaire, non cyclique. Autant le développement embryonnaire est facilement accessible à l’expérimentation car il est assez prévisible même sur un grand nombre d’embryons de différentes générations, autant l’évolution se prête difficilement à des expériences dans sa dimension historique (il faudrait remonter dans le temps et changer des paramètres). Ernst Haeckel (1834-1919) a tenté néanmoins de relier les deux temporalités selon la formule « L’ontogenèse récapitule la phylogenèse » mais il s’agit d’une généralisation excessive du fait que certaines espèces partagent des stades embryonnaires très proches (comme le stade phylotypique à la fin de la neurulation/début organogenèse chez les Vertébrés).
Charles Darwin publie L’origine des espèces en 1859. Il s’appuie sur le transformisme mis en avant une cinquantaine d’années plus tôt par Lamarck mais avec un autre mécanisme : la sélection naturelle. Des variations des caractères apparaissent au hasard et les plus avantageux pour la survie et la reproduction sont logiquement plus transmis à la descendance.
Darwin ne comprend pas l’origine des variations et les mécanismes de leur transmission d’une génération à l’autre. Pour lui, les cellules reproductrices sont constituées de « gemmules » issues de toutes les parties du corps (théorie de la pangenèse). La distinction cellules germinales/cellules somatiques n’est absolument pas connue de Darwin. Il s’intéresse cependant à la règle de Von Baer (du nom de Karl Ernst Von Baer (1792-1876)) qui stipule que les structures les plus communément partagées parmi les groupes d’animaux se forment plus tôt au cours du développement que les structures partagées par un groupe plus restreint. Darwin y voit un argument pour un ancêtre commun entre différentes espèces. Mais l’embryologie est absente du reste de son raisonnement. C’est Thomas Huxley en 1893 qui remet en selle l’embryologie dans le cadre de la théorie darwinienne en rappelant l’importance de la construction des plans d’organisation, ce qu’il nomme épigenèse.
L’étude du développement va cependant se trouver détaché de l’étude de l’évolution pendant une grande partie du XXème siècle. Le développement concerne un individu que l’on peut perturber expérimentalement (greffes ou ablations de Hans Spemann par exemple) alors que l’évolution concerne des populations dont on n’a généralement qu’une vision historique et rétrospective (bien que quelques expériences puissent être tentées pour des espèces avec des temps de génération faibles comme la drosophile). Cependant, le petit-fils de Thomas Huxley, Julian Huxley (et par ailleurs le frère d’Aldous Huxley qui a écrit « Le Meilleur des Mondes ») précise en 1942 qu’il est indispensable de comprendre le rôle des gènes dans le développement pour comprendre l’évolution.
La biologie du développement se retrouve aussi longtemps détachée de la génétique qui ne s’attache dans un premier temps qu’à étudier des caractères observables de manière simple chez l’adulte. Gregor Mendel (1822-1884) à Brno (actuellement en République Tchèque) met en évidence les lois qui gouvernent la transmission des caractères mais ne s’intéresse pas du tout aux mécanismes qui font le lien entre les gènes et le phénotype (caractère apparent chez un individu). Cependant, des concepts émergent des études purement génétiques qui vont ensuite être très utiles aux biologistes du développement comme la notion de gènes liés aux chromosomes sexuels (Thomas Morgan sur la drosophile dans les années 1910) et la notion de pléiotropie (décrite pour la première fois par Ludwig Plate en 1910 : elle qualifie un gène dont la mutation peut avoir des effets phénotypiques sur plusieurs organes ou tissus. On sait maintenant que de très nombreux gènes du développement sont pléiotropes) .Plus tard, au détour de la discussion sur comment des changements spectaculaires de plans d’organisation ont pu avoir lieu alors que la théorie darwinienne classique présente une évolution graduelle et lente (« Natural selection can never take a leap but must advance by the shortest and slowest steps », écrit Darwin en 1859), le chercheur Richard Goldschmidt en 1940 dans son ouvrage Les bases matérielles de l’évolution développe l’idée que de macromutations dans des gènes de contrôle du développement et il développe le terme de « monstre prometteur », c’est-à-dire un mutant avec un phénotype anormal marqué mais qui pourrait être sélectionné dans un certain environnement et être ainsi à la base d’un « saut » dans l’évolution ou macro-évolution. La théorie des équilibres ponctués de Gould et Eldredge dans les années 1970 indiquant que l’évolution procède alternativement de périodes de changements brusques puis de stabilité des espèces fait la synthèse entre macro- et microévolution.
Ce n’est qu’avec l’avènement des techniques de biologie moléculaire et les clonages des premiers gènes du développement comme les gènes Hox (Ed Lewis en 1978, Gehring en 1984) que la génétique moléculaire du développement et l’ »évo-devo » vont prendre leur essor à partir de la fin des années 1980. C’est le début d’une période de multiplicité des approches et de la fusion de concepts qui avaient jusqu’à cette époque été étudiés séparément.
Pendant des décennies, le déchiffrement de la fonction des gènes était basé sur la génétique directe : l’identification des phénotypes chez des mutants apparus au hasard ou générés par des agents mutagènes venait en premier, puis chaque phénotype d’intérêt était lié à une mutation et à un locus spécifiques. La puissance de cette approche a été clairement démontrée par les travaux de Christiane Nüsslein-Volhard et Eric Wieschaus en 1978 qui ont disséqué les bases de la mise en place des axes de polarité de la drosophile à travers un criblage génétique avancé. Ce criblage a identifié et caractérisé 600 mutants, dont les mutations ont été cartographiées sur 120 gènes, dont beaucoup sont parmi les gènes les plus étudiés en biologie du développement encore actuellement (Wieschaus et Nüsslein-Volhard, 2016).
Une approche de génétique inverse a commencé à émerger dans les années 1980 et a bénéficié des approches de modifications directes et contrôlées du génome ou de l’expression des gènes : invalidation de gènes par recombinaison homologue (knock-out), remplacement d’un allèle par un autre (pas forcément complètement non fonctionnel) (knock-in puis CRISPR-Cas9), morpholinos, siARN…
Les progrès de la génomique (séquençage entier des génomes des organismes modèles tels que C. elegans, la drosophile, la souris) et aussi de la transcriptomique (puces à ADN, RNAseq, et étude transcriptomique de cellules uniques) vont amener un changement d’échelle à partir des années 2000 : on ne raisonne plus gène par gène mais par de larges ensembles de gènes sur des éléments de plus en plus précis (embryons entiers, tissus puis chaque cellule d’un tissu). Les modifications épigénétiques (état de la chromatine) seront aussi étudiées de manière de plus en plus fine.
On se rend compte également avec le séquençage du génome humain du nombre relativement faible de gènes chez l’Homme par rapport à des organismes dits « simples » comme le nématode C. elegans (23.000 gènes chez l’Homme pour des dizaines de milliards de cellules et 15.000 gènes chez C. elegans pour environ un millier de cellules). Cela renforce l’idée que la complexification des processus géniques (formation de différentes isoformes, épissages alternatifs…) et des réseaux de régulation génique (modifications épigénétiques de la chromatine, contrôle de la traduction…) jouent un rôle essentiel au cours du développement et que le nombre « brut » de gènes n’est pas le paramètre le plus pertinent pour comprendre la génétique du développement.
De plus, plus de 20 ans après la publication du génome humain, jusqu’à un tiers des gènes humains restent mal caractérisés, et nous savons peu de choses sur leur importance physiologique (Stoeger et al., 2018). De même, malgré une grande amélioration de la technologie de séquençage et de la modélisation des structures 3D, environ 20 % des protéines de toutes les espèces eucaryotes n’ont pas de fonction attribuée claire (Wood et al., 2019).
A cela s’ajoute les progrès de l’étude de la conformation de la chromatine (initiée sur des modèles restreints comme les puffs des chromosomes polytènes des insectes mais généralisée ensuite à partir du début des années 2000 par les techniques de capture de conformation chromosomique (3C, Hi-C) et d’immunoprécipitation de la chromatine) qui a permis de mieux comprendre les modifications épigénétiques qui sont fondamentaux pour le contrôle de l’expression des gènes.
Des chercheurs comme Eric Davidson (voir cette biographie) ont popularisé le concept de réseau de régulation génique qui permet une vue intégrée de la détermination et de la différenciation des types cellulaires et qui met en évidence que c’est une combinaison de facteurs qui sous-tend ces processus. Cela permet une modularité qui permet à l’évolution de créer des « monstres prometteurs » mais certains éléments du réseau (« kernel » ou composant fondamental) résistent à la variation par contrainte interne.
Progrès dans la compréhension des modalités du développement embryonnaire
Dans les modalités du développement, la discussion a beaucoup tourné de la fin du XIXème siècle jusqu’à la fin du XXème siècle sur l’opposition entre le développement mosaïque et le développement à régulation. Sur la base des premières observations sur divers modèles, le développement était généralement considéré comme mosaïque avec des cellules qui très tôt ne peuvent changer de destinée. C’était par exemple les conclusions de Wilhelm Roux (1850-1924) à la suite de la dissociation de deux blastomères de grenouille avec un clou brûlé qui avait observé un développement partiel de chaque blastomère. Laurent Chabry (1855-1894) est arrivé à la même conclusion avec l’étude des ascidies.
Citons également les travaux de Edward Conklin qui, en 1905, a observé que le cytoplasme coloré en jaune de l’ascidie Styela partita était toujours, au cours des divisions cellulaires, hérité par les cellules dont les descendantes allaient donner des cellules musculaires. Si on retire les cellules qui héritent de ce cytoplasme (les blastomères B4.1) alors il n’y a plus de cellules musculaires. Si du cytoplasme jaune est transféré dans une cellule qui ne donne habituellement pas de muscle alors sa destinée change et elle donne du tissu musculaire. [On a depuis compris le déterminisme moléculaire des propriétés de ce cytoplasme : il contient des ARNm qui permettent de synthétiser la protéine macho qui engage les cellules dans le lignage musculaire (Nishida et Sawada, 2001)]. Il s’agit d’un exemple classique de déterminisme de lignage autonome, par héritage de cytoplasme au cours des divisions cellulaires sans besoin d’induction en provenance des cellules voisines.
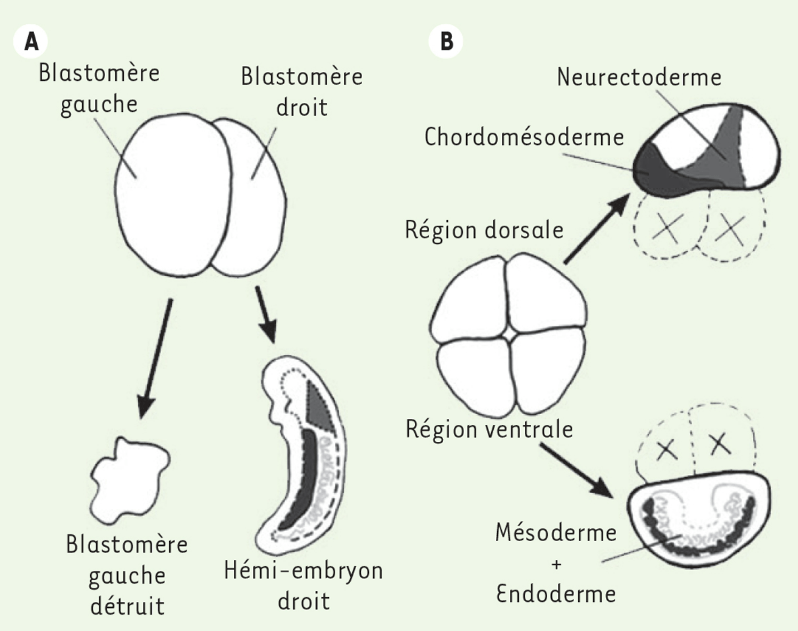
Le premier à avoir mis en évidence un développement à régulation est Hans Driesch, un biologiste allemand (1867-1941).
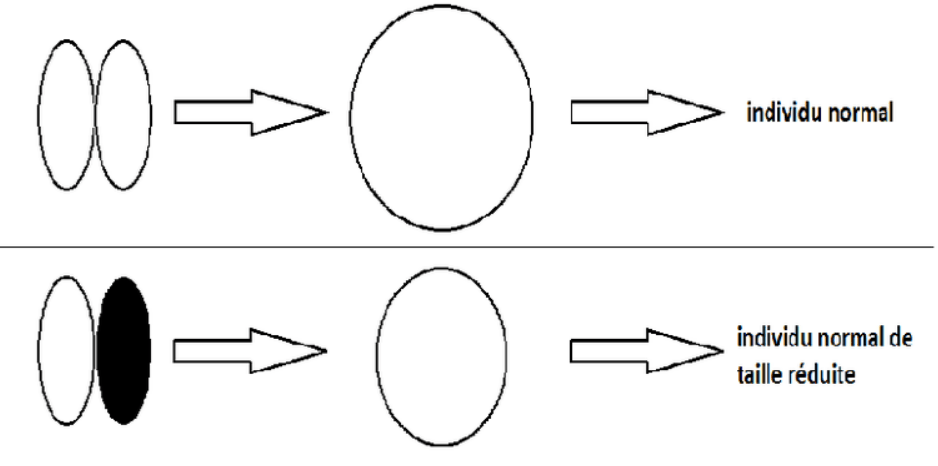
Cette expérience a permis de montrer qu’une cellule embryonnaire était capable de compenser la perte d’une cellule voisine, d’où le terme de régulation. Driesch est allé plus loin et a même réussi à séparer les 4 premiers blastomères d’un embryon d’oursin : chacun de ces blastomères isolé a donné une larve (à peu près) normale mais plus petite. Cela démontrait la totipotence de ces cellules et aussi les capacités de régulation importantes des embryons à ce stade.

La vision actuelle est qu’aucun développement n’est entièrement mosaïque ou entièrement régulé mais que chaque développement est un cocktail de chacun des deux processus avec différentes proportions selon les modèles et les stades de développement.
L’idée que les cellules adoptent des destins différents en détectant la présence ou l’absence de produits chimiques, appelés facteurs déterminants du destin ou «déterminants» remonte au début du XXème siècle. Cependant, l’expérience qui a permis de cimenter l’idée qu’une population de cellules peut contrôler le destin d’autres cellules est celle de Spemann et Mangold en 1924. La transplantation de la lèvre dorsale du blastopore d’un embryon d’amphibien sur la région ventrale d’un autre embryon induit la formation d’un nouveau tube neural et de nouvelles structures mésodermiques dorsales. Les cellules du greffon n’ont que marginalement participées à ces nouvelles structures : il s’agit bien d’une instruction envoyée par un groupe de cellules à un autre groupe de cellules qui a changé sa destinée. C’est une induction embryonnaire.

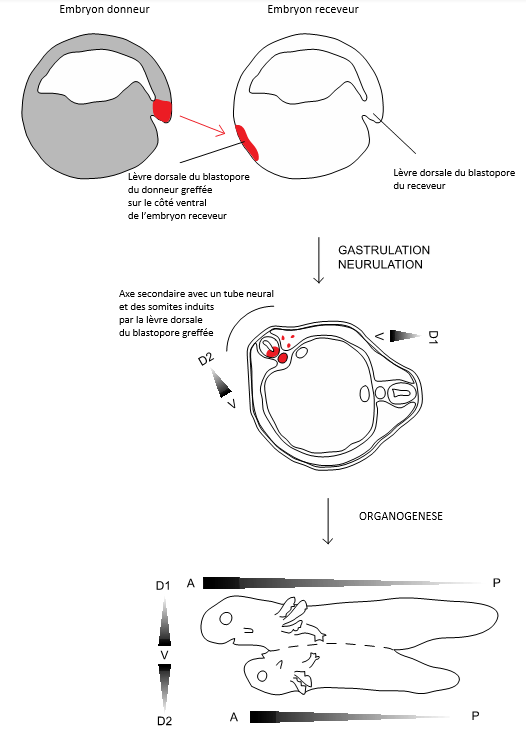
Conrad H. Waddington a élargi la notion d’inducteur aux Oiseaux et aux Mammifères par ses greffes de l’extrémité antérieure de la ligne primitive d’embryons de poulet, de canard et de lapin dans des embryons de poulet précoce et a observé une duplication de l’axe antéropostérieur de l’hôte.
Les expériences de Boveri sur des embryons d’oursins en 1901 ont montré que les modèles de développement pourraient être déterminés par des gradients opposés, tandis que des expériences de régénération sur des planaires en 1904 postulaient l’existence de « substances formatrices » qui influencent le plan de développement de l’embryon. En 1952, Alan Turing a postulé que des concentrations de produits chimiques spécifiques, appelés « morphogènes », pourraient instruire le destin des cellules et donc l’organogenèse dans un organisme en développement.

Après avoir déchiffré le code de la machine allemande Enigma au cours de la seconde guerre mondiale, Turing s’est intéressé à en 1952 aux équations de réaction-diffusion, puis a élaboré un modèle biomathématique de la morphogenèse, applicable aux animaux ou aux végétaux. Il fait paraître un article à ce sujet, «The Chemical Basis of Morphogenesis» (Philosophical Transactions of the Royal Society, août 1952). Vous pouvez lire cet article ici : https://www.dna.caltech.edu/courses/cs191/paperscs191/turing.pdf
Dans les années 1990, des expériences de chimie confirment expérimentalement les modèles théoriques de Turing.
Voir le chapitre consacré aux inductions embryonnaires
et aux morphogènes
Histoire de l’étude et de la production des cellules souches
La notion de cellules souches est venu des études sur la régénération, quelque fois spectaculaire comme dans le cas suivant une amputation chez les hydres ou les planaires ou les membres de certains amphibiens (axolotl, salamandre) mais aussi dans le cas plus discret mais significatif du renouvellement cellulaire quotidien dans la plupart de nos organes et tissus.
Voir le chapitre consacré aux cellules souches
En 1948, Charles Leblond, Catherine Stevens et Rita Bogoroch ont réalisé la première expérience de traçage de lignée, en marquant par pulse-chase les cellules mitotiques avec de la thymidine tritiée (3H). Ils ont démontré que, dans l’intestin grêle, les cellules marquées pendant la phase pulsée de l’expérience étaient d’abord repérées dans les cryptes et, pendant la période de chasse, étaient déplacées dans les villosités. Cette découverte importante, associée à l’identification de Leblond et Stevens (1948) selon laquelle les pointes des villosités étaient des zones d’extrusion cellulaire, a mené à l’idée que l’axe crypte-villosités est un tapis roulant continu de cellules, avec la production active de cellules due à la ces mitoses …équilibrées par une perte cellulaire équivalente, afin de maintenir l’état d’équilibre des tissus. Des études sur la peau et les lymphocytes utilisant le marquage 3H-thymidine ont tiré des conclusions similaires sur le renouvellement cellulaire. McCulloch, Till et leurs collègues démontrent l’existence de cellules souches hématopoïétiques adultes en 1961.
Ainsi, l’existence généralisée du renouvellement cellulaire dans de nombreux organes matures a été rapidement montrée et la notion de cellule souche capable de soutenir ce renouvellement sur le long terme a été mis en évidence.
Les cellules ES (embryonnaires souches) ont été dérivées pour la première fois en 1981 en cultivant la masse cellulaire interne des blastocystes de souris (Evans et Kaufman, 1981 ; Martin, 1981).


Leur milieu de culture a été basé initialement sur celui des cellules ECC (ou cellules de carcinomes embryonnaires) issues de tumeurs testiculaires qui forment des tératocarcinomes où des dérivés des trois feuillets embryonnaires peuvent être décelés et qui avaient été caractérisés lors de leur apparition spontanée chez certaines lignées de souris dans les années 1960.
La pluripotence des cellules les ES peut être démontrée en les cultivant en suspension dans une boite de Pétri avec un substrat non adhésif dans un milieu qui ne maintient pas les cellules à l’état indifférencié. Elles forment alors des corps embryonnaires où on peut déceler par des analyses d’expression de marqueur la présence de cellules dérivées des 3 feuillets (ectoderme, mésoderme et endoderme) (Itskovitz-Eldor et al., 2000). Alternativement, l’injection des cellules ES dans une souris (immunodéprimée pour éviter les rejets) peut aboutir à la formation de tératomes qui contiennent également des cellules dérivées des 3 feuillets.

La capacité des cellules ES à contribuer aux chimères, à coloniser la lignée germinale et à engendrer une progéniture saine a été démontrée en 1984 (Bradley et al., 1984), établissant qu’elles sont non transformées et génétiquement normales (bien qu’il y ait une tendance à l’aneuploïdie au fur et à mesure des passages). Cette découverte a permis d’introduire des modifications génétiques ciblées chez la souris en mettant en œuvre une recombinaison homologue dans les cellules ES (méthode du knock-out). Ce n’est toutefois que dans les années 1990 que la technologie est devenue relativement routinière.
Les conditions de culture originales pour les cellules ES comprenaient une co-culture avec une couche nourricière de fibroblastes embryonnaires arrêtés en mitose et un milieu contenant du sérum de veau fœtal (FCS) sélectionné (Robertson, 1987).
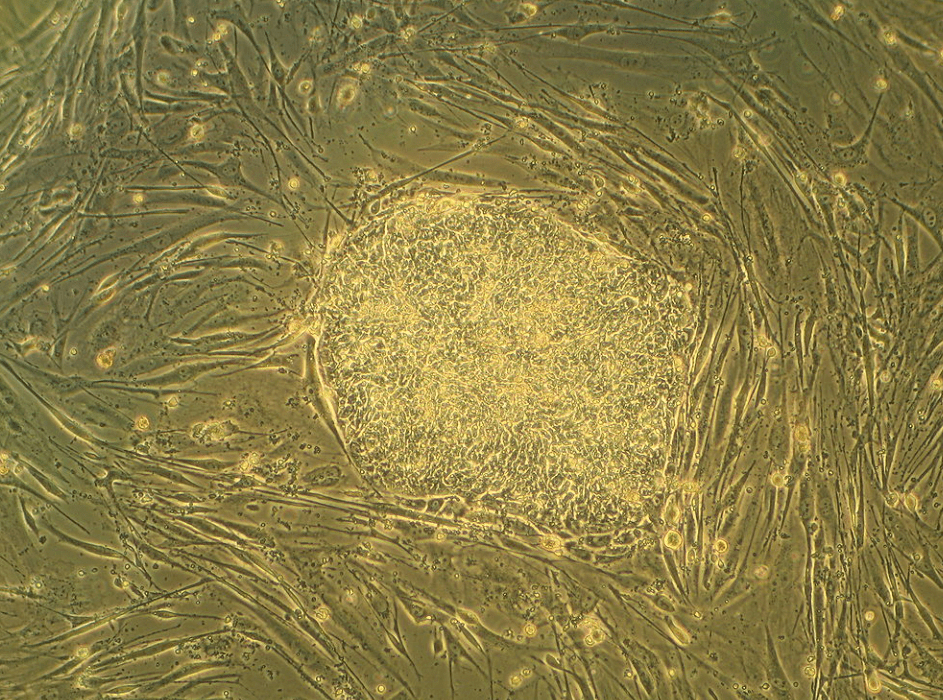
Ce système efficace mais complexe (co-culture, variabilité de la qualité des cellules nourricières et du sérum, sérum extrait d’animaux donc potentiellement problématique pour les cultures dans un but thérapeutique…) a été simplifié avec la découverte qu’une contribution majeure de la couche nourricière est de fournir le facteur LIF (pour Leukemia Inhibitory Factor) (Smith et al., 1988; Williams et al., 1988). L’ajout de LIF augmente la robustesse des cultures de cellules ES par rapport à la co-culture avec des fibroblastes et cela reste un système largement utilisé. Les conditions ont encore été améliorées pour avoir une meilleure homogénéité dans les cultures lorsque les cellules ES ont été maintenues dans un milieu défini dans lequel la voie de signalisation Erk1/2 est bloquée et la glycogène synthase kinase 3 (GSK3) est partiellement inhibée (Wray et al., 2010; Ying et al., 2008). Sous cette double inhibition, connue sous le nom de 2i, les cellules ES présentent une similitude de transcriptome avec l’épiblaste préimplantatoire (Boroviak et al., 2014).
Les cellules ES humaines ont été isolées et cultivées pour la première fois en 1998. Elles présentent quelques différences avec les cellules ES de souris (les colonies sont aplaties sur la boite de Pétri et ne forment pas de dome, elles nécessitent du FGF pour leur maintenance alors que les cellules ES de souris se portent mieux sans signalisation FGF) (Dowell et al., 2014). Leur utilisation en thérapie génique a été freinée par la nécessité de produire un nouvel embryon humain (éventuellement par clonage thérapeutique) pour pouvoir les produire à partir des blastocystes.
Les cellules souches pluripotentes induites iPS, elles, sont générées à partir de cellules différenciées en leur faisant exprimer 4 facteurs de transcription : Oct4, Sox2, Klf4, c-Myc.
La production de cellules iPS a été mise au point par Shinya Yamanaka en 2007 et lui a valu le Prix Nobel de Médecine en 2012. Le fait que mis dans un environnement favorable, un génome de cellules différenciées puisse fonctionner dans une cellule redevenu pluripotente permet d’avoir une source « inépuisable » et facile d’accès, sans restrictions éthiques, pour produire des cellules souches pluripotentes humaines.

La dédifférenciation et la remise en prolifération des cellules pour produire des cellules iPS reposent en partie sur l’ajout d’un vecteur d’expression avec l’oncogène c-Myc mais des recherches ont abouti à pouvoir l’éviter. La reprogrammation est aussi possible sans intégration génomique des transgènes. Initialement, Yamanaka avait utilisé des vecteurs rétroviraux pour introduire les gènes nécessaires à la production de cellules iPS mais maintenant l’utilisation de virus non intégratifs (comme le virus de Sendai), d’épisomes ou même un apport direct des ARNm ou des protéines permet d’éviter d’altérer le patrimoine génétique des patients.
Signalons qu’il existe des moyens de produire des cellules différenciées sans passer par des cellules souches telles que les cellules ES ou iPS. Une reprogrammation causée par l’expression forcée de facteurs de détermination a pu convertir des fibroblastes de peau en neurones, cardiomyocytes ou en cellules hématopoïétiques (phénomène de transdifférenciation) (Xu et al., 2020).
- Adhérences cellule-cellule
- Arabidopsis thaliana
- Axe antéro-postérieur chez la drosophile
- Biomécanique du développement
- Caenorhabditis elegans
- Concepts principaux
- Contrôle de la traduction
- Contrôle de la transcription
- Contrôle génétique et épigénétique
- Croissance du tube pollinique et double fécondation chez les Angiospermes
- Croissance et guidage axonal
- Des modèles animaux moins classiques
- Développement de l’oeil des Vertébrés
- Développement et évolution
- Et l’Humain ?
- Exercices sur l’ovogenèse, la spermatogenèse et la fécondation
- Exercices sur le contrôle de l’expression des gènes
- Exercices sur le développement des bourgeons de membre
- Exercices sur le développement des muscles striés squelettiques
- Exercices sur le développement des végétaux et les hormones végétales
- Exercices sur les cycles et les divisions cellulaires
- Exercices sur les étapes du développement, les inductions embryonnaires et la mise en place des axes de polarité
- Exercices sur les matrices extracellulaires, le cytosquelette et les adhérences cellule-cellule
- Exercices sur les voies de signalisation
- Glossaire
- Glossaire des termes liés à la génétique
- Glossaire des termes liés au cytosquelette, la matrice extracellulaire, l’adhérence et la migration cellulaire
- Hématopoïèse et développement des cellules du système immunitaire
- L’acide rétinoïque
- L’apoptose
- L’autophagie
- L’organogenèse
- L’ovogénèse prépare le développement embryonnaire
- La drosophile
- La fécondation
- La formation des somites
- La gastrulation
- La gastrulation (version allégée)
- La métamorphose chez les Hexapodes et les Amphibiens
- La neurogénèse chez les mammifères adultes
- La neurulation
- La poule
- La signalisation calcique
- La souris
- La superfamille TGFβ et ses voies de signalisation
- La voie de signalisation de l’auxine et ses rôles
- La voie de signalisation Hedgehog
- La voie de signalisation Hippo et ses composants YAP/TAZ
- La voie de signalisation Notch
- Le clivage
- Le cytosquelette
- Le destin des cellules et les réseaux de régulation génique
- Le développement des bourgeons de membre
- Le développement des muscles striés squelettiques
- Le développement des organes génitaux et des cellules germinales
- Le développement du cortex
- Le méristème apical caulinaire en phase végétative et lors de la formation d’une fleur
- Le poisson zèbre
- Le xénope
- Les cellules des crêtes neurales
- Les cellules et les gènes en action dans le développement
- Les cellules souches
- Les cellules tumorales
- Les cycles et les divisions cellulaires
- Les étapes du développement
- Les étapes du développement embryonnaire d’Arabidopsis thaliana et leur contrôle
- Les inductions embryonnaires et les gradients de morphogène
- Les matrices extracellulaires animales
- Les organismes modèles
- Les outils pour étudier l’expression et la fonction des gènes
- Les parois des cellules végétales
- Les techniques et les outils pour la biologie cellulaire
- Les transitions épithélio-mésenchymateuses et les migrations cellulaires
- Les vésicules extracellulaires
- Les voies de signalisation
- Les voies de signalisation FGF
- Mise en place des axes chez les Vertébrés
- Structures et processus cellulaires
- Voies de signalisation WNT
