par Patrick PLA, Université Paris-Saclay

La gastrulation est une étape critique dans le développement de tous les animaux, car c’est l’étape où les trois feuillets (ectoderme, mésoderme et endoderme) prennent leur position définitive dans l’embryon. Les cellules prolifèrent et surtout migrent abondamment pendant cette étape. Il y a aussi des migrations cellulaires à des étapes ultérieures du développement, mais ici, il s’agit de mouvements généralisés à l’échelle de l’embryon alors que plus tard, ce ne seront que des mouvements localisés.
La gastrulation, un terme introduit par Ernst Haeckel en 1872, veut dire littéralement “mise en place du gaster”, c’est-à-dire mise en place de l’intestin primitif. C’est une des principales résultantes de cette phase de développement, mais c’est une vision trop restreinte, car non seulement l’endoderme qui forme l’intestin est concerné mais aussi les deux autres feuillets.
La gastrulation chez les Amphibiens
La gastrulation a été très étudiée chez les Amphibiens, car ce sont les organismes où elle est particulièrement accessible et bien visible. Les mouvements de la gastrulation ont pu être mis en évidence par Vogt par la technique des marques colorées en 1929 où il y a utilisation de colorants vitaux (rouge neutre, bleu de Nil) pour marquer un groupe de cellules et suivre leur migration.

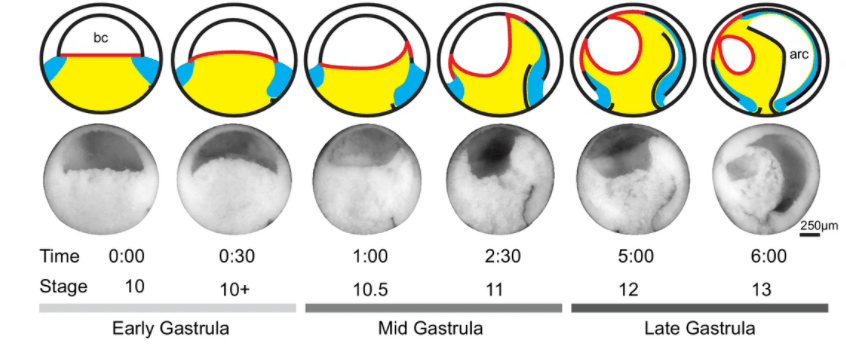
Ligne du haut : Carte des territoires et déformation des tissus des feuillets embryonnaires de X. laevis pour les stades 10 à 13. Les mouvements de l’ectoderme (blanc), du mésoderme (bleu) et de l’endoderme (jaune) sont indiqués. Le plancher du blastocœle est indiqué par une ligne rouge. Ligne médiane : Gastrulas en coupes sagittales aux stades 10 à 13. Le pôle animal est en haut, le pôle végétatif en bas, le côté ventral à gauche et le côté dorsal à droite. Ligne du bas : les gastrulas aux stades précoce, intermédiaire et avancé sont indiqués avec le stade de développement (stades définis par Nieuwkoop et Faber (1994)) et la chronologie correspondante. Le début de la gastrulation est fixé à 0:00 en heures et minutes. Le blastocœle (bc) et l’archentéron (arc) sont indiqués. Source : https://elifesciences.org/articles/27190
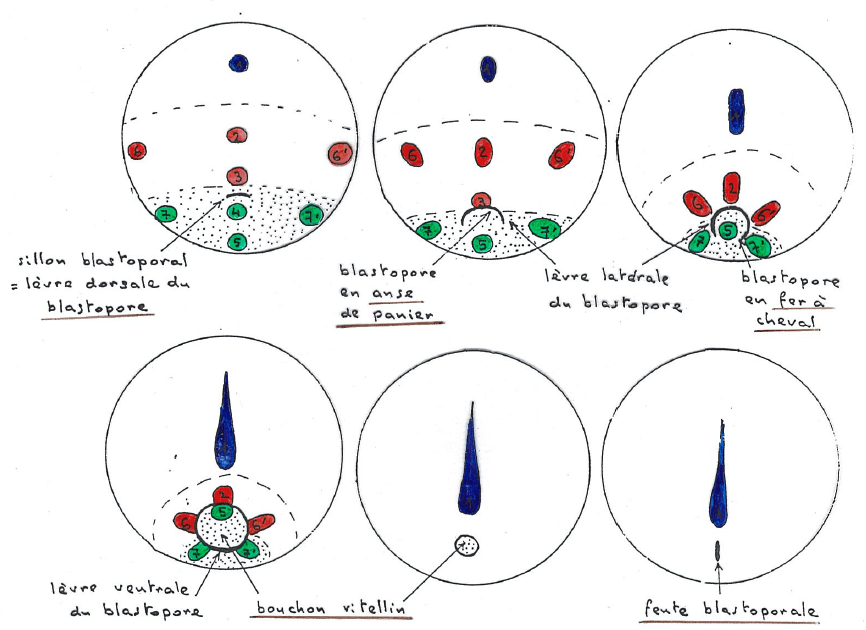
Durant la gastrulation, la cavité dans la blastula appelée blastocœle est envahie par des cellules. On observe qu’une invagination, le blastopore, se creuse et finit par former une cavité, l’archentéron, qui constituera la lumière du tube digestif. L’archentéron se développe au détriment du blastocœle qui est écrasé. Le mésoderme entre par la lèvre dorsale du blastopore et entraîne l’endoderme à l’intérieur. Une partie de l’endoderme forme le bouchon vitellin dans le blastopore. L’ectoderme qui recouvrait juste une partie de la surface de l’embryon, recouvre tout l’ensemble après la gastrulation.

Pour observer une vidéo de la gastrulation vue du pôle végétatif, suivre ce lien (et regarder uniquement la vidéo de gauche où l’embryon est normal).
Autre vidéo, également vue du pôle végétatif. On y voit aussi la neurulation suivre la gastrulation :
Les mouvements de la gastrulation chez les Amphibiens peuvent être caractérisés en plusieurs composantes :
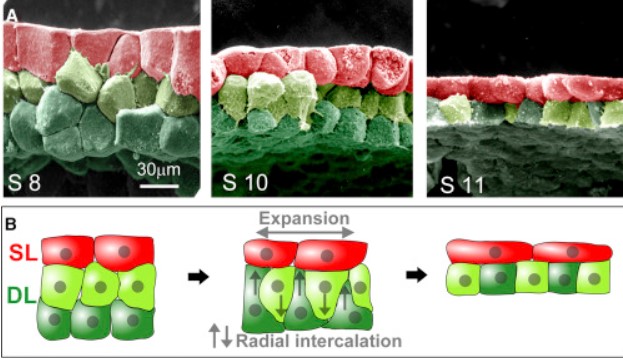
● L’épibolie est le mouvement de recouvrement de l’ensemble de la surface de l’embryon par l’ectoderme (alors qu’avant la gastrulation, l’ectoderme ne recouvre que l’hémisphère animal, le reste de la surface étant de l’endoderme). Deux processus interviennent dans cette augmentation de surface : la prolifération cellulaire et aussi l’intercalation radiaire : initialement l’ectoderme est constitué de 3 couches de cellules. Au cours de la gastrulation, les cellules des 2 couches profondes s’intercalent les unes avec les autres ce qui finit par ne faire qu’une couche profonde : cela crée mécaniquement plus de surface d’ectoderme (analogie de la pâte à modeler moins épaisse mais plus étendue).
● L’encoche blastoporale se forme par l’invagination de cellules en bouteille. Ces cellules ont un « cou » sous-apical mince et le reste du cytoplasme forme un bulbe basal. Ce sont des cellules de l’endoderme pharyngien qui se déforment ainsi grâce à l’action de leur cytosquelette : la constriction apicale est due aux microfilaments d’actine associés à la myosine et l’élongation est due aux microtubules.
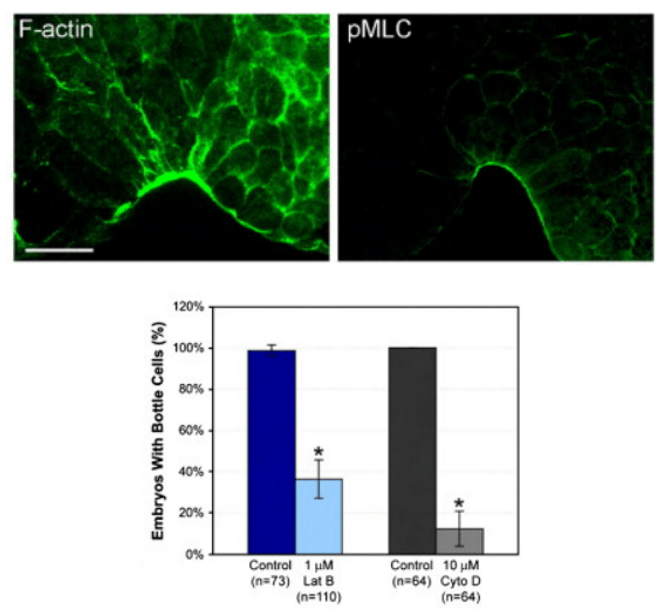
Si on isole les cellules de l’endoderme pharyngien, la constriction apicale a lieu alors que l’élongation ne se fait pas, ce qui indique que la constriction apicale se fait de manière autonome tandis l’élongation dépend de l’interaction avec les cellules adjacentes (Hardin et Keller, 1988).
La constriction apicale s’accompagne aussi d’endocytose qui a probablement pour rôle de diminuer la surface membranaire du côté de la constriction (Lee et Harland, 2010)
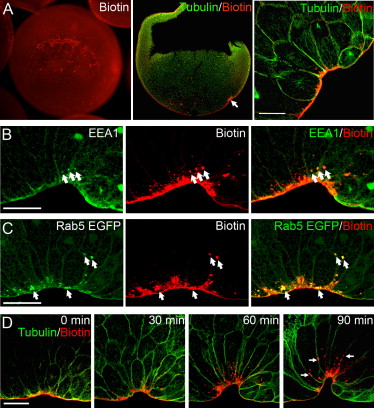
(A) Vue du pôle végétatif (gauche), coupe sagittale médiane (centre) et grossissement supérieur de la coupe sagittale médiane (à droite) des embryons de stade 10 marqués avec NHS-LC-sulfo biotine (reconnu par un anticorps fluorescent rouge couplé à la streptavidine) et avec un anticorps anti-DM1α (tubuline, vert). La flèche indique les cellules en bouteille. Barre d’échelle = 25 µm. (B) Sections confocales sagittales médianes d’embryons colorées avec un anticorps anti-EEA1 (un marqueur d’endosome précoce, vert) et la biotine est repérée en rouge. On constate que la biotine d’origine externe est colocalisée avec le marqueur d’endosome précoce, mettant en évidence une endocytose. (C) Sections confocales sagittales médianes d’embryons injectés d’ARNm de Rab5 couplé à la eGFP (Rab5 est présent dans les endosomes précoces) puis fixées et colorées avec de l’anticorps anti-GFP. Les flèches dans (B) et (C) indiquent la colocalisation de la biotine avec des marqueurs d’endosomes précoces. (D) Sections confocales sagittales médianes d’embryons après marquage pulse-chasse avec de la biotine (incubation avec de la biotine limitée dans le temps puis incubation sans biotine). Les embryons ont été fixés aux moments indiqués et colorés avec de l’anti-DM1α (tubuline) et de la streptavidine (qui se lie à la biotine). Les flèches indiquent les endosomes qui semblent être sur ou près de la membrane basolatérale. Dans toutes les coupes sagittales médianes, les images sont orientées le côté végétatif vers le bas à gauche.
Barres d’échelle pour (B)–(D) = 50 µm. Source : https://www.cell.com/current-biology/fulltext/S0960-9822(09)02143-5
Avec un délai de 2h, les cellules en bouteille apparaissent aussi latéralement et ventralement, complétant une zone de constriction apicale circulaire : le blastopore prend la forme d’un anneau après avoir eu une forme de anse de panier puis de fer à cheval.
Les cellules en bouteille servent de butée lors de l’initiation de la gastrulation pour les cellules mésodermiques qui remontent ainsi vers l’hémisphère animal (involution – voir juste après).
● L’involution est le mouvement du mésoderme qui passe par la lèvre dorsale du blastopore et qui fait une rotation de presque 180° pour remonter par l’intérieur le long des couches superficielles de l’hémisphère animal.

● Les cellules en tête de la lame de cellules mésodermiques qui pénètrent dans l’embryon migrent activement le long de la matrice extra-cellulaire riche en fibronectine qui recouvre l’intérieur du toit du blastocœle.

Si on retourne le toit du blastocœle (de telle manière à ce qu’il n’y ait plus de fibronectine du bon côté), ou si on empêche les interactions fibronectine-intégrine par des peptides RGD qui servent de « leurres » aux intégrines, les mouvements de migration sont inhibés, ce qui donne des embryons déformés. L’épibolie n’étant pas perturbé dans ce cas, la surface de l’embryon se plisse.
L’endoderme a longtemps été considéré comme passif lors de la gastrulation des amphibiens mais des méthodes d’imagerie plus fines ont permis de mettre en évidence des mouvements actifs de ses cellules (voir par exemple cette vidéo).
● La convergence-extension est le mouvement qui permet l’allongement de l’embryon selon l’axe antéro-postérieur à la fin de la gastrulation et lors de la neurulation. Le tissu qui s’allonge devient en même temps plus étroit d’où le terme de convergence associé à l’extension. Des cellules de la corde (mais aussi du neurectoderme qui va former le tube neural) deviennent polarisées, convergent de la droite ou de la gauche vers le plan médian (ou plan de symétrie bilatérale) et s’intercalent ce qui a pour effet de créer une force qui allonge l’embryon le long de l’axe antéro-postérieur.
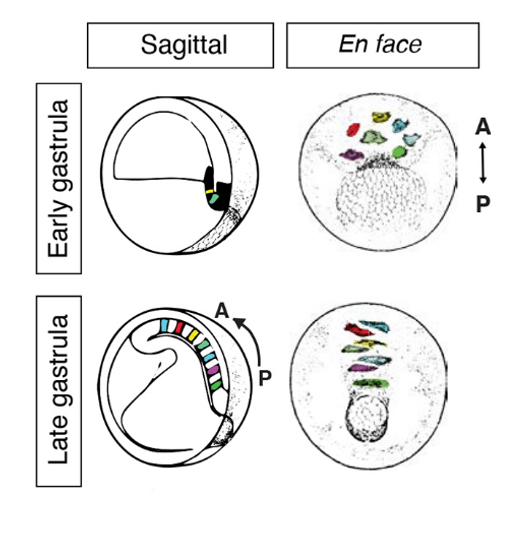
Des explants dits sandwich, adapté de Schechtman (1942), montrent que le
mésoderme chordal/somitique présomptif et que le tube neural postérieur présomptif peuvent avoir un mouvement de convergence-extension alors qu’ils ne sont pas attachés à un substrat et sont indépendants d’autres processus générateurs de force dans l’embryon (Keller et Danilchik, 1988). Les mouvements de convergence-extension proviennent donc de déterminants intrinsèques à la population de cellules concernée.
Chez le xénope mais aussi chez le poisson-zèbre, l’allongement de l’embryon le long de l’axe antéro-postérieur ne provient pas seulement des mouvements de convergence-extension mais aussi, un peu plus tard, d’une vacuolisation des cellules de la corde, notamment celles qui se trouvent dans sa partie antérieure (McLaren et al., 2021). Des glycosaminoglycanes sont sécrétés dans les vacuoles ce qui favorise l’absorption osmotique d’eau et l’augmentation de leur taille.

Le blastopore, en train de se refermer, est rempli par un bouchon vitellin formé par des macromères végétatifs riches en vitellus. Il est repoussé vers l’arrière et donne l’anus (nous sommes chez un Deutérostomien).

Voir également ce site sur la gastrulation des amphibiens.
La gastrulation chez les Amniotes
L’embryon de poulet est un organisme modèle pratique pour l’étude de la gastrulation chez les amniotes, car il est plat, transparent et se développe à l’extérieur de la mère (contrairement à l’embryon de souris qui est incurvé « en hamac » et implanté dans l’utérus maternel). Les mouvements cellulaires pendant la gastrulation sont cependant similaires chez les oiseaux et les mammifères.
Au moment de la ponte, c’est-à-dire à la fin du clivage, l’embryon de poulet est constitué d’environ 20 000 à 30 000 cellules. Un sous-ensemble de ces cellules forme un disque quasi-épithélial épais d’une seule couche, l’épiblaste, d’un diamètre de 3 mm. À la périphérie de l’embryon, l’épiblaste repose sur une couche rigide de plusieurs cellules épaisses de grandes cellules mésenchymateuses, qui entrent directement en contact avec le vitellus sous-jacent. Cette portion externe est connue sous le nom d’Area Opaca (AO) et ne donnera que des tissus extra-embryonnaires. La partie centrale est l’Area Pellucida (AP) et l’ensemble de l’embryon stricto sensu provient de cette partie. La couronne de tissu séparant l’AO et l’AP s’appelle la zone marginale (MZ).
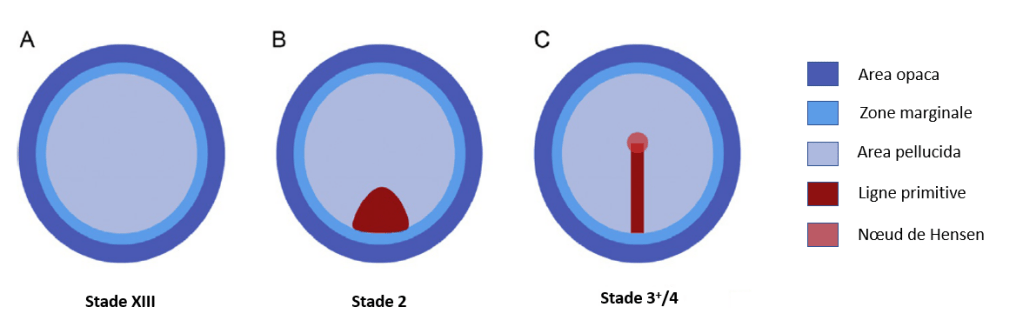
Lorsque la MZ est retirée et que l’AO entoure directement l’AP centrale, une nouvelle MZ est induite, exprimant des marqueurs génétiques spécifiques tels que ASTL (Lee et al., 2022). L’AO joue donc un rôle dans l’établissement de la MZ et le signal envoyé par l’AO a été identifié comme étant Wnt8c (Fadaili et al., 2025).
Dans l’AP, des amas de quelques petites cellules arrondies s’attachent à la face ventrale (inférieure) de l’épiblaste, formant l’hypoblaste primaire. L’hypoblaste primaire s’aplatit pour former une couche épithéliale de grandes cellules minces, l’hypoblaste. L’hypoblaste tout comme l’AO ne forme que des structures extra-embryonnaires.
Une bande de cellules épithéliales à la limite latérale postérieure entre l’AO et l’AP (la zone marginale postérieure ou PMZ) prend une forme allongée, formant le croissant de Koller en s’épaississant. C’est l’étape de pré-gastrulation qui rend visible la perte de la symétrie circulaire qui était jusqu’alors celle de la morphologie de l’embryon. Les signaux inductifs dans la zone marginale sont constitués par cVg1, un ligand de la famille de TGFβ, dans la PMZ et un gradient de Wnt8c dans l’AO (plus exprimé dans la région postérieure) (Skromme et Stern, 2001). Ils induisent une expression de Nodal dans l’épiblaste recouvrant le croissant de Koller et les cellules qui sont spécifiées en mésendoderme (les cellules mésodermiques ne sont pas clairement séparées des cellules endodermiques à ce stade).
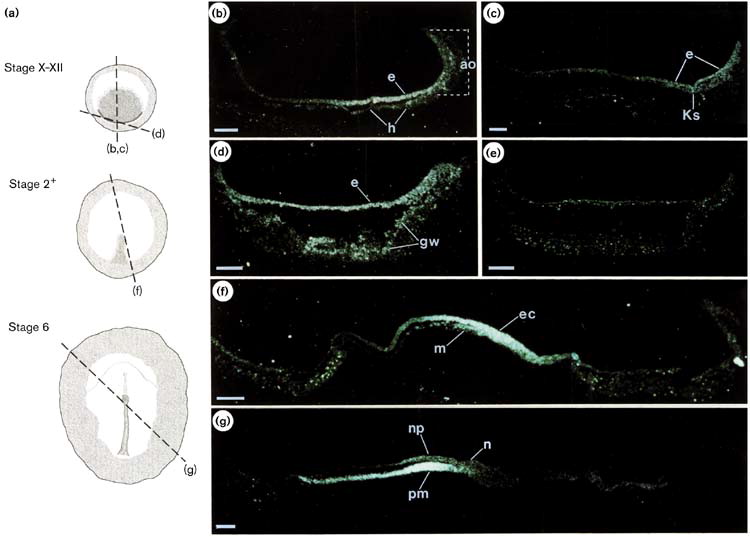
L’expression dans la PMZ de cVg1 est activée par le facteur de transcription Pitx2 (Torlopp et al., 2014). Une autre manifestation de l’axe antéro-postérieur est l’expression de Gata2 qui est exprimé dans l’épiblaste de l’AO selon un gradient antéro-postérieur (expression plus forte dans la région antérieure). La fonction de Gata2 dans la région antérieure est d’empêcher à cet endroit la succession d’évènements qui ont lieu dans la région postérieure ce qui permet d’éviter la formation de deux axes (Bertocchini et Stern, 2012). L’expression de Gata2 est activée par BMP4 qui est exprimé exclusivement antérieurement.
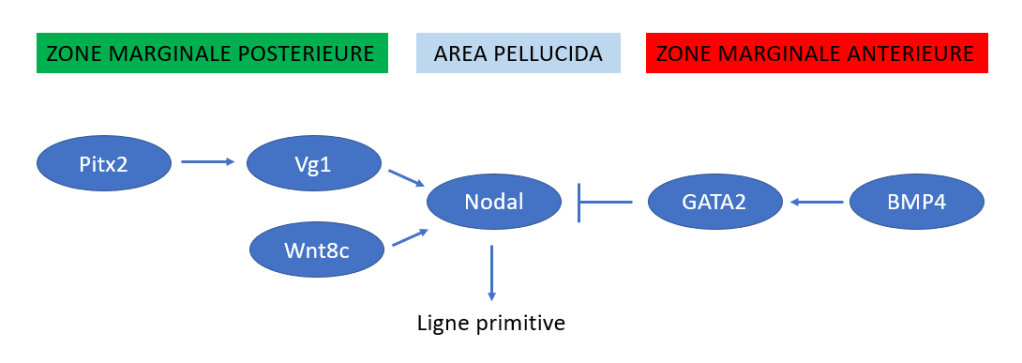
Dans la région postérieure, la ligne primitive qui caractérise l’étape suivante du développement ne se forme pas immédiatement car l’action de Nodal est restreinte par l’hypoblaste sous-jacent qui secrète l’antagoniste Cerberus (Voiculescu et al., 2014). Cette sécrétion finit par se tarir.
La gastrulation stricto sensu commence par la formation de la ligne primitive, alors que le mésendoderme de la région du croissant de Koller à l’interface entre l’AO et l’AP se déplace dans la région médiane postérieure de l’embryon. Cet événement a lieu 10h après la ponte (stade Hamburger et Hamilton HH2) et est entièrement dépendant de la bonne formation préalable du croissant de Koller que nous avons vu aux paragraphes précédents.
Lorsque des cellules COS de mammifères transfectées avec un vecteur d’expression de cVg1 sont greffées sur la MZ dans la future région antérieure de l’embryon (donc du côté opposé à l’expression habituelle de cVg1), une ligne primitive ectopique se développe dans plus de 50 % des cas montrant le rôle inductif de cVg1 dans la formation de la ligne primitive (Seleiro et al., 1996).
Lorsqu’on réitère la même expérience aux stades HH 2 ou 4, alors que la ligne primitive normale s’est déjà formée, rien ne se passe montrant que la compétence des tissus s’est éteinte (Shah et al., 1997).
La ligne primitive s’allonge vers l’avant jusqu’à son extension maximale 18 heures après la ponte (stade HH4), atteignant les deux-tiers du diamètre de l’AP. Son extrémité antérieure s’épaissit et forme le nœud de Hensen, l’homologue de la lèvre dorsale du blastopore, c’est-à-dire l’organisateur de Spemann. Chez les Amniotes, le nœud de Hensen est non seulement impliqué dans l’induction neurale mais aussi dans la mise en place de l’axe droite-gauche.
Pour voir une vidéo de la formation et de l’allongement de la ligne primitive, suivre ce lien.

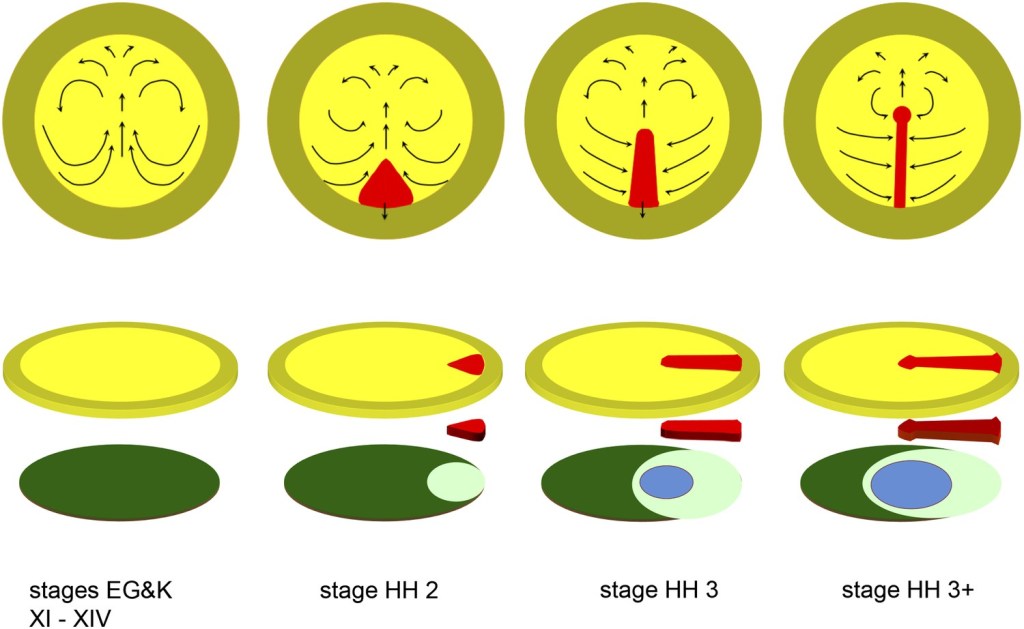
La ligne supérieure de schémas montre les embryons aux stades XI-XIV (avant la ligne primitive), HH2 (ligne primitive précoce), HH3 (ligne primitive moyenne) et HH3+ (ligne primitive moyenne à tardive), vus du côté dorsal (épiblaste). Les flèches désignent les principaux mouvements morphogénétiques (dits «à la Polonaise » ou en tourbillon) se produisant dans le plan de l’épiblaste. Après le stade 4 (fin de la gastrulation), la convergence des cellules et leur entrée par la partie antérieure de la ligne primitive ralentit ou cesse (et ces mouvements continuent à travers les parties médiane et postérieure de la ligne primitive). L’épiblaste antérieur à la ligne primitive (future plaque neurale) s’allonge (Sheng et al., 2003). Plus tard, la ligne primitive commence à régresser, allongeant davantage la plaque neurale postérieurement (Spratt, 1947). La ligne inférieure de schémas montre une vue éclatée des embryons à chacun des stades ci-dessus, avec la rangée supérieure de schémas représentant la couche supérieure (épiblaste en nuances de jaune), la rangée inférieure montrant la couche inférieure (nuances de bleu/vert : hypoblaste en vert foncé, endoblaste en vert clair, endoderme définitif ou intestinal en bleu) et la rangée centrale montrant la couche médiane (mésodermique) (ligne primitive, en rouge). Au sein de l’épiblaste, la région centrale (jaune) est l’area pellucida et la région externe (moutarde) est l’area opaca extra-embryonnaire. Source : https://elifesciences.org/articles/01817
Pour former cette ligne primitive, d’importants flux tourbillonnaires de cellules se déroulent dans l’épiblaste. Ces tourbillons tournent dans des directions opposées, à partir de la ligne médiane dans la partie antérieure et vers la ligne médiane dans la partie postérieure. Dans la partie postérieure de l’épiblaste, là où les flux cellulaires se rencontrent, les cellules s’empilent les unes sur les autres et l’épiblaste devient épais de plusieurs diamètres cellulaires, formant la structure visible sous la forme de la ligne primitive.
Les mouvements de la gastrulation chez l’oiseau sont déterminés par la contraction graduelle d’un anneau d’actomyosine supracellulaire à grande échelle localisé entre les territoires embryonnaire et extraembryonnaire. La propagation de ces forces est rendue possible par une réponse similaire à celle d’un fluide du disque embryonnaire épithélial et cette réponse dépend de la division cellulaire. Un modèle mathématique simple de mouvement fluidique provoqué par un anneau de tension est capable de modéliser les mouvements tourbillonnaires qui accompagnent la formation de la ligne primitive. La géométrie de l’embryon en gastrulation résulte ainsi en partie de la transmission de forces actives générées le long de sa frontière entre l’area pellucia et l’area opaca (Saadaoui et al., 2020).
La ligne primitive s’allonge vers l’avant par des mouvements de convergence extension que vous pouvez observer sur ce lien.
Et également sur cette vidéo (très brève) :
Une fois que la ligne primitive s’est étendue à travers l’épiblaste, les cellules plus profondes de la ligne primitive commencent à s’éloigner radialement de l’axe sagittal car elles sont remplacées par des cellules de l’épiblaste qui pénètrent dans la ligne primitive après avoir subi une transition épithélio-mésenchymateuse.

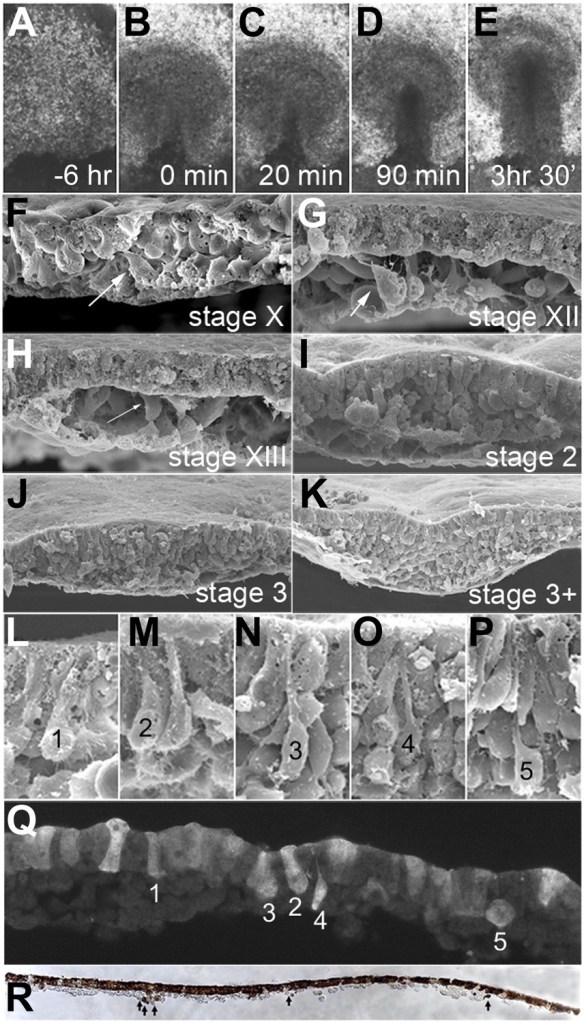
(A–E) Images montrant l’épiblaste uniforme 6 heures (A, stade EG&K XII) et juste avant la formation de la ligne primitive (B, stade EG&K XIV), la première apparition de la ligne primitive (C, stade HH2), l’accumulation de mésoderme sous la ligne primitive (D, stade HH3), apparition d’un sillon dans la ligne primitive et l’émigration du mésoderme (E, stade HH3+). (F-K) Microscopie électronique à balayage d’embryons fracturés avant (F-H) et après (I-K) formation de la ligne primitive. Les flèches blanches indiquent une transition épithélio-mésenchymateuse (TEM) possible avant la formation de la ligne primitive. (L–P) Microscopie électronique à balayage de ligne primitive fracturée, montrant des cellules en TEM avec divers degrés de constriction apicale et d’expansion basolatérale (classées comme « stades d’entrée 1 à 5 »). (Q) Cet embryon a été cultivé pendant 1 heure après électroporation d’un morpholino fluorescent témoin dans tout l’épiblaste au stade XI, puis sectionné sagittalement et visualisé sous fluorescence. Les cellules marquées dans l’épiblaste présentent des morphologies similaires à celles des images de microscopie électronique (panneaux L-P, « stades d’entrée 1 à 5 »). (R) Cet embryon a été cultivé pendant 4 heures après électroporation d’un morpholino fluorescent témoin dans tout l’épiblaste au stade XI, puis fixé (au stade XII), sectionné sagittalement et coloré avec un anticorps anti-fluorescéine (marron). La coupe montre plusieurs cellules qui ont quitté l’épiblaste et se trouvent maintenant dans l’espace sous-jacent dans toute l’étendue antéro-postérieure de l’embryon (flèches). Source : https://elifesciences.org/articles/01817
Les cellules de l’épiblaste latéral commencent à se déplacer médialement vers la ligne primitive pour remplacer les cellules que la ligne perd par pénétration. Les premières cellules à pénétrer forment l’endoblaste ou endoderme définitif, qui remplace l’hypoblaste. Entrent ensuite les cellules du mésoderme.
Sur la vidéo suivante, on voit bien les mouvements des cellules de l’épiblaste. La ligne primitive se situe en bas à gauche :
La ligne primitive régresse au cours de la dernière phase de la gastrulation lorsque le nœud de Hensen se déplace vers l’arrière. La ligne primitive se raccourcit jusqu’à ce qu’elle disparaisse finalement dans les stades où a lieu la formation des premiers somites. Plus en avant, la neurulation et la formation du tube neural a déjà commencé. Il y a une désynchronisation des phases de développement chez les Amniotes avec l’avant qui est plus mature que l’arrière. Ce n’est pas le cas chez les Amphibiens.
La gastrulation des Amniotes est complexe et il ne faut pas tomber dans des dichotomies caricaturales. Par exemple, les cellules mésodermiques qui pénètrent sont essentiellement mésenchymateuses et se déplacent en tant qu’individus, mais elles le font de manière très coordonnée, formant des contacts fréquents avec les cellules voisines. Signalons aussi que les flux cellulaires associés à la formation de la ligne primitive ont lieu dans une couche épithéliale de cellules reposant sur une lame basale complexe et reliées par des jonctions adhérentes et serrées bien développées. Ainsi, il ne faut pas tomber dans la caricature suivante : cellules épithéliales = cellules statiques. Cellules mésenchymateuses individualisées = cellules en mouvement.
L’un des concept clé pour comprendre les mouvements au sein d’un épithélium est la polarité cellulaire planaire (PCP). La voie de signalisation Wnt non canonique est l’un des nombreux régulateurs de la PCP. L’inhibition de la voie Wnt-PCP perturbe la formation de la ligne primitive. Par exemple, une version dominante négative de Dishevelled (Dsh-ΔDEP), qui inhibe spécifiquement la voie Wnt-PCP mais n’affecte pas la signalisation Wnt canonique (dépendante de la β-caténine), n’interfère pas avec la spécification du mésoderme mais abolit l’allongement de la ligne primitive. Un résultat similaire est obtenu par électroporation d’un mélange de morpholinos inhibant PRICKLE1, CELSR1 et VANGL2, des protéines impliquées dans la voie Wnt-PCP (Voiculescu et al., 2007). Chez le poisson zèbre, des mutations dans le locus vangl2 perturbent les mouvements de convergence-extension pendant la gastrulation, entraînant un axe antéro-postérieur raccourci et un corps élargi (Solnica-Krezel et al., 1996).
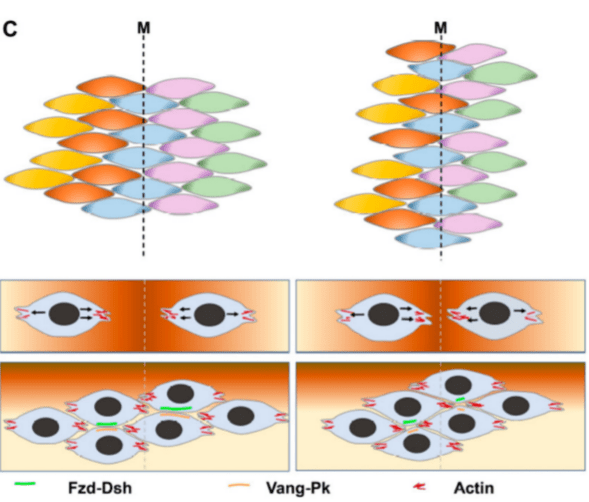
La gastrulation chez la souris a été moins étudiée que chez la poule car elle est moins accessible et la topologie est compliquée par la forme « en hamac » que prend l’embryon et par la présence de structures extra-embryonnaires plus étendues à ce stade chez la souris que chez la poule. Mais les mécanismes fondamentaux restent les mêmes. Notons que l’embryon humain n’a pas cette forme en hamac et sa forme ressemble plus à celle de l’embryon de poule. La gastrulation chez l’Homme commence 14 jours après la fécondation.
Après l’implantation de l’embryon de souris dans l’utérus maternel au stade tardif du blastocyste, l’embryon prend la forme d’un cylindre radialement symétrique constitué d’un épithélium à deux couches, qui est composé d’épiblaste et d’endoderme viscéral distalement, et d’épiblaste et d’ectoderme extra-embryonnaire de manière proximale au site d’implantation.
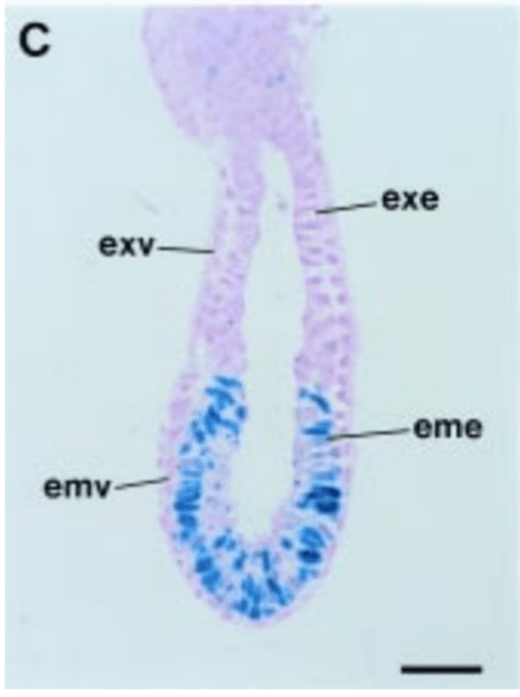
exe = ectoderme extra-embryonnaire. emv = endoderme viscéral. exv = endoderme viscéral extraembryonnaire
Barre d’échelle = 25 µm. Source : http://www.ijdb.ehu.es/web/descarga/paper/10794075
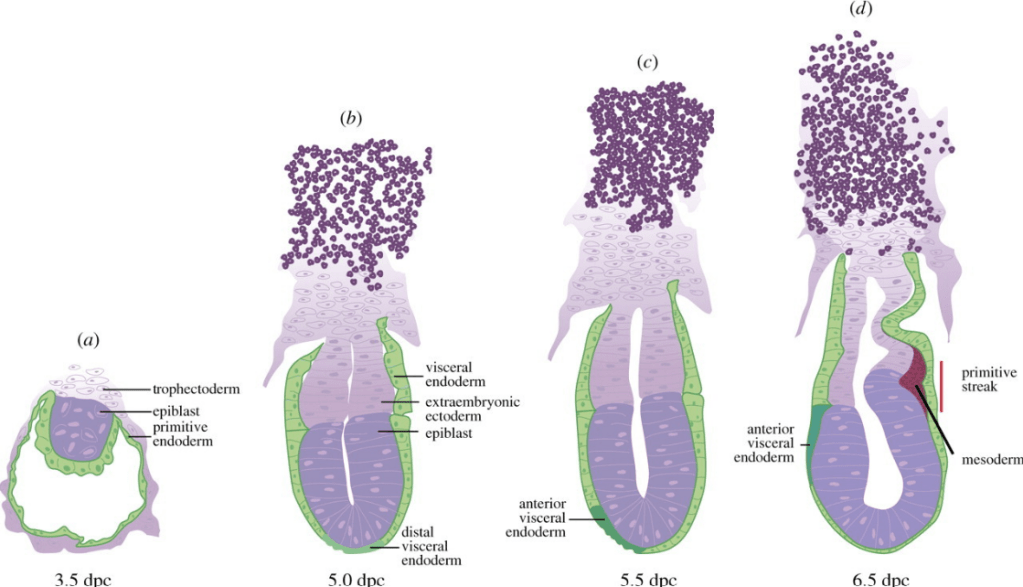
Au cours de la gastrulation chez la souris, la ligne primitive se forme à E6,25 dans l’épiblaste postérieur, à la jonction entre les régions embryonnaires et extra-embryonnaires (notez l’homologie avec la zone marginale postérieure de l’embryon de poulet entre l’area pellucida et l’area opaca).
C’est l’activation différentielle de la voie de signalisation Nodal dans l’épiblaste postérieur (et non pas antérieur) qui permet la formation localisée de la ligne primitive (voir les mécanismes plus loin) (Brennan et al., 2001). De même, la voie Wnt est active dans la partie postérieure mais pas antérieure avec par exemple Wnt3 qui est exprimé dans l’épiblaste postérieur et dans l’endoderme viscéral postérieur (Liu et al., 1999; Rivera-Perez et al., 2005) tandis que l’endoderme viscéral antérieur exprime plutôt des antagonistes de Wnt. Cette asymétrie est essentielle pour la mise en place de l’axe antéro-postérieur de l’embryon et la formation de la ligne primitive.
La ligne primitive s’allonge ensuite jusqu’à l’extrémité antérieure de l’embryon. Cette ligne primitive est la région de l’embryon où les cellules épiblastiques se délaminent par transition épithéliale-mésenchymateuse pour générer une population de cellules mésenchymateuses qui forme le mésoderme et les couches de l’endoderme définitif (par opposition à l’endoderme primitif). On constate une fois de plus l’homologie avec ce que nous avons décrit chez la poule.
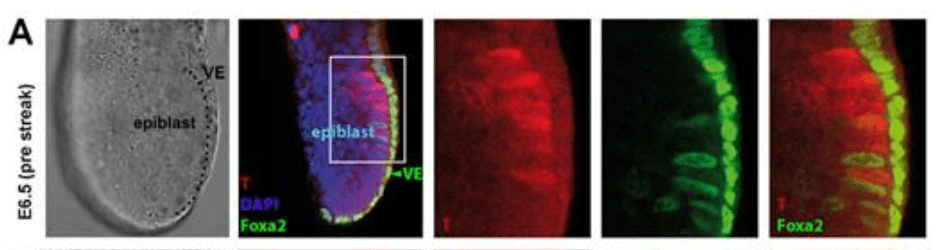
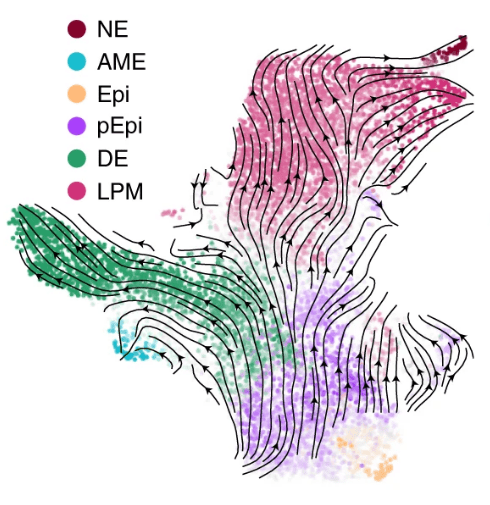
Lors de la gastrulation, les cellules de l’épiblaste qui forment un épithélium incurvé et qui migrent en même temps sont soumises à des tensions mécaniques importantes, notamment dans leur région apicale.

La protéine ASPP2 qui est présente dans les jonctions apicales est alors nécessaire pour maintenir l’intégrité de l’épithelium dans des conditions de fortes contraintes biomécaniques (Royer et al., 2022).
La transition épithélio-mésenchymateuse dans la ligne primitive est sous la dépendance du facteur de transcription Snail (ce qui sera aussi le cas un peu plus tard au cours du développement, pour la transition épithélio-mésenchymateuse des cellules de crêtes neurales). Snail réprime notamment directement l’expression de la E-cadhérine épiblastique et active l’expression de marqueurs mésenchymateux tels que la vimentine.
Voir la page sur les transitions épithélio-mésenchymateuses et les migrations cellulaires.
Après la transition épithélio-mésenchymateuse et le passage par la ligne primitive, les cellules du mésoderme migrent en avant vers leurs sites à destinée embryonnaire ou latéralement pour former du mésoderme extra-embryonnaire (plutôt dans la région postérieure de la ligne primitive). Le mésoderme extra-embryonnaire contribue à l’amnios, à l’allantoïde, au chorion et au sac vitellin (ou vésicule vitelline). Ce dernier a des fonctions importantes dans la protection et la communication materno-fœtale, ainsi que dans l’érythropoïèse primitive. Des études de lignage montrent que la destinée des cellules du mésoderme dépend du moment et de l’endroit où elles quittent la ligne primitive à la gastrulation.
Des études en microscopie électronique ont montré que les jeunes cellules du mésoderme ont des protubérances, suggérant que ces cellules les utilisent pour migrer activement. Le cytosquelette se réorganise de manière rapide dans ces cellules et les petites GTPases RhoA et Rac1, des médiateurs de la réorganisation du cytosquelette, sont nécessaires au bon déroulement de la migration du mésoderme chez la souris (Migeotte et al., 2011). Les embryons avec la mutation tw9 (également appelée tw18) présentent des défauts majeurs de formation du mésoderme avec des cellules dépourvues de filopodes. Le gène affecté code une sous-unité de la sérine/thréonine phosphatase PP2A qui est sous le contrôle de la petite GTPase Rho (Bousquet et al., 2016).
Brachyury ou T est un gène très important pour le développement du mésoderme lors de la gastrulation et ce, quelque soit le vertébré. Brachyury est le membre fondateur d’une famille de facteurs de transcription caractérisés par un domaine de liaison à l’ADN conservé, la boîte T ou T-box. À partir d’un orthologue brachyury dans l’ancêtre commun des métazoaires et des champignons, plusieurs gènes T-box ont été générés par duplication, et ils se sont encore diversifiés au sein des métazoaires (Sebé-Pedrós et al., 2013 ; Papaioannou, 2014 ; Gentsch et al., 2017). Le nom du gène Brachyury fait référence au phénotype le plus évident du mutant T hétérozygote de souris, une queue tronquée, qui a été décrit par Dobrovolskaia-Zavadskaia dès 1927. Les mutations homozygotes T−/− sont léthaux pour l’embryon et présentent une accumulation de cellules du mésoderme au niveau de la ligne primitive de la gastrula et une perte du mésoderme postérieur.
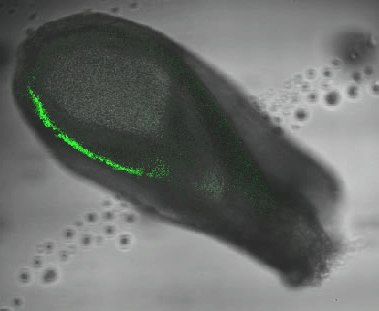

Des expériences comme celles montrées ci-dessus ont démontré que Brachyury est nécessaire à la transition épithélio-mésenchymateuse des cellules du mésoderme au cours de la gastrulation (Turner et al., 2014).
Pour les cellules de l’endoderme, la transition épithélio-mésenchymateuse n’est que partielle et le facteur de transcription Foxa2 (qui est exprimé dans l’endoderme mais pas dans le mésoderme) est responsable de cette transition incomplète (Scheibner et al., 2021). Le facteur de transcription Sox17 est essentiel pour la détermination des cellules endodermiques. Il est notamment requis pour la synthèse de la membrane basale de l’endoderme qui permet de bien séparer ce feuillet du mésoderme après la migration (Viotti et al., 2014). La voie Wnt/β-caténine est également essentielle et les cellules endodermiques où on la rend non fonctionnelle deviennent des cellules mésodermiques cardiaques (Lickert et al., 2002). Par ailleurs, certaines cellules issues de l’endoderme viscéral participent aussi à la formation de l’endoderme qui forme le tube digestif de l’embryon, comme l’ont montré des données de transcriptomique en cellules isolées (Nowotschin et al., 2019).
Lors de la phase précoce de la gastrulation des Mammifères, des mouvements sont aussi requis dans les tissus extraembryonnaires, notamment l’endoderme viscéral distal qui migre dans la future région antérieure pour devenir l’endoderme viscéral antérieur (AVE). La migration cellulaire épithéliale collective dans l’AVE le positionne correctement et c’est important car il produit des inhibiteurs de la signalisation de Wnt et Nodal (par exemple, Lefty1, Dkk1, Cerberus1) qui évitent que la ligne primitive se forme du côté antérieur (Belo et al., 1997, Kemp et al., 2005, Perea-Gomez et al., 2002).
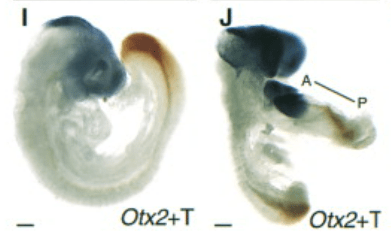
Parmi les facteurs essentiels à la migration des cellules de l’AVE, on peut citer les petites GTPases et leurs activateurs, les GEF (guanine nucleotide exchange factor). β-Pix (Arhgef7) est une GEF des GTPases Rac1 et Cdc42 et qui se localise sur les adhérences focales. β-Pix favorise à la fois la formation des protubérances cellulaires et inhibe la maturation des adhérences focales. Les embryons de souris mutantes nulles β-Pix arrêtent leur développement avant E8.0 et ne parviennent pas à spécifier un axe antéro-postérieur car β-Pix est requis pour la migration épithéliale collective des cellules de l’AVE. En l’absence de β-Pix, les cellules de l’AVE forment de multiples protubérances cellulaires en raison de l’échec de la localisation de l’activité Rac1 qui dépend de Cdc42. Cette multitude de protubérances ne permet pas de faire migrer les cellules dans une direction précise. La migration collective de cette population épithéliale échoue ce qui aboutit à des signalisations Wnt et Nodal non circonscrites et un axe antéro-postérieur correct ne peut pas se former.
Après la gastrulation, vient l’étape de la neurulation.
EN DIRECT DES LABOS : La formation de gastruloïdes
LA CARTE MENTALE :

DES MOTS CROISES POUR REVISER

VOIR DES EXERCICES SUR LES ETAPES DU DEVELOPPEMENT EMBRYONNAIRE
- Adhérences cellule-cellule
- Arabidopsis thaliana
- Axe antéro-postérieur chez la drosophile
- Biomécanique du développement
- Caenorhabditis elegans
- Concepts principaux
- Contrôle de la traduction
- Contrôle de la transcription
- Contrôle génétique et épigénétique
- Croissance du tube pollinique et double fécondation chez les Angiospermes
- Croissance et guidage axonal
- Des modèles animaux moins classiques
- Développement de l’oeil des Vertébrés
- Développement et évolution
- Et l’Humain ?
- Exercices sur l’ovogenèse, la spermatogenèse et la fécondation
- Exercices sur le contrôle de l’expression des gènes
- Exercices sur le développement des bourgeons de membre
- Exercices sur le développement des muscles striés squelettiques
- Exercices sur le développement des végétaux et les hormones végétales
- Exercices sur les cycles et les divisions cellulaires
- Exercices sur les étapes du développement, les inductions embryonnaires et la mise en place des axes de polarité
- Exercices sur les matrices extracellulaires, le cytosquelette et les adhérences cellule-cellule
- Exercices sur les voies de signalisation
- Glossaire
- Glossaire des termes liés à la génétique
- Glossaire des termes liés au cytosquelette, la matrice extracellulaire, l’adhérence et la migration cellulaire
- Hématopoïèse et développement des cellules du système immunitaire
- Histoire de la biologie cellulaire et de la biologie du développement
- L’acide rétinoïque
- L’apoptose
- L’autophagie
- L’organogenèse
- L’ovogénèse prépare le développement embryonnaire
- La drosophile
- La fécondation
- La formation des somites
- La gastrulation (version allégée)
- La métamorphose chez les Hexapodes et les Amphibiens
- La neurogénèse chez les mammifères adultes
- La neurulation
- La poule
- La signalisation calcique
- La souris
- La superfamille TGFβ et ses voies de signalisation
- La voie de signalisation de l’auxine et ses rôles
- La voie de signalisation Hedgehog
- La voie de signalisation Hippo et ses composants YAP/TAZ
- La voie de signalisation Notch
- Le clivage
- Le cytosquelette
- Le destin des cellules et les réseaux de régulation génique
- Le développement des bourgeons de membre
- Le développement des muscles striés squelettiques
- Le développement des organes génitaux et des cellules germinales
- Le développement du cortex
- Le méristème apical caulinaire en phase végétative et lors de la formation d’une fleur
- Le poisson zèbre
- Le xénope
- Les cellules des crêtes neurales
- Les cellules et les gènes en action dans le développement
- Les cellules souches
- Les cellules tumorales
- Les cycles et les divisions cellulaires
- Les étapes du développement
- Les étapes du développement embryonnaire d’Arabidopsis thaliana et leur contrôle
- Les inductions embryonnaires et les gradients de morphogène
- Les matrices extracellulaires animales
- Les organismes modèles
- Les outils pour étudier l’expression et la fonction des gènes
- Les parois des cellules végétales
- Les techniques et les outils pour la biologie cellulaire
- Les transitions épithélio-mésenchymateuses et les migrations cellulaires
- Les vésicules extracellulaires
- Les voies de signalisation
- Les voies de signalisation FGF
- Mise en place des axes chez les Vertébrés
- Structures et processus cellulaires
- Voies de signalisation WNT
