Par Patrick PLA, Université Paris-Saclay
- Bicoid et Nanos
- Un exemple de gène gap précoce : hunchback
- Des gènes gap aux gènes homéotiques
- Les gènes homéotiques
Les insectes sont des organismes segmentés (métamérisés) le long de l’axe antéro-postérieur (AP). Plusieurs segments sont rassemblés en tagmes : tête, thorax, abdomen. Il y a une forte régionalisation des segments ce qui est évident lorsqu’on observe les appendices spécifiques pour chacun d’entre eux (antennes, pièces buccales, pattes…). Cette régionalisation se met en place par une cascade de régulation d’expression génique qui démarre très tôt, dès l’ovogenèse.
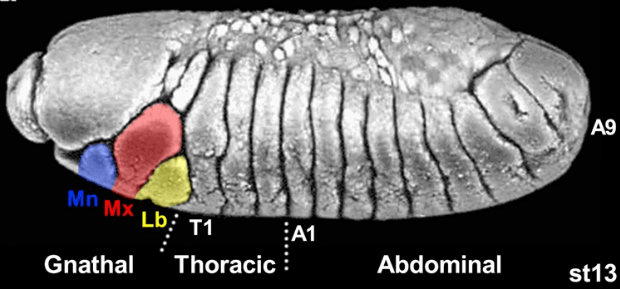
Au cours du développement précoce de la drosophile, les facteurs de transcription distribués en gradients dans l’unique cellule aux multiples noyaux servent de morphogènes pour contrôler la spécification du destin cellulaire en contrôlant l’activité des enhancers, des silencers et des promoteurs. Il existe aussi un contrôle de la traduction.
Signalons qu’au cours de l’embryogénèse, ce sont les parasegments et non directement les segments qui sont délimités. Un parasegment comprend la partie postérieure d’un segment n et la partie antérieure d’un segment n+1.
Bicoid et Nanos
Chez la drosophile, des gradients de protéines établis maternellement tels que celui du facteur de transcription et de traduction Bicoid (Bcd) et du régulateur de la traduction Nanos définissent les régions antérieures et postérieures, et activent une cascade complexe de régulation des gènes qui conduisent finalement à la segmentation et à la spécification régionale de l’axe antéro-postérieur (AP).
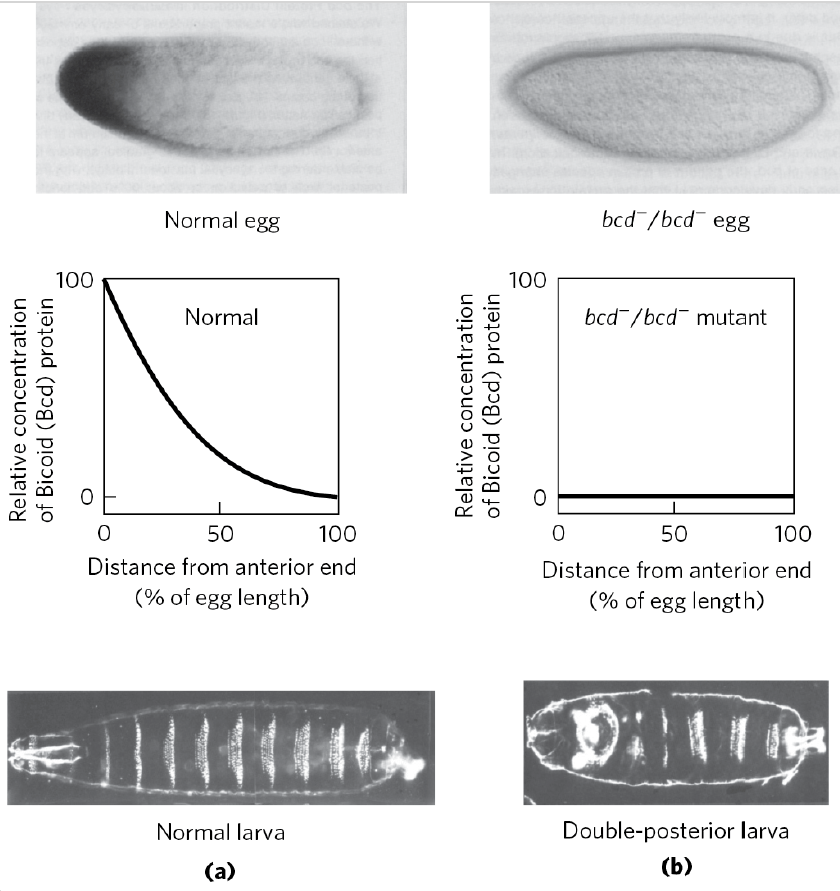
Les images du haut obtenus par immunohistochimie montrent la distribution de la protéine Bicoid (Bcd) dans un œuf normal (à gauche) et un œuf mutant bcd⁻/bcd⁻ (à droite). Les graphiques du milieu illustrent la concentration relative de Bicoid en fonction de la distance depuis l’extrémité antérieure (à droite). Dans l’œuf normal, un gradient antéro-postérieur de Bicoid est observé, tandis que l’œuf mutant ne présente aucune concentration détectable de cette protéine. En conséquence, les larves obtenues (en bas) diffèrent : la larve normale (a) présente une segmentation typique avec une tête, un thorax et un abdomen bien définis, tandis que la larve mutante (b) adopte un phénotype « double-région postérieure », dépourvu de structures céphaliques et antérieures, confirmant le rôle essentiel de bicoid dans la spécification de ces régions. Source : https://www.cell.com/cell/abstract/0092-8674(88)90183-3
Cependant, chez d’autres Arthropodes, comme les coléoptères, les millepattes et les araignées, ainsi que chez les Vertébrés, la segmentation AP est causée par un mécanisme d’oscillation semblable à une horloge dépendant de Hairy/Notch/Delta, qui est initié et contrôlé par un gradient de signalisation Wnt (et, dans le cas des vertébrés, également par la signalisation FGF) à l’extrémité postérieure (Chipman et Akam, 2008 ; El-Sherif et al., 2012 ; Gomez et al., 2009 ; Schönauer et al., 2016). Étonnamment, le régulateur du développement crucial Bicoid s’est avéré être une innovation évolutive au sein des Diptères (l’Ordre des Insectes auquel appartient la drosophile) résultant de la duplication et de la divergence de l’homologue du gène de la famille Hox zerknüllt (Stauber et al., 2002). Tout ce qui va suivre est donc spécifique aux Diptères et pas généralisable à l’ensemble des Insectes et encore moins à l’ensemble des animaux.
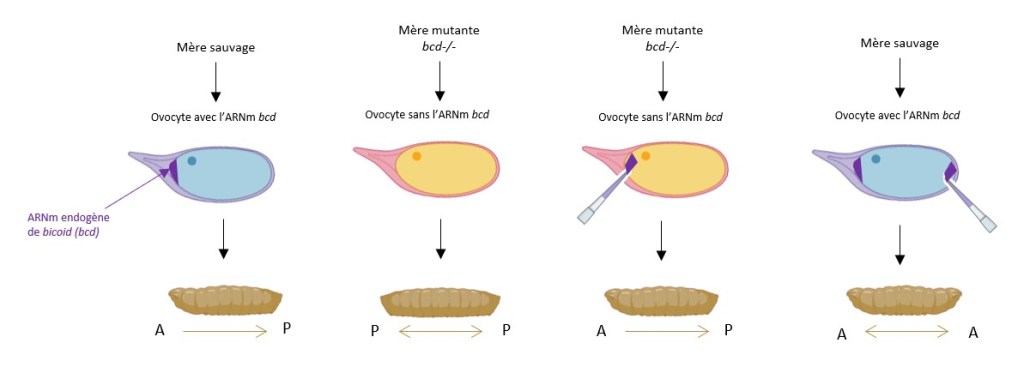
L’ARNm bicoid (bcd) exprimé par la mère contient des séquences de localisation dans son 3’UTR qui aboutissent à la concentration des transcrits au pôle antérieur de l’ovocyte puis des embryons de drosophile. Lors de la fécondation, la traduction de ces transcrits localisés aboutit à un gradient de protéine le long de l’axe AP (découvert par Driever et Nüsslein-Volhard en 1988). La synthèse dans le pôle antérieur est suivie de la diffusion, ainsi que du transport « de retour » vers le côté antérieur ou de la dégradation des protéines, ce qui affine la forme du gradient Bcd (Durrieu et al., 2018).
Une fois le gradient formé, la protéine Bcd, un facteur de transcription à homéodomaine, se lie à des motifs de séquence d’ADN spécifiques et active de manière différentielle les gènes le long de l’axe AP (Struhl et al., 1989).
Bcd peut affecter l’expression de gènes cibles, bien sûr dans les régions antérieures où il est le plus concentré mais aussi dans les régions postérieures, où le gradient est plus diffus, en formant des centres locaux dans les noyaux qui sont suffisamment concentrés pour rendre possible la liaison du Bcd aux enhancers (Mir et al., 2017). De plus, malgré le court laps de temps pendant lequel les molécules Bcd sont liées à l’ADN (Mir et al., 2018), cet apport se traduit par des régulations d’expression génique précises et rapides, à l’échelle de quelques minutes (Desponds et al., 2020).
Ensemble, ces mécanismes qui régulent la distribution de Bcd dans l’embryon et son interaction avec les enhancers cibles déterminent la capacité de ce morphogène à affecter différemment l’expression des gènes à travers l’axe AP.
L’un des gènes cibles de Bcd est hunchback. L’étude de l’enhancer proximal hb (hunchback), une région de 750 pb régulée par Bicoid a démontré qu’avec le promoteur associé, P2, il est suffisant pour récapituler correctement la dynamique spatio-temporelle d’établissement de l’expression de Hunchback (Lucas et al., 2018). Cependant, dans ce cas particulier, la modélisation mathématique a suggéré que les six sites de liaison Bcd présents dans cette séquence activatrice sont insuffisants pour soutenir dans le temps une expression qui est aussi précise que l’expression réelle du gène hb. Une régulation supplémentaire doit être à l’œuvre. Des sites supplémentaires cryptiques, notamment de faible affinité de liaison de Bcd et/ou d’autres facteurs de transcription distribués en gradients pourraient également contrôler le maintien de l’expression et la délimitation de la frontière de son domaine. Par exemple, la protéine Hb maternelle est également présente dans un gradient antéro-postérieur et soutient l’expression zygotique de hb en facilitant cette expression à un seuil de concentration de Bcd inférieur (Porcher et al., 2010). Bien que Bcd active plus de 40 gènes cibles pour initier la formation de l’axe AP d’une manière apparemment dépendante de la concentration, l’apport d’autres facteurs est nécessaire pour soutenir l’expression appropriée des gènes cibles (Briscoe et Small, 2015).
Bcd a également un rôle de répresseur de la traduction avec le même homéodomaine avec lequel il se fixe sur l’ADN et contrôle la transcription. Sa principale cible est l’ARNm de caudal qui est uniformément réparti dans le cytoplasme. L’homéodomaine de Bcd se fixe sur une séquence du 3’UTR de l’ARNm de caudal et empêche la fixation correcte du complexe d’initiation de la traduction. Cette fonction nécessite l’activité de Bin3, une ARN méthyltransférase qui méthyle l’ARN 7SK qui est impliqué dans le complexe répresseur de la traduction initié par Bcd (Singh et al., 2011). Ainsi, malgré la présence d’ARNm caudal uniforme dans l’embryon, y compris dans la partie antérieure, la protéine Caudal ne sera présente que dans la partie postérieure. Caudal est nécessaire à la formation de l’abdomen.
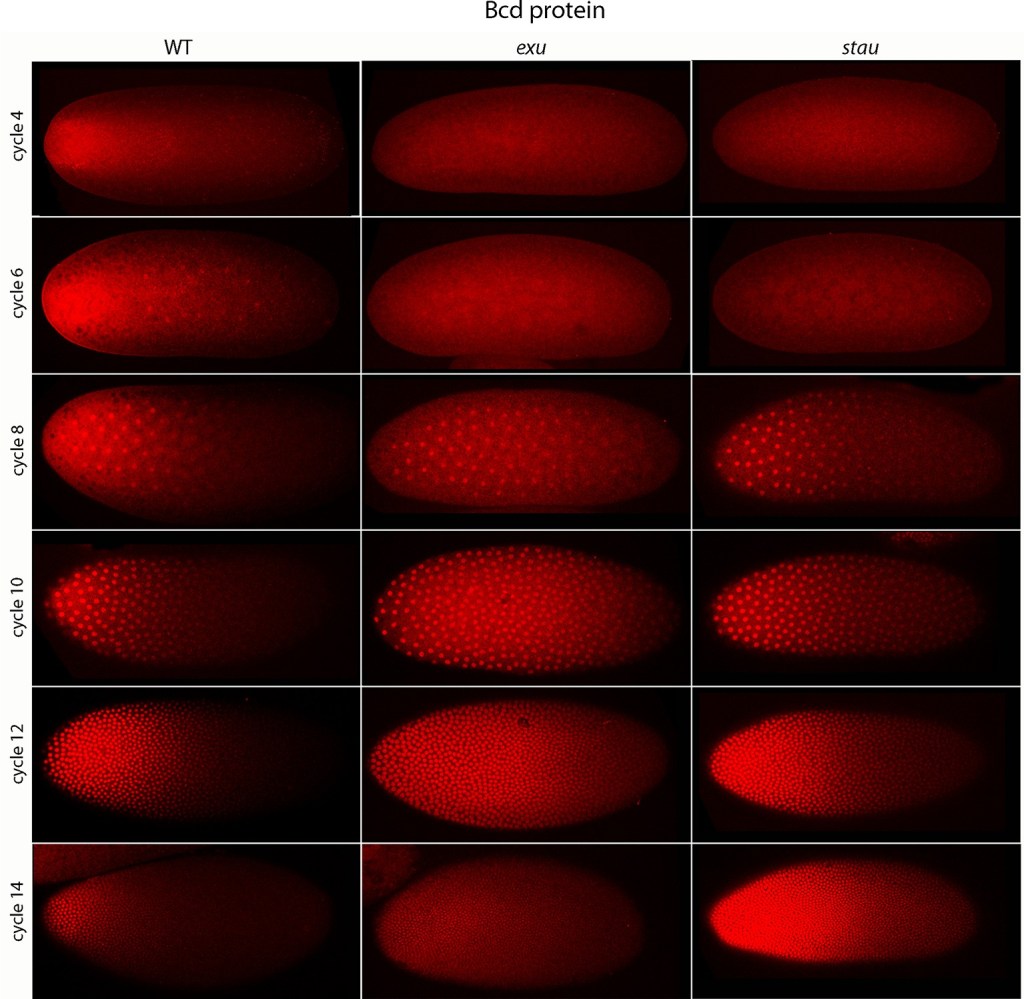
On l’a vu, la localisation antérieure de l’ARNm de bcd est fondamentale et elle dépend de la protéine Staufen. Chez le mutant perte de fonction staufen (stau), le gradient n’est pas visible comme on peut le constater sur l’une des figures précédentes (immunodétection en rouge de Bcd dans différents contextes mutants). L’ARNm de bcd est synthétisé dans les cellules nourricières qui appartiennent à la lignée germinale. Les ARNm passent entre cellules nourricières puis vers l’ovocyte grâce à des ponts cytoplasmiques. Les cellules nourricières se trouvent du côté du pôle antérieur de l’ovocyte, ainsi l’ARNm de bcd est spontanément localisé antérieurement dans un premier temps. Mais sans Staufen, les phénomènes de diffusion aboutissent à une uniformisation du gradient de l’ARNm de bcd.
La région 3’UTR de l’ARNm de bcd présente une séquence particulière qui provoque une structure secondaire remarquable de l’ARN. Cette structure avec des tiges et des boucles est reconnue par Staufen, lequel forme un complexe avec le moteur moléculaire dynéine. Dans l’ovocyte, le réseau de microtubules est orienté de telle manière que le pôle négatif des microtubules est orienté du côté du futur pôle antérieur de l’embryon. Ainsi, même si l’ARNm de bcd tend à diffuser postérieurement, il est sans arrêt ramené vers la région antérieure par la dynéine qui se déplace vers le pôle négatif des microtubules.
La segmentation postérieure est contrôlée par Nanos, qui est traduit à la fin de l’ovogenèse à partir du sous-ensemble d’ARNm nos synthétisé par la mère et localisé dans le pôle plasmique du cortex postérieur de l’ovocyte. La localisation postérieure de l’ARNm de nanos dépend d’Oskar qui est lui-même localisé à ce pôle postérieur où il a non seulement un rôle dans la mise en place de l’axe AP mais aussi dans la mise en place du plasme germinatif d’où émergeront les cellules germinales primordiales.
Le transport de l’ARNm osk dans l’ovocyte dépend de réseaux de microtubules polarisés dont les extrémités positives sont enrichies au pôle postérieur. Une fois localisé, l’ARNm osk produit 2 isoformes, Osk long et court, grâce à des utilisations alternatives de 2 codons d’initiation dans le même cadre de lecture. L’Osk long partage l’intégralité de la fraction Osk court, mais ils ont des fonctions distinctes. Osk court initie l’assemblage de plasme germinatif en recrutant des composants tels que Vasa (Vas), Tudor (Tud) et Aubergine (Aub), ainsi que des ARNm qui codent des facteurs impliqués dans l’établissement de cellules germinales. En revanche, le long Osk n’a pratiquement aucune activité pour recruter les composants du plasme germinatif mais est indispensable pour les ancrer au cortex de l’ovocyte. Dans les ovocytes dépourvus d’Osk long, les composants du plasme germinatif, y compris l’Osk court, rediffusent dans le cytoplasme de l’ovocyte. La défaillance de l’ancrage du plasme germinatif au cortex entraîne une réduction drastique du nombre de cellules polaires formées au pôle postérieur. Les 2 isoformes d’Osk diffèrent également par leurs distributions subcellulaires : l’Osk court est situé sur les granules polaires, des complexes ribonucléoprotéiques dans le plasme germinatif, tandis que l’Osk long est présent à la surface des endosomes.
Revenons à Nanos. C’est un répresseur qui régule la segmentation en bloquant la traduction de l’ARNm hunchback (hb) maternel (Cho et al., 2006). En plus de cette fonction au début du développement embryonnaire, Nanos joue de nombreux autres rôles dans l’organisme, notamment la régulation de plusieurs aspects du développement des cellules germinales primordiales, le maintien du destin des cellules souches dans le germe ovarien, la régulation du développement et de l’activité neuronale, et la protection des cellules contre la perte d’activité de la protéine du rétinoblastome (Rb). Des études sur des cellules de mammifères et des souris ont révélé que les fonctions de tampon Rb et de maintien des cellules germinales de Nanos sont conservées au cours de l’évolution.
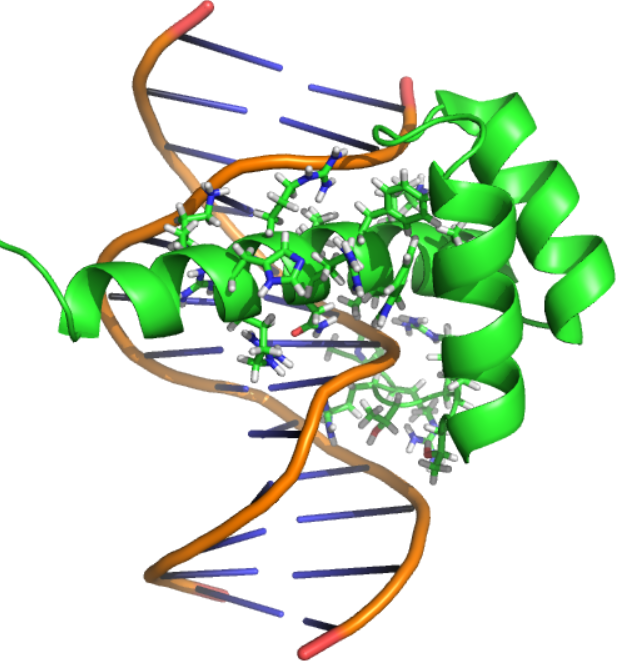
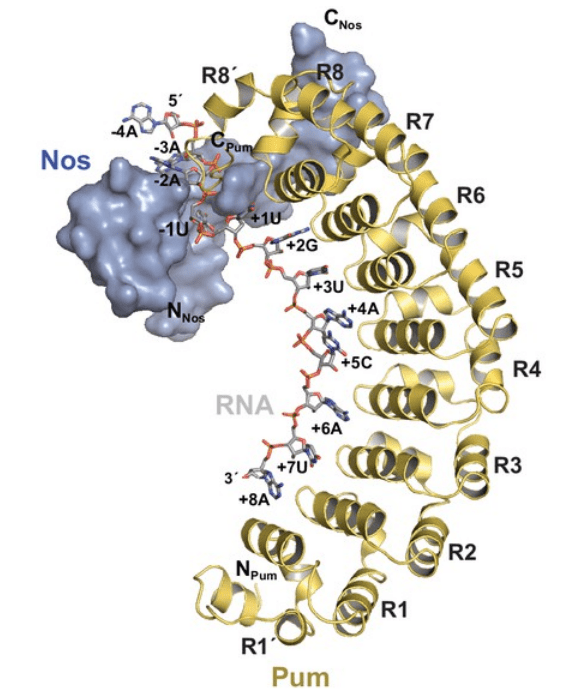
Nanos ne reconnaît pas seul les ARNm cibles ; des expériences sur trois cibles régulatrices de Nanos bien étudiées – hb, bcd et CycB – ont montré que Nanos se lie conjointement avec Pumilio (Pum) à des éléments de séquence conservés dans chaque 3′-UTR (appelé NRE pour Nanos Response Elements) (Marhabaie et al., 2024). Pumilio est une protéine de liaison à l’ARN de grande spécificité qui est uniformément distribuée dans l’embryon précoce. Pumilio reconnaît 8 nucléotides, un avec chacune des 8 répétitions qui constituent son domaine Puf de liaison à l’ARN. En revanche, Nanos n’a essentiellement aucune spécificité de liaison propre, mais peut être recruté spécifiquement pour les complexes Pumilio-ARN. Des études structurelles ont montré que la queue C-terminale de Nanos interagit avec le domaine Puf de liaison à l’ARN de Pumilio pour modifier sa conformation, permettant aux deux protéines de se lier de manière coopérative à des sites qui fonctionnent in vivo en tant qu’éléments régulateurs Nanos (NRE) (Weidmann et al., 2016).
Au cours du développement embryonnaire précoce, les régions activatrices doivent devenir exemptes de nucléosomes, afin d’être accessibles à la liaison des facteurs de transcription morphogènes. Ce processus est initié par une classe particulière de facteurs de transcription appelés facteurs pionniers. Un facteur pionnier peut se lier aux activateurs cibles dans la chromatine «fermée» ou inaccessible et faciliter les processus de remodelage de la chromatine, ce qui permet à d’autres facteurs de transcription de se lier ultérieurement aux activateurs pour contrôler l’activité du gène cible (Zaret et Carroll, 2011). Au stade précoce du blastoderme, Zelda (Zld) déposé par la mère agit comme un facteur pionnier crucial pour augmenter l’accessibilité de la chromatine en permettant le déplacement local des nucléosomes, l’effet dépendant du nombre et de la position des motifs Zld (Li et al., 2014; Schulz et al., 2015; Sun et al., 2015). En outre, Zld fonctionne comme un activateur global pour initier l’expression génique zygotique, notamment des gènes impliqués dans la mise en place de l’axe antéro-postérieur chez les embryons (Harrison et al., 2011; Nien et al., 2011).
Bcd devient inutile à la fin de la cycle nucléaire 14. À ce stade, les limites d’expression de nombreuses cibles, notamment hb, knirps (kni) et Krüppel (Kr), sont maintenues par la régulation croisée des gènes gap qui fonctionnent comme des répresseurs (Jaeger et al., 2004; Liu et al., 2013; Manu et al., 2009).
Un exemple de gène gap précoce : hunchback
Les gènes gap sont activés ou réprimés par les gènes à effet maternel,
et sont exprimés dans un ou deux domaines larges le long de l’axe antéro-postérieur.
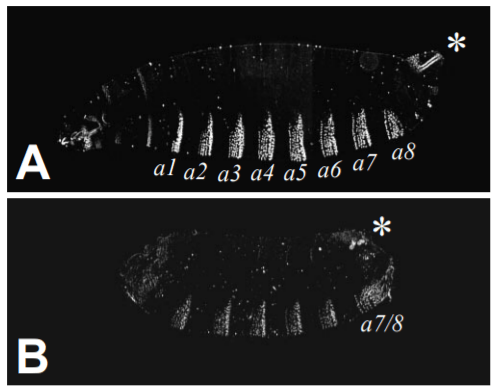
Le gène gap hunchback (hb) (pour bossu) est essentiel pour la régionalisation de l’axe antéro-postérieur lors de l’embryogenèse de la drosophile, principalement par l’établissement des limites d’expression génique d’autres gènes gap par répression transcriptionnelle. Les embryons présentant une perte complète de la fonction hb sont dépourvus de segments mandibulaire et thoracique, présentent une polarité inversée des deux ou trois premiers segments abdominaux et une fusion des septième et huitième segments abdominaux (Lehmann et Nusslein-Volhard, 1987; Margolis et al., 1995).
hb est exprimé maternellement et zygotiquement. L’ARNm hb exprimé maternellement est uniformément distribué dans l’embryon, mais sa traduction est réprimée dans la partie postérieure par Nanos avec l’aide de Pumilio, Brain Tumor et eIF4EHP (Cho et al., 2006; Sonoda et Wharton, 1999).
L’expression de l’hb zygotique est dynamique. hb est d’abord transcrit dans un large domaine antérieur dans des embryons du cycle nucléaire 11, en réponse au gradient de Bicoid (Driever et Nüsslein-Volhard, 1989). À partir du cycle nucléaire 14, les transcrits de hb s’accumulent dans une bande positionnée à la limite postérieure du domaine antérieur de l’expression de hb, à environ 50% de la longueur de l’embryon, ainsi que dans la région postérieure de l’embryon (Margolis et al., 1995). A ce moment, le large domaine antérieur de l’ARNm hb s’est désintégré de sorte que seules deux bandes plus faibles d’ARNm sont détectables dans la partie antérieure, en plus de la bande centrale nouvellement activée.
La distribution de la protéine Hb reflète celle du modèle d’ARNm zygotique décrit précédemment, sauf que la protéine persiste dans toute la moitié antérieure des embryons après le cycle nucléaire 14, probablement en raison d’une dégradation plus lente de la protéine que de l’ARNm (Perry et al., 2012; Wu et al., 2001). Le domaine Hb antérieur présente une frontière abrupte de la protéine Hb au centre de l’embryon.
Des gènes gap aux gènes homéotiques
D’autres gènes gap que hb interviennent dans la délimitation de larges régions le long de l’axe AP. Par exemple, Krüppel est exprimé dans les parasegments 4 à 6, au centre de l’embryon.
Une sensibilité plus importante des méthodes de détection a permis de montrer que l’activation de la transcription de certains gènes zygotiques étaient plus précoces que ce que l’on pensait et se déroule avant la transition mi-blastuléènne qui a lieu au cycle nucléaire 14. Le gène gap Krüppel fait partie des gènes dont la transcription démarre dès le cycle nucléaire 7 alors même que l’embryon n’est pas encore cellularisé (Ali-Murthy et al., 2016).
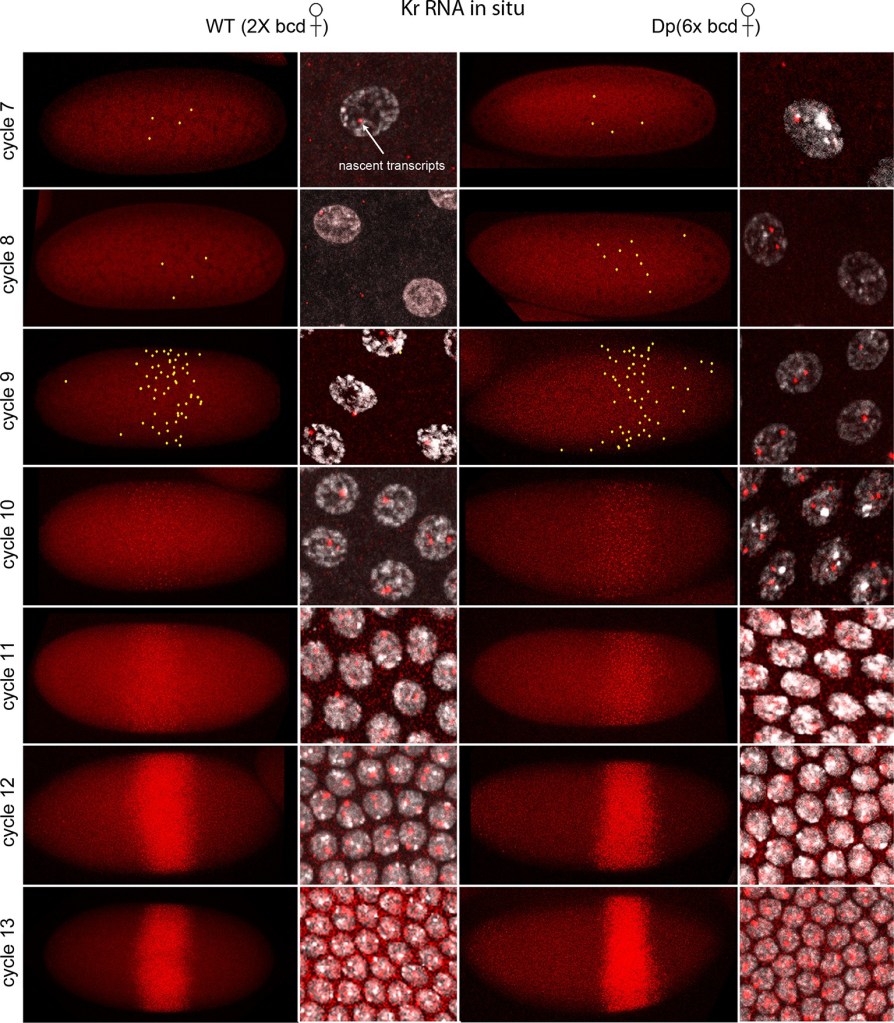
L’hybridation in situ a détecté l’ARN Kr (rouge) dans les embryons du cycle nucléaire 7-13 qui ont été produits par des femelles avec deux (deux colonnes à gauche) ou six (deux colonnes à droite) copies du gène bcd. Les embryons sont au stade de la prophase, le côté dorsal est en haut et le côté antérieur à gauche. Les images d’embryons sont des composites de projection à partir de coupes optiques en série au microscope confocal; les images à fort grossissement montrent des noyaux avec des points fluorescents rouges. Le nombre de noyaux avec des points rouges et l’intensité des points augmentent à chaque cycle successif. Deux points sont visibles dans la plupart des noyaux ; certains n’en ont qu’un mais aucun n’en a trois. Les points jaunes dans les embryons du cycle nucléaire 7-9 indiquent des points trop pâles pour être visibles à faible grossissement. La largeur de la bande des noyaux exprimant Kr était approximativement la même dans les deux génotypes ; sa position s’est déplacée « plus postérieurement » dans les embryons avec un excès de Bcd, ce qui est attendu (les embryons sont antériorisés donc l’expression de Kr est repoussée vers une position qui semble plus postérieure). Source : https://elifesciences.org/articles/13222
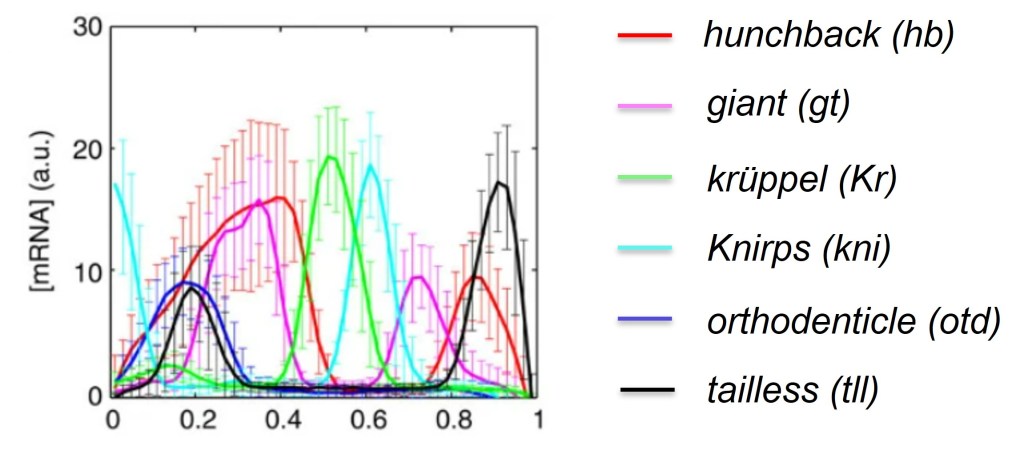
Des niveaux élevés de Bicoid et de Hunchback induisent l’expression de giant, tandis que la transcription de krüppel apparaît sur la région où Hunchback commence à baisser. Des niveaux élevés de Hunchback (en absence de Bicoid) empêchent également la transcription des gènes gap postérieurs (tels que knirps et giant) dans la partie antérieure de l’embryon (Struhl et al. 1992). Un gradient de la protéine Caudal, plus élevé au pôle postérieur, est responsable de l’activation des gènes gap abdominaux knirps et giant dans la partie postérieure de l’embryon. Le gène giant a donc deux modes d’activation (Rivera-Pomar 1995 ; Schulz et Tautz 1995) : une pour sa bande d’expression antérieure (via Bicoid et Hunchback) et une autre pour sa bande d’expression postérieure (par Caudal).
Une fois établis, les patrons d’expression des gènes gap sont maintenus par des régulations croisées entre eux : par exemple Giant et Krüppel inhibent mutuellement l’expression de leur gène. L’expression des différents gènes gap par ailleurs peut être partiellement chevauchante : par exemple, Krüppel et Hunchback sont exprimés ensemble sur une épaisseur de 8 noyaux environ le long de l’axe AP.
Une segmentation plus fine est mise en place grâce aux gènes pair-rule qui commencent à être exprimés au cycle nucléaire 13 alors que l’embryon se prépare à être cellularisé. Les gènes pair-rule sont exprimés dans un parasegment sur deux. Cela donne des patrons d’expression avec 7 bandes.

La distance entre les bandes est précisément déterminée par les différents gradients des gènes gap et même une modification du nombre de noyaux ne perturbe pas cet agencement (Day et Lawrence, 2000).
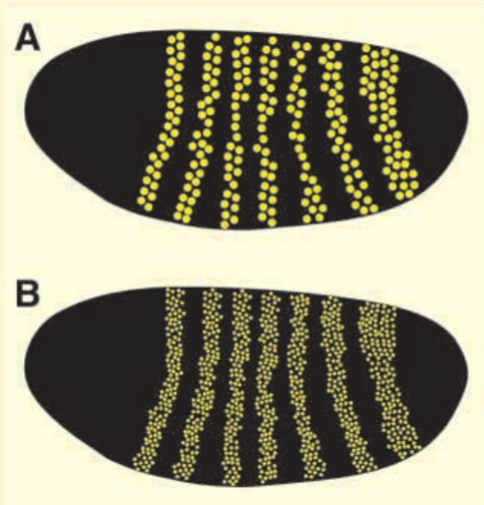
Les promoteurs et enhancers des gènes gap sont modulaires, c’est-à-dire qu’ils présentent des séquences discrètes qui contrôlent leur expression dans une ou deux bande.s en particulier. Quand on mute l’une de ces séquences régulatrices, une bande d’expression de gène pair-rule disparaît mais les autres restent normales. Ce sont des combinaisons de protéines codés par les gènes gap qui interviennent principalement pour activer (ou réprimer) l’expression des gènes pair-rule.
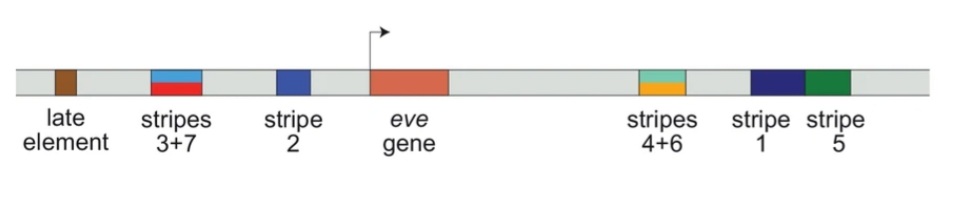
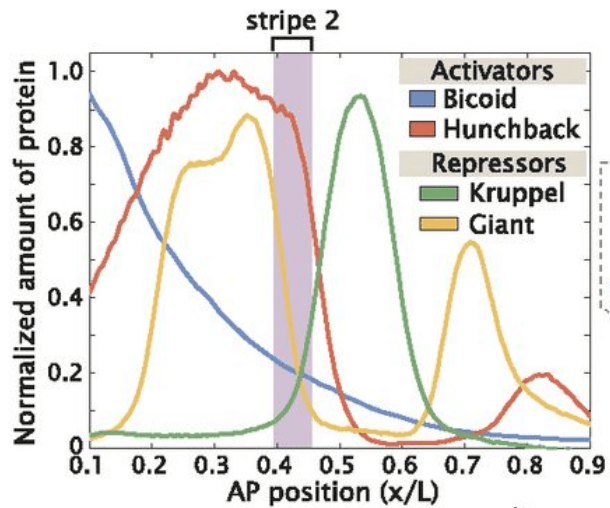
Une version commentée de cette figure est disponible en vidéo.
Source : https://www.pnas.org/doi/full/10.1073/pnas.1410022111
Une première génération de pair-rule active une seconde génération de pair-rule puis ce sont les gènes de polarité segmentaire qui sont activés. L’embryon est maintenant cellularisé et il n’est plus question pour les facteurs de transcription de passer d’un noyau à l’autre. Des signaux paracrines intercellulaires se mettent en place.
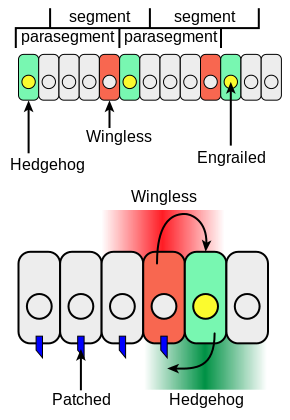
Les gènes de polarité segmentaire codent des protéines qui sont des constituants de la voie de signalisation Wnt (ou Wg = wingless chez la drosophile) et de la voie de signalisation Hedgehog (Ingham 2016). Des mutations dans ces gènes entraînent des défauts dans la segmentation générale et dans la polarité AP de chaque parasegment.
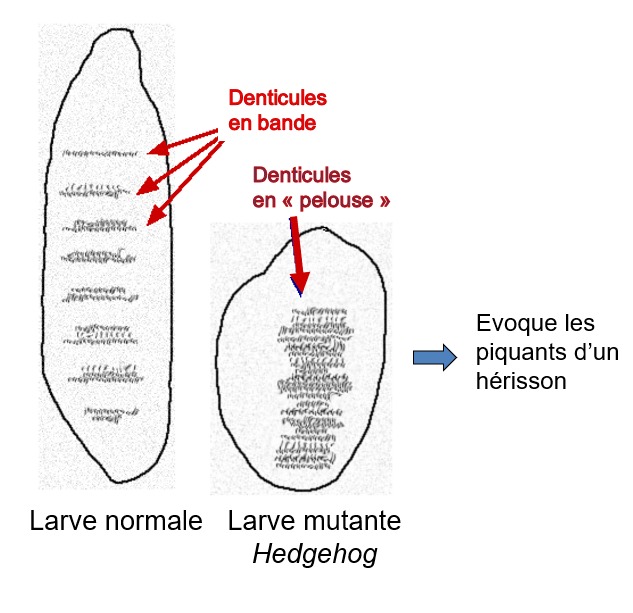
En temps normal, une seule rangée de cellules dans chaque parasegment exprime la protéine Hedgehog, et une seule rangée de cellules dans chaque parasegment exprime la protéine Wingless. Le gène engrailed est exprimé dans les cellules les plus antérieures de chacun des 14 parasegments ce qui correspond aux cellules juste postérieures par rapport à celles qui vont exprimer Wingless. Son expression est contrôlée par une combinaison activatrice et inhibitrice de protéines codées par les gènes pair-rule.

Les gènes homéotiques
Au cours de l’évolution des insectes, le dernier ancêtre commun de tous les insectes volants était à quatre ailes (une paire sur le 2ème segment thoracique + une paire sur le 3ème segment thoracique; le premier segment thoracique ne porte jamais d’ailes), comme en témoigne les archives fossiles. L’ordre des Diptères à deux ailes auquel appartient la drosophile apparait plus tard (Carroll et al., 1995). À la place de la 2ème paire d’ailes, les diptères présentent sur le 3ème segment thoracique une paire de structures rudimentaires appelées «haltères», qui sont des organes d’équilibration pendant le vol. Cette transformation évolutive d’aile en haltère est considérée comme un exemple d ‘«homéose» [vient du terme grec signifiant «remplacement»; terme inventé par William Bateson en 1894]. La découverte des mutants classiques du complexe bithorax (BX-C) par Calvin Bridges ont été les premiers exemples de transformation « homéotique » observés directement (Bridges, 1944). Dans le cas de la mutation perte-de-fonction ultrabithorax, les haltères sont transformés en ailes, et donc le 3ème segment thoracique devient une réplique du 2ème segment thoracique. On retrouve alors le plan d’organisation « classique » des insectes avec deux paires d’ailes.

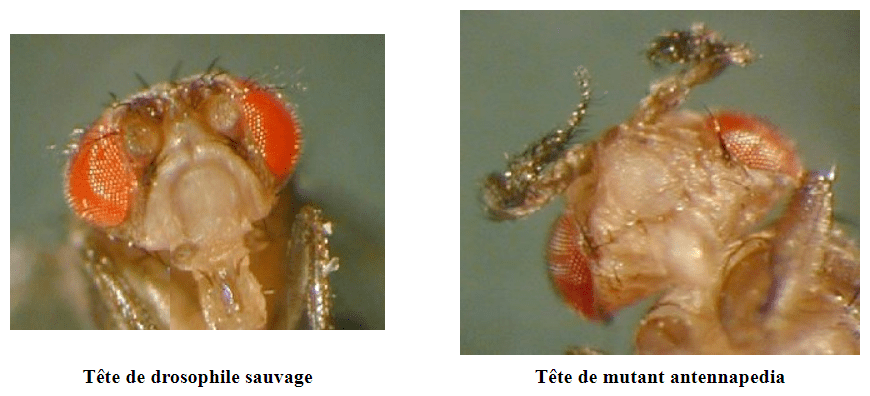
De même, des mutations homéotiques affectant la région antérieure ont été caractérisées telle la mutation Antennapedia (Antp) où des pattes se développent à la place des antennes.
Les gènes « homéotiques » impliqués dans ce type de transformation ont été caractérisés en détail par Ed Lewis (Lewis, 1963, 1978, 1998). Il se trouve que ces gènes codent des facteurs de transcription qui se fixent à l’ADN par un homéodomaine auquel ils ont donné leur nom. Mais il y a d’autres facteurs de transcription à homéodomaine qui n’appartiennent pas aux complexes des gènes Hox (par exemple la famille des Pax ou encore bicoid).
Chez la drosophile, les gènes Hox se trouvent positionnés dans deux complexes différents : le complexe ANT-C (qui fait 400 kilobases de long) et le complexe BX-C (qui fait 350 kilobases de long). Ils se trouvent sur 2 portions assez éloignées du chromosome 3 (mais ce n’est pas le cas général chez les insectes où ils sont le plus souvent contigus). Signalons que Bcd que nous avons vu agir très tôt au cours du développement précoce de la drosophile pour la mise en place de l’axe AP se trouve localisé dans le complexe ANT-C sans faire partie formellement dans ce que l’on appelle les gènes Hox.
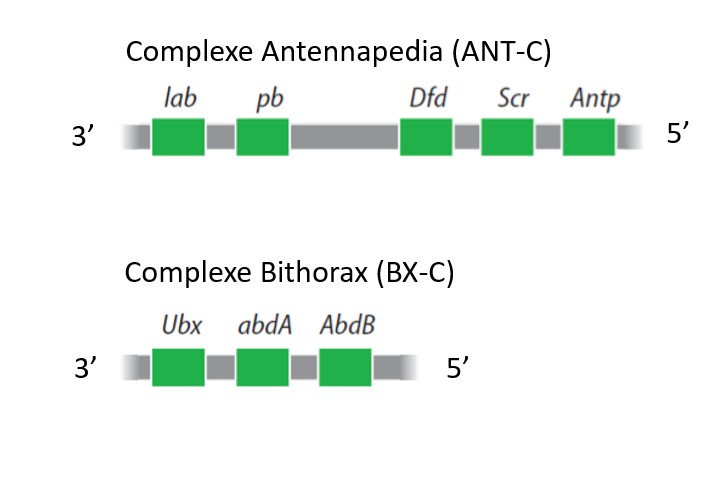
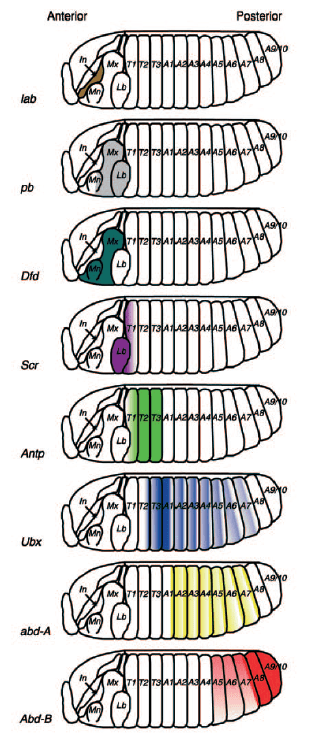
lab = labial palps; pb = proboscipedia; Dfd = Deformed; Scr = Sex combs reduced; Antp = Antennapedia; Ubx = Ultrabithorax; abdA = abdominal A; AbdB = Abdominal B.
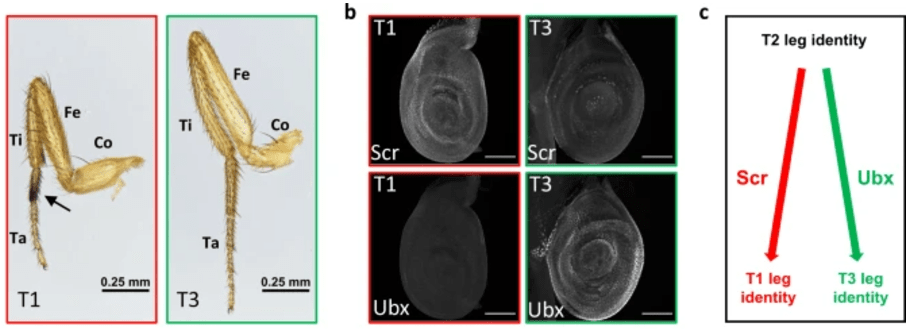
Le gène homéotique Scr (pour Sex combs reduced) a été appelé ainsi car l’un de ses allèles mutants aboutit à une réduction des « peignes sexuels » sur les pattes antérieures des mâles qui leur servent pour la parade nuptiale et la copulation. Il s’agit d’un allèle hypomorphe avec un phénotype peu marqué par rapport à une allèle perte-de-fonction total où c’est toute la partie postérieure de la tête et le premier segment thoracique portant la première paire de pattes qui sont profondément affectés.

La position des gènes Hox dans les complexes n’est pas anodine. Plus ils se trouvent en 3′, plus ils sont exprimés antérieurement (et précocement). C’est la règle de colinéarité.


Les séquences d’acides aminés des homéodomaines des différents gènes Hox (lab, pb, Dfd, Scr, Antp, Ubx, abd-A, abd-B) sont alignées afin de comparer leur similarité. Les acides aminés conservés sont indiqués par du jaune, montrant le haut degré de conservation entre les différentes protéines. Les acides aminés en vert et bleu sont partagés par plusieurs homéodomaines tandis que les acides aminés en orange sont spécifiques à un homéodomaine. En dessous, la séquence consensus est indiquée, représentant les acides aminés les plus fréquents à chaque position. Les trois hélices α caractéristiques de l’homéodomaine sont soulignées : elles constituent la structure tridimensionnelle responsable de la liaison à l’ADN. Source : https://www.academia.edu/22160235/From_DNA_to_Diversity_Molecular_Genetics_and_the_Evolution_of_Animal_Design_by_S_B_Carroll_J_K_Grenier_and_S_D_Weatherbee
Le mutant Antp avec les pattes à la place des antennes, s’est révélé être une mutation gain-de-fonction à cause d’une inversion dans le génome qui a mis le gène codant Antp sous l’influence d’un promoteur exprimé dans la tête. Cette expression ectopique (en dehors de sa région habituelle) a modifié l’information de position le long de l’axe AP et les cellules dans la tête qui devraient produire un appendice céphalique (les antennes) produisent à la place un appendice thoracique (les pattes).
Au sein du BX-C, Ultrabithorax (Ubx) est le gène homéotique clé orchestrant la transformation de l’aile en haltère. Les mutations perte-de-fonction dans Ubx modifient l’identité d’un segment entier, à savoir la transformation du 3ème segment thoracique (qui a normalement une paire d’haltères) en un 2ème segment thoracique dupliqué et donc avec une paire d’ailes. A l’inverse, l’expression de Ubx dans la future région de l’aile du 2ème segment thoracique aboutit à la transformer en haltère et on obtient une drosophile sans ailes et avec 2 paires d’haltères (Pavlopoulos et al., 2011).
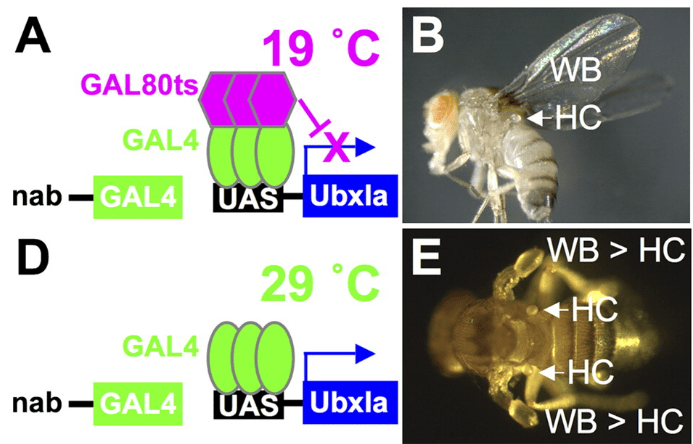
Ubx est fortement exprimé dans le troisième segment thoracique tout au long du développement, en commençant dans l’embryon lors de la subdivision de l’axe corporel AP, où il influence la structuration segmentaire des ceintures denticulaires cuticulaires de la larve (Crocker et al., 2015). Il existe également une expression d’Ubx dans les segments abdominaux, où il coopère avec deux autres facteurs de transcription du complexe BX-C abd-A et Abd-B pour modifier le motif de la ceinture denticulaire et réprimer la formation d’appendices dans l’abdomen (Castelli-Gair et al., 1995; Gebelein et al., 2002).
Pour voir une vision en 3D du patron d’expression d’Ubx (et également d’Engrailed, un gène de polarité segmentaire), voir ce lien.
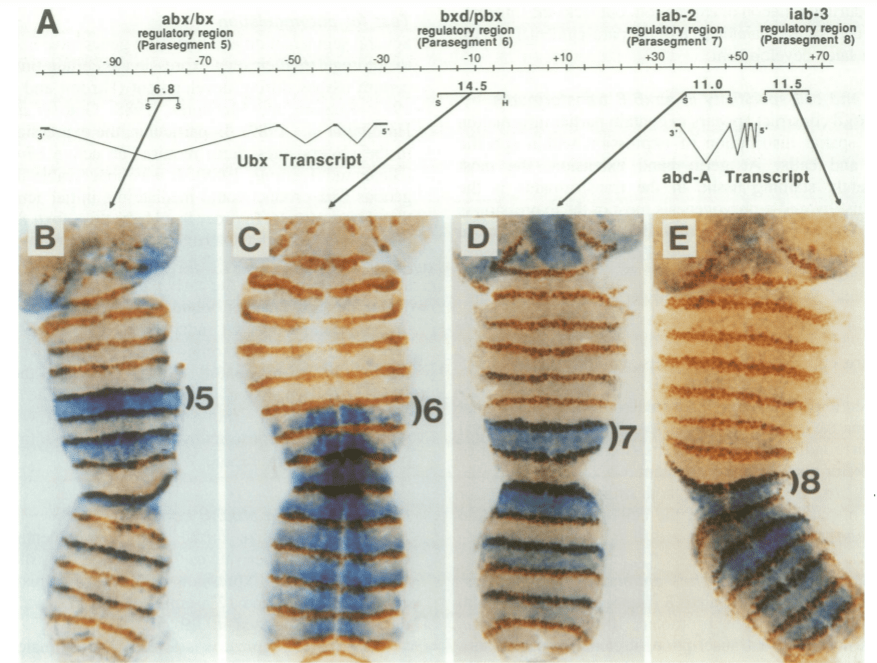
Dans le 3ème segment thoracique, l’expression d’Ubx conduit à la transformation de la 2ème paire d’ailes en balanciers, et a des effets plus subtils sur le développement des pattes, qui sont relativement similaires entre les segments à l’exception des différences de taille et des dispositions des soies (Davis et al., 2007; Rozowski et Akam, 2002).
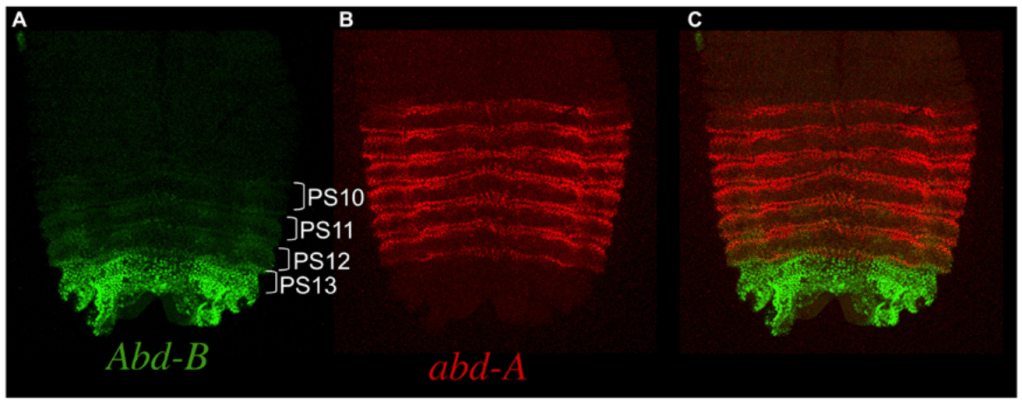
L’expression initiale d’Ubx est activée par le produit du gène pair-rule Fushi tarazu (d’ailleurs Ubx a très transitoirement un patron d’expression de gène pair-rule lui-même). Elle est réprimée par Hunchback. Une fois l’expression d’Ubx établie, sa frontière postérieure est maintenue par une répression d’abd-A. Ubx lui-même réprime Antp et maintient la frontière postérieure d’expression de celui-ci. Ainsi, on voit que de proche en proche les gènes du complexe contrôlent la frontière d’expression de leur voisin plus antérieur. C’est la règle de dominance postérieure. Cette règle de dominance postérieure doit être nuancée dans le cas de l’inhibition d’abdominal-A (abd-A) par Abdominal-B (Abd-B). Les animaux dépourvus d’Abd-B présentent une expression ectopique d’abd-A dans l’épiderme du 8ème segment abdominal, mais pas dans le système nerveux central. La répression dans ces cellules neuronales est accomplie non pas par Abd-B mais par un ARN non codant de 92 kb, transcrit à partir d’un locus situé entre ceux d’abd-A et d’Abd-B. Cet « ARN iab-8 » produit un microARN qui réprime la traduction d’abd-A, mais agit également par un deuxième mécanisme de répression redondant, sans doute une interférence transcriptionnelle avec le promoteur de abd-A.
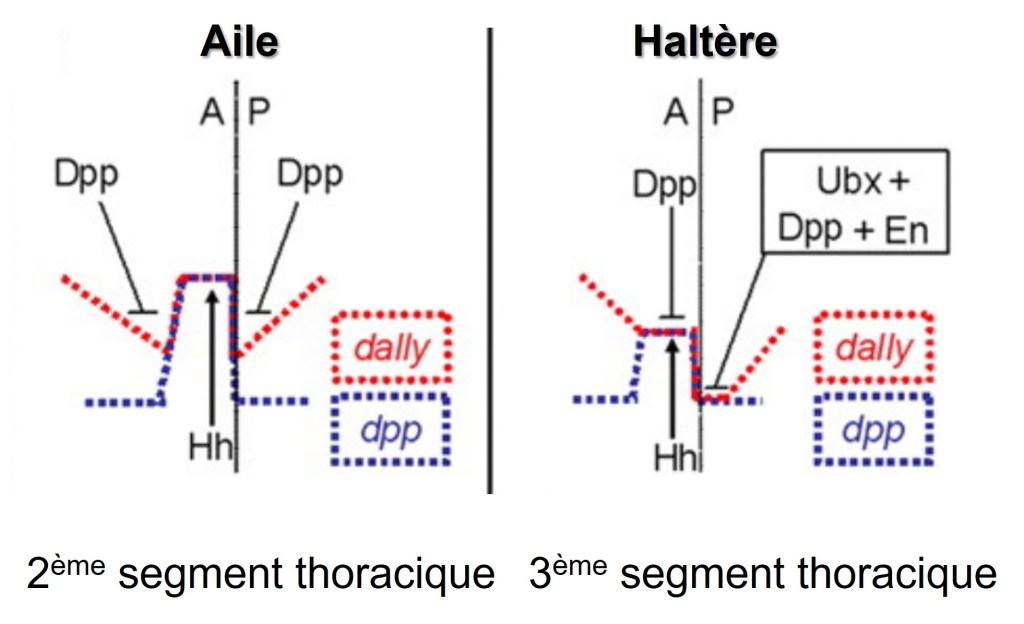
Comme le gène Ubx est exprimé dans des régions homologues à la fois chez la drosophile et les insectes à quatre ailes, tels que les papillons, c’est l’acquisition évolutive de nouveaux gènes cibles de Ubx qui est responsable de la perte de la deuxième paire d’ailes dans les diptères tels que la drosophile. Les recherches visant à identifier les gènes cibles de Ubx responsables de la transformation d’une aile en haltères ont montré qu’Ubx modifie notamment l’expression de dpp (l’orthologue des BMP chez la drosophile) qui est un morphogène important pour le développement des ailes (Agrawal et al., 2011; Crickmore et Mann, 2007; Makhijani et al., 2007; Pavlopoulos et Akam, 2011).
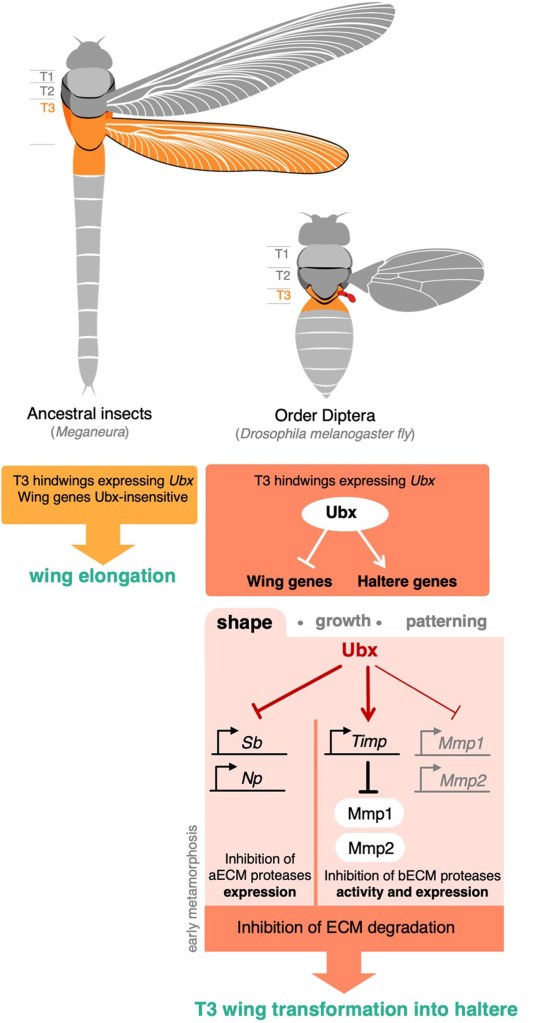
Le remodelage protéolytique de la matrice extracellulaire dans les disques imaginaux est crucial pour la morphogenèse de l’aile, et ce processus est réprimé par Ubx dans les haltères (Diaz-de-la-Loza et al., 2018). Ubx agit en réprimant directement l’expression de deux gènes codant pour des protéases dégradant l’ECM: Stubble (Sb) et Notopleural (Np) et en induisant l’expression d’un troisième gène codant pour Timp, un inhibiteur des protéases Mmp1/2 (Diaz-de-la-Loza et al., 2020).
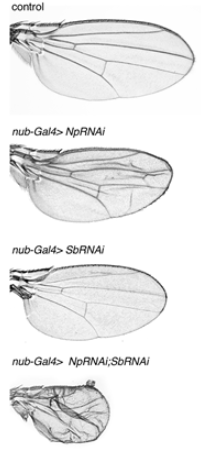
Signalons que dans le premier segment thoracique des insectes, l’absence d’ailes n’est pas due à Ubx (qui n’y est pas exprimé) mais à l’action d’une autre protéine codée par le complexe homéotique Scr (Sex combs reduced) qui inhibe l’expression de Nubbin qui est nécessaire à la production des ailes (Prud’homme et al., 2011).
Les protéines des complexes Hox contiennent un homéodomaine (HD) qui permet la reconnaissance de l’ADN, déterminant la spécificité tissulaire en régulant l’expression des gènes cibles. Mais, à l’exception d’Abd-B qui possède l’un des homéodomaines les plus divergents et une préférence pour les séquences TTAT ou TTAG, toutes les protéines Hox se lient à la même séquence centrale TAAT. Étant donné que les HD sont ainsi hautement conservés avec des propriétés de liaison à l’ADN qui se ressemblent, il n’est pas clair comment les protéines Hox instruisent la morphogenèse différentielle, ce qui constitue le « paradoxe de la spécificité des Hox ». La solution à ce paradoxe vient probablement du fait que les protéines Hox se lient à l’ADN en association avec des cofacteurs supplémentaires et peuvent également interagir avec des facteurs de régulation transcriptionnelle (notamment Extradenticle (Exd) et Homothorax (Hth)), des ARN non codants et des complexes de remodelage de la chromatine variés. Tout cela amène à la notion d’interactome Hox avec une multiplicité d’interactions. Les interactions avec Exd et Hth sont particulièrement importantes car elles étendent la séquence cible des HD sur l’ADN à 12 paires de bases et permet de révéler une spécificité de chaque protéine Hox pour des séquences particulières (Slattery et al., 2011).
Dans ces interactions, la relation entre les protéines Hox et la machinerie de transcription générale est très importante pour la régulation transcriptionnelle. La première preuve d’une protéine Hox établissant un contact fonctionnel avec un facteur de transcription général est l’interaction entre le motif YPWM d’Antennapedia (Antp) et BIP2 (TAF3), un composant associé à la protéine de liaison à la boîte TATA de TFIID. De plus, la sous-unité Med19 du complexe MED, le composant majeur de la machinerie de l’ARN polymérase II, interagit avec Proboscipedia (Pb), Deformed (Dfd), Antp, Ultrabithorax (Ubx), Abdominal A (AbdA) et Abdominal B (AbdB). Les protéines Hox sont également impliquées dans les mécanismes de pause de l’ARN polymérase II, interagissant avec le facteur de pause de transcription M1BP, modifiant l’état de la chromatine et améliorant l’efficacité de la transcription. Un criblage d’interactome Hox de 35 facteurs de transcription a révélé que TFIIEβ interagit avec Scr, Antp, Ubx, AbdA et AbdB dans l’embryon de drosophile. Une interaction physique directe de TFIIEβ avec deux positions d’acides aminés de l’hélice 2 de l’homéodomaine de Antp est nécessaire pour la fonction d’Antp.
Ubx agit essentiellement en tant que facteur de transcription grâce à son homéodomaine, mais il est impliqué également dans l’épissage alternatif : il se déplace au cours de la transcription en complexe avec l’ARN polymérase II et il est aussi capable d’interagir directement avec des ARN. Il contribue à recruter différents éléments du spliceosome en cours de transcription (Carnesecchi et al., 2021).
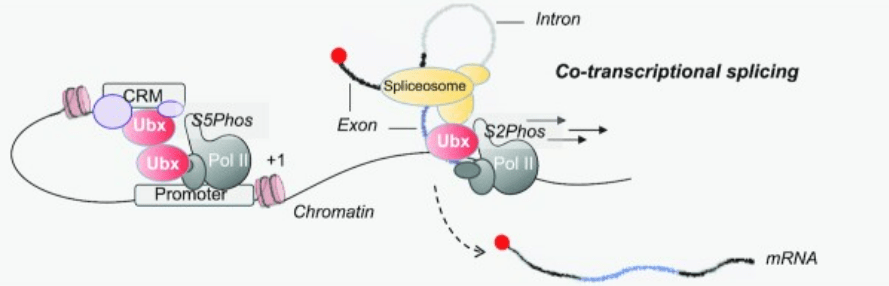
Une fois activée, l’expression (ou la non-expression) des gènes du complexe Hox doit être maintenue alors que les facteurs de transcription qui ont induit (ou inhibé) leur expression ne sont plus exprimés. Ce contrôle se fait par des modifications épigénétiques stables. Les protéines d’identité cellulaire appartenant aux groupes « Polycomb » (PcG) et « Trithorax » sont des familles qui ont été découvertes chez la drosophile et qui sont capables de remodeler la structure de la chromatine et de moduler ainsi l’expression des gènes du développement. Ces protéines s’associent à l’ADN ainsi qu’à des facteurs de transcription responsables de la régulation des gènes du développement. Polycomb et Trithorax ont des rôles antagonistes : les protéines Polycomb maintiennent les gènes homéotiques Hox « éteints », alors que les protéines Trithorax les maintiennent actifs.

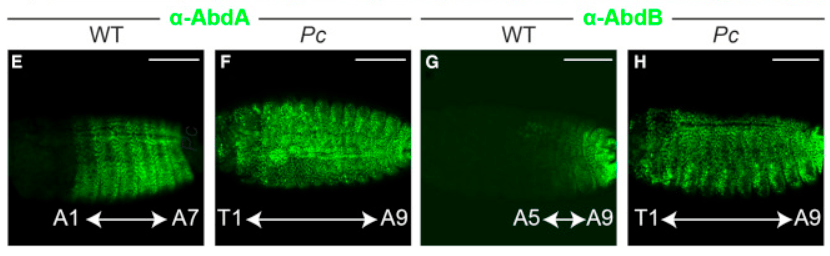
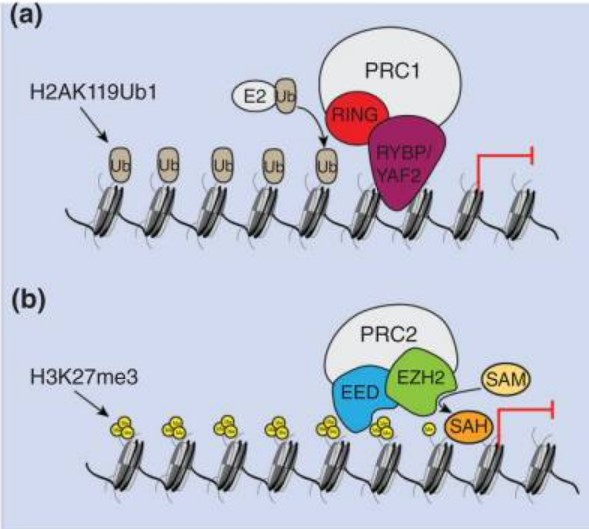
C’est un équilibre variable entre ces deux états qui détermine l’identité et la place de la cellule dans l’organe et l’organisme. Le premier complexe PcG identifié, nommé Polycomb Repression Complex 1 (PRC1), agit comme une histone H2A ubiquitine E3 ligase et est également capable de modifier l’architecture de la chromatine par compactage local et interactions à longue distance. PRC1 peut également inhiber directement la transcription et déstabiliser les complexes de pré-initiation de la transcription (par inhibition de l’association de l’ARN polymérase II phosphorylée sur la Ser5 avec les sites d’initiation de la transcription). PRC2, un autre complexe protéique PcG, méthyle l’histone H3 sur la lysine 27 (H3K27me), une activité essentielle à la fonction PcG (Poynter et Kadoch, 2016). Le complexe PcG est capable de s’associer à des séquences cibles qui peuvent aller jusqu’à 1500 pb : des PRE (Polycomb Response Elements) (Chan et al., 1994; Zink et Paro, 1995).
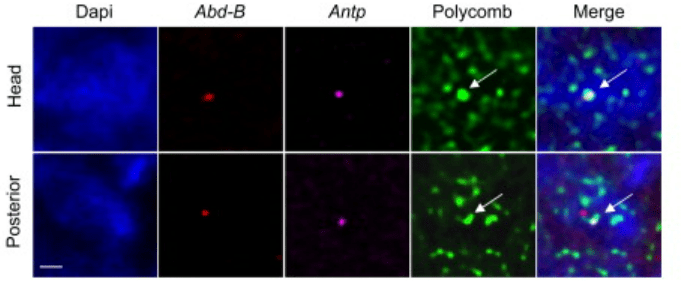
Les complexes Trithorax comprennent une histone méthyl transférase qui triméthyle l’histone H3 lysine 4, une modification épigénétique associée
avec les promoteurs de gènes activement transcrits. Ils comprennent également Brahma qui appartient à la famille de protéines SWI/SNF qui remodèlent la chromatine de manière ATP-dépendante (Tamkun et al, 1992). Ces protéines sont capables de se lier à la fois aux histones des nucléosomes et à l’ADN et de faire glisser les nucléosomes le long de l’ADN permettant de rendre accessible des séquences importantes pour des facteurs de transcription.
Précisons que les protéines Polycomb et Trithorax ont des cibles bien plus larges que juste les gènes du complexe HOM-C.
Pour comparer avec la régionalisation de l’axe AP des Vertébrés et notamment comprendre le rôle des gènes Hox dans ce processus, vous pouvez lire cette partie de chapitre.
COURS EN VIDEO : Par Mike Levine (Université de Berkeley). Ce cours est en anglais mais vous pouvez activer les sous-titres et la traduction simultanée en français.
Par Denis Deboule (Collège de France). Toute une partie de ce cours (à partir de la 20ème minute environ), concerne les gènes Hox.
QUIZZ
Q1. Quel est l’effet d’une mutation perte-de-fonction du gène à effet maternel bicoid sur le développement de la larve de drosophile ?
A) L’embryon développe une structure en miroir avec 2 régions postérieures sans tête ni thorax
B) L’embryon développe une structure en miroir avec 2 régions antérieures sans abdomen ni thorax
C) L’embryon ne présente plus de tête
D) L’embryon de présente plus d’abdomen
Q2. Comment la protéine Caudal est-elle distribuée dans l’embryon, sachant que son ARNm est réparti uniformément ?
A) La protéine est transportée dans la région postérieure
B) L’ARNm n’est traduit que dans la région postérieure
C) La protéine est dégradée dans la région antérieure
Q3. Quelle est la principale caractéristique des gènes de polarité segmentaire par rapport aux étapes précédentes de la cascade génétique ?
A) Leur expression est contrôlée par des signaux paracrines
B) Ils sont exprimés dans un parasegment sur deux
C) Ils forment un complexe génétique où leur position contrôle leur expression dans l’embryon.
Q4. Dans le cas d’une mutation perte-de-fonction du gène Ultrabithorax (Ubx), quel phénotype observe-t-on chez la drosophile ?
A) Les ailes du 2ème segment thoracique sont transformées en haltères
B) Les ailes du 3ème segment thoracique sont transformées en halères
C) Les haltères du 2ème segment thoracique sont transformés en ailes
D) Les haltères du 3ème segment thoracique sont transformés en ailes
Q5. Expliquez la différence entre les règles de colinéarité et de dominance postérieure pour les gènes Hox
Réponses : Q1. C; Q2. B; Q3. A; Q4. D; Q5. Dans le cadre du développement de la drosophile, les gènes homéotiques (Hox), qui spécifient l’identité des segments le long de l’axe antéro-postérieur, suivent deux principes fondamentaux mais distincts : la colinéarité et la dominance postérieure. La colinéarité établit une correspondance directe entre le positionnement des gènes sur le chromosome et le déploiement de leur expression dans l’espace et le temps au sein de l’embryon (Colinéarité spatiale : Plus un gène Hox se trouve en position 3′ dans le complexe génétique, plus sa limite d’expression est antérieure dans l’embryon. À l’inverse, les gènes situés en 5′ sont exprimés dans les régions les plus postérieures. Par exemple, dans le complexe BX-C, le gène Abdominal-B (Abd-B) est situé plus en 5′ que abdominal-A (abd-A), et son expression est effectivement plus postérieure. Colinéarité temporelle : Les gènes situés en 3′ sont généralement activés plus précocement que ceux situés en 5′.) La dominance postérieure (parfois appelée prévalence postérieure) décrit la relation hiérarchique et fonctionnelle entre ces gènes lorsqu’ils sont présents dans une même cellule. Selon cette règle, les gènes Hox exprimés dans les régions postérieures ont la capacité de réprimer l’expression ou l’activité des gènes Hox normalement exprimés plus antérieurement. Le gène Ubx (postérieur par rapport à Antp) réprime Antp et maintient ainsi sa frontière d’expression postérieure. Cette règle assure que chaque segment acquiert l’identité la plus postérieure possible parmi les gènes Hox qui y sont activés. Si un gène postérieur est absent (mutation perte-de-fonction), le gène antérieur qu’il réprimait habituellement prend le relais, provoquant une transformation homéotique (comme le 3ème segment thoracique se transformant en 2ème segment dans le cas d’une mutation Ubx).
- Adhérences cellule-cellule
- Arabidopsis thaliana
- Biomécanique du développement
- Caenorhabditis elegans
- Concepts principaux
- Contrôle de la traduction
- Contrôle de la transcription
- Contrôle génétique et épigénétique
- Croissance du tube pollinique et double fécondation chez les Angiospermes
- Croissance et guidage axonal
- Des modèles animaux moins classiques
- Développement de l’oeil des Vertébrés
- Développement et évolution
- Et l’Humain ?
- Exercices sur l’ovogenèse, la spermatogenèse et la fécondation
- Exercices sur le contrôle de l’expression des gènes
- Exercices sur le développement des bourgeons de membre
- Exercices sur le développement des muscles striés squelettiques
- Exercices sur le développement des végétaux et les hormones végétales
- Exercices sur les cycles et les divisions cellulaires
- Exercices sur les étapes du développement, les inductions embryonnaires et la mise en place des axes de polarité
- Exercices sur les matrices extracellulaires, le cytosquelette et les adhérences cellule-cellule
- Exercices sur les voies de signalisation
- Glossaire
- Glossaire des termes liés à la génétique
- Glossaire des termes liés au cytosquelette, la matrice extracellulaire, l’adhérence et la migration cellulaire
- Hématopoïèse et développement des cellules du système immunitaire
- Histoire de la biologie cellulaire et de la biologie du développement
- L’acide rétinoïque
- L’apoptose
- L’autophagie
- L’organogenèse
- L’ovogénèse prépare le développement embryonnaire
- La drosophile
- La fécondation
- La formation des somites
- La gastrulation
- La gastrulation (version allégée)
- La métamorphose chez les Hexapodes et les Amphibiens
- La neurogénèse chez les mammifères adultes
- La neurulation
- La poule
- La signalisation calcique
- La souris
- La superfamille TGFβ et ses voies de signalisation
- La voie de signalisation de l’auxine et ses rôles
- La voie de signalisation Hedgehog
- La voie de signalisation Hippo et ses composants YAP/TAZ
- La voie de signalisation Notch
- Le clivage
- Le cytosquelette
- Le destin des cellules et les réseaux de régulation génique
- Le développement des bourgeons de membre
- Le développement des muscles striés squelettiques
- Le développement des organes génitaux et des cellules germinales
- Le développement du cortex
- Le méristème apical caulinaire en phase végétative et lors de la formation d’une fleur
- Le poisson zèbre
- Le xénope
- Les cellules des crêtes neurales
- Les cellules et les gènes en action dans le développement
- Les cellules souches
- Les cellules tumorales
- Les cycles et les divisions cellulaires
- Les étapes du développement
- Les étapes du développement embryonnaire d’Arabidopsis thaliana et leur contrôle
- Les inductions embryonnaires et les gradients de morphogène
- Les matrices extracellulaires animales
- Les organismes modèles
- Les outils pour étudier l’expression et la fonction des gènes
- Les parois des cellules végétales
- Les techniques et les outils pour la biologie cellulaire
- Les transitions épithélio-mésenchymateuses et les migrations cellulaires
- Les vésicules extracellulaires
- Les voies de signalisation
- Les voies de signalisation FGF
- Mise en place des axes chez les Vertébrés
- Structures et processus cellulaires
- Voies de signalisation WNT
