Par Patrick Pla, Université Paris-Saclay
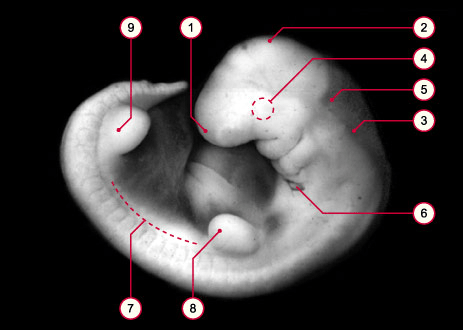
Les bourgeons de membre chiridien se développent à partir d’expansions latérales du corps. Ils apparaissent entre la 4ème et la 5ème semaine de développement chez l’embryon humain. Ils donnent les os, les tendons et l’épiderme du membre, mais d’autres cellules migrent dans le bourgeon et participent à son organogenèse.
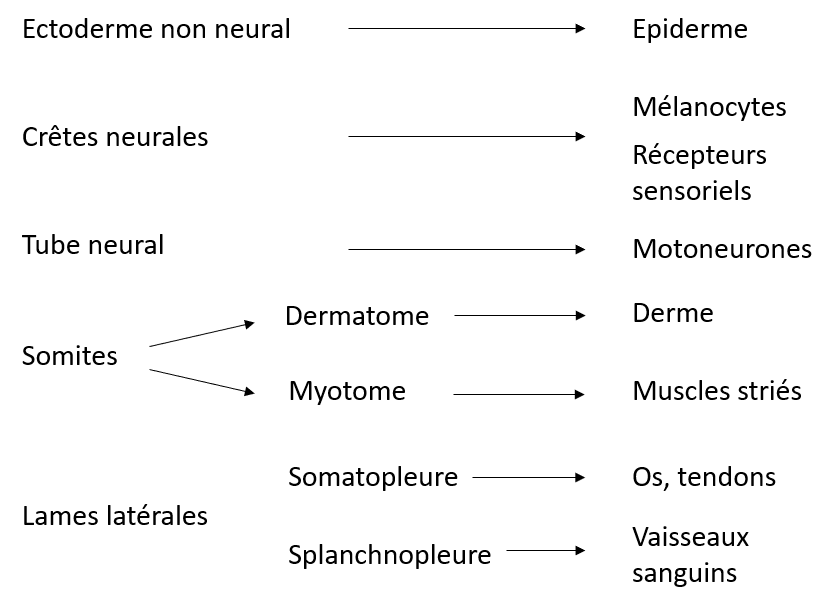
Ce sont donc des cellules de différentes origines qui vont devoir former une structure fonctionnelle et correctement régionalisée selon plusieurs axes :
● l’axe proximo-distal (la succession stylopode-zeugopode-autopode)
● l’axe antéro-postérieur (visible sur les doigts : le pouce est le doigt le plus antérieur, le petit doigt est le plus postérieur)
● l’axe dorso-ventral (bien visible en regardant la différence entre le dos et la paume de la main).
Etudier le développement du bourgeon de membre peut permettre une approche plus simple que pour un embryon entier pour comprendre comment une structure tridimensionnelle se met en place.
- Contrôle de la position des bourgeons de membre sur l’axe antéro-postérieur de l’animal
- L’axe proximo-distal et son contrôle
- L’axe antéro-postérieur et son contrôle
- Polarité dorso-ventrale du bourgeon de membre
- Contrôle de l’apoptose interdigitale
- La régénération des bourgeons de membre
- Aspects Evo/Dévo
Contrôle de la position des bourgeons de membre sur l’axe antéro-postérieur de l’animal
Des expériences classiques ont montré que la mise en place d’une barrière imperméable entre les somites et les lames latérales à un moment critique abolit la spécification des cellules des lames latérales en cellules du bourgeon de membre. Le signal inducteur en provenance des somites a été identifié comme étant l’acide rétinoïque (RA). Le bourgeon de membre antérieur se forme justement dans une zone où l’acide rétinoïque a une activité importante. La mutation de gène codant la rétinaldehyde déshydrogénase-2 (Raldh2), l’enzyme clé de la synthèse de RA, abolit la formation des nageoires pectorales et des bourgeons de membre antérieurs chez le poisson-zèbre et la souris (Begemann et al., 2001, Niederreither et al., 1999). L’acide rétinoïque produit par les somites s’oppose notamment à l’action du FGF8 qui est exprimé dans le cœur et dans les régions plus postérieures et il induit l’épaississement localisé de la lame latérale externe (la somatopleure) qui est la première étape de la formation du bourgeon de membre.

L’induction du développement du bourgeon de membre est réalisée par l’acide rétinoïque mais aussi par Wnt2b qui est exprimé dans les somites et dans la partie médiale des lames latérales (Ng et al., 2002). L’acide rétinoïque et Wnt2b induisent l’expression de Tbx5 qui active ensuite directement l’expression de FGF10 dans le mésenchyme (Agarwal et al., 2003). Dans le bourgeon de membre postérieur, c’est Tbx4 qui joue le rôle de Tbx5.
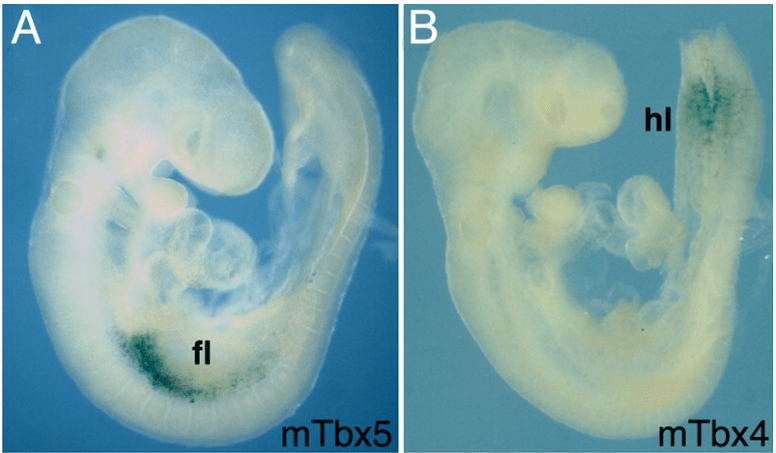
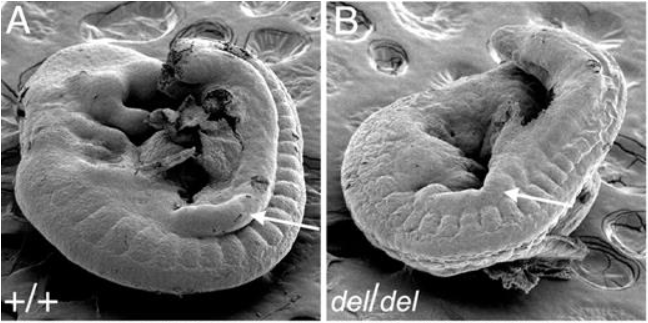
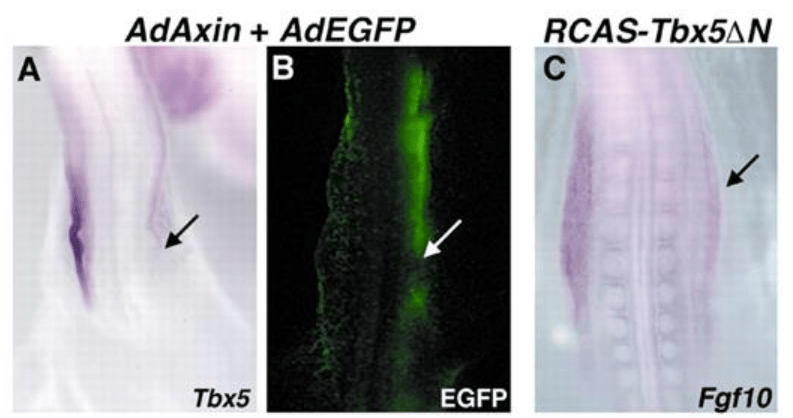
FGF10 active FGF8 dans l’ectoderme qui s’épaissit et forme l’AER (pour Apical Ectodermal Ridge ou crête apicale ectodermique).

C’est ensuite la boucle de régulation positive entre FGF10 mésenchymateux et FGF8 de l’épiderme qui pousse à la croissance du bourgeon. On remarque que d’un signal inhibiteur initial, FGF8 devient un signal activateur, un exemple de plus démontrant qu’une molécule de signalisation ne porte pas d’instructions en soi et que tout dépend du contexte.
Le thalidomide, un médicament qui a été largement prescrit comme anti-nauséeux et sédatif dans les années 1950 et 1960 avant d’être interdit aux femmes enceintes, cause des raccourcissements et des malformations des membres au cours du développement, en inhibant notamment l’expression de FGF10 et de FGF8 (Ito et al., 2010).

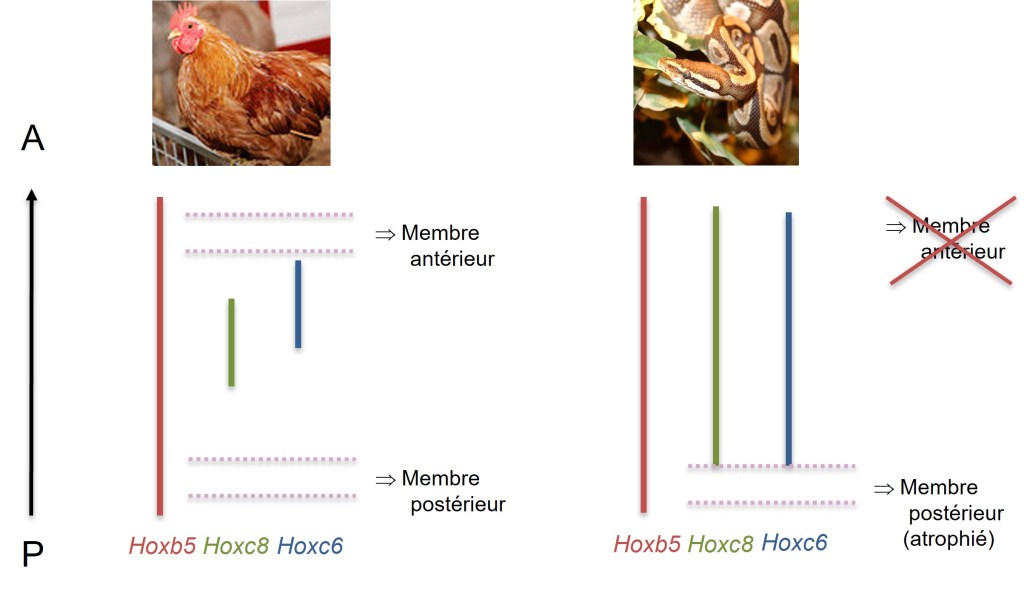
Les gènes Hox ont bien entendu leur mot à dire sur le positionnement des bourgeons de membre le long de l’axe AP. Par exemple, les bourgeons de membres antérieurs ne sont induits que dans une région qui exprime Hoxb5 mais pas Hoxc6 et Hoxc8. C’est par modification de l’expression de ces deux derniers gènes que les serpents ont perdu leur capacité à former des membres antérieurs. L’expression de Hoxc6 et Hoxc8 remonte bien plus antérieurement chez l’embryon du python comparé à l’embryon de poulet et la région où le bourgeon de membre antérieur pourrait se former n’existe plus d’un point de vue de la détermination génétique.
L’axe proximo-distal et son contrôle
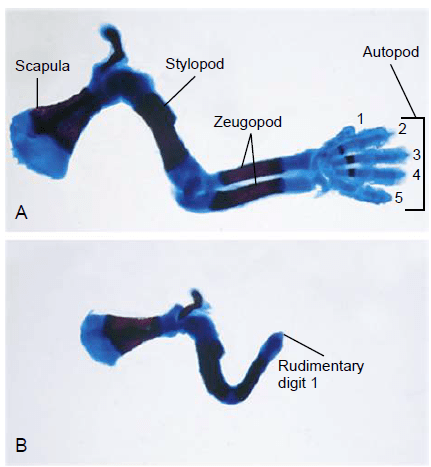
Le plan d’organisation du membre chiridien des tétrapodes se compose de trois segments principaux séparés par des articulations. Selon l’axe proximo-distal, depuis la paroi corporelle jusqu’à la pointe distale, il s’agit du stylopode (bras, cuisse), du zeugopode (avant-bras, mollet) et de l’autopode (main, pied). Le stylopode et le zeugopode contiennent respectivement un et deux éléments squelettiques, tandis que le segment distal ou autopode contient les multiples éléments squelettiques de la main et du pied, carpes/tarses, métacarpes/métatarses et phalanges. Cette organisation morphologique est très conservée chez les Tétrapodes malgré une variation évolutive considérable liée à des adaptations à des locomotions variées (course, saut, vol…).
Au cours du développement, les bourgeons s’agrandissent et les éléments cartilagineux du futur squelette et les masses musculaires se mettent progressivement en place.
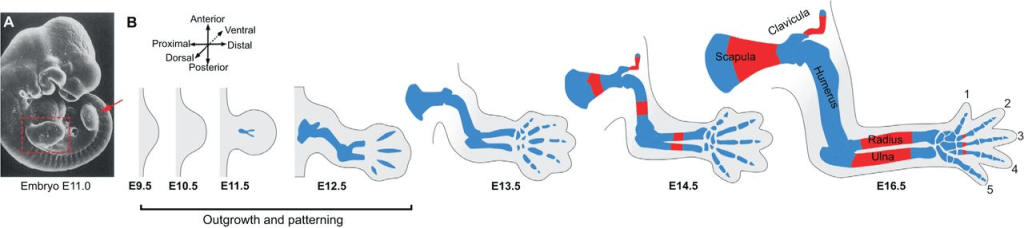
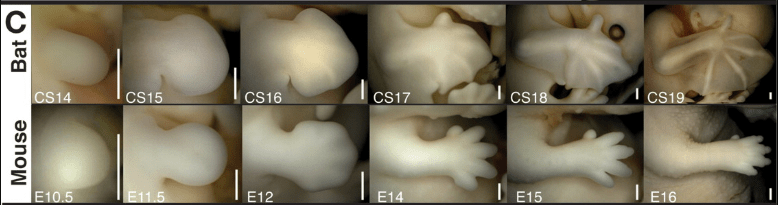
À l’extrémité des membres chiridiens, les doigts sont initialement reliés par une zone interdigitale où les cellules sont finalement éliminées par apoptose. Des différences notables sont observées entre certaines espèces comme par exemple entre la souris et la chauve-souris. Chez les bourgeons de membre antérieurs de la chauve-souris, la zone interdigitale ne meurt pas et permet de générer la surface portante de ce Mammifère volant.
L’axe proximo-distal est contrôlé par un épaississement du l’épiderme distal appelé AER (pour Apical Ectodermal Ridge ou crête apicale ectodermique). Cet épithélium épaissi borde la région distale du bourgeon de membre en croissance. Son ablation entraîne un membre tronqué de sa partie distale. L’AER produit des facteurs de croissance indispensables à la croissance du bourgeon de membre.

L’AER se caractérise par l’expression de plusieurs membres de la famille des facteurs de croissance des fibroblastes (FGF), dont FGF8 est le plus important (Mariani et al., 2008). Nous avons vu dans la partie précédente que son expression est induite par FGF10 qui est exprimé dans le mésenchyme du bourgeon de membre. FGF10 n’agit pas seul et la voie Wnt3a/β-caténine doit être simultanément activée (Barrow et al., 2003).
La fonction cruciale de l’AER a été révélée pour la première fois par les expériences classiques d’ablation réalisées sur l’embryon de poulet par Saunders et ses collaborateurs. L’ablation de l’AER produit des membres atrophié de leur partie distale où le niveau tronqué est précisément corrélé avec le stade où l’AER a été retiré. Ces expériences ont révélé pour la première fois que les segments de membre se forment progressivement, dans une séquence proximo-distale et ont caractérisé l’AER en tant que tissu inducteur essentiel au développement des membres, contrairement à l’hypothèse courante à l’époque selon laquelle l’ectoderme n’était qu’une structure passive et protectrice.
Afin de tenir compte des résultats des expériences d’élimination de l’AER et ainsi d’expliquer comment diverses cellules mésodermiques acquièrent leur propre information proximo-distale, Wolpert et ses collègues ont proposé le « modèle de la zone de progression ». Ce modèle postule que les cellules mésodermiques distales, sous-apicales, dans une région appelée la zone de progression (ZP) acquièrent progressivement des valeurs positionnelles plus distales selon le temps passé sous l’influence de l’AER. Cependant, l’épaisseur de la ZP n’a pas été définie avec précision. Bien que plusieurs gènes présentent des domaines d’expression rappelant la ZP, parmi lesquels Msx1, N-myc et Tfap2a, un marqueur de ZP fiable n’a pas été identifié.
Le modèle ZP a été réévalué à plusieurs reprises et les mécanismes et modèles par lesquels les cellules progénitrices des membres mésenchymateux acquièrent progressivement des destins plus distaux est encore un sujet de recherche actif. Des études sur des embryons de poulet soutiennent un « modèle signal-temps » où la spécification du segment de membre proximal dépend de signaux en provenance du tronc de l’embryon, tandis que la spécification des segments distaux dépend de l’activation d’un programme qui commence une fois que les progéniteurs du membre distal sont exempts de signaux proximaux en raison de la croissance du bourgeon. Ce programme implique la transition progressive d’un mode proximal à un mode distal d’expression des gènes Hox qui est contrôlé par un gradient proximo-distal des facteurs de transcription Meis sous le contrôle de la signalisation FGF provenant de l’AER.
La perte génétique conditionnelle de Meis1/2 dans le membre de la souris entraîne des défauts de structuration proximodistale.
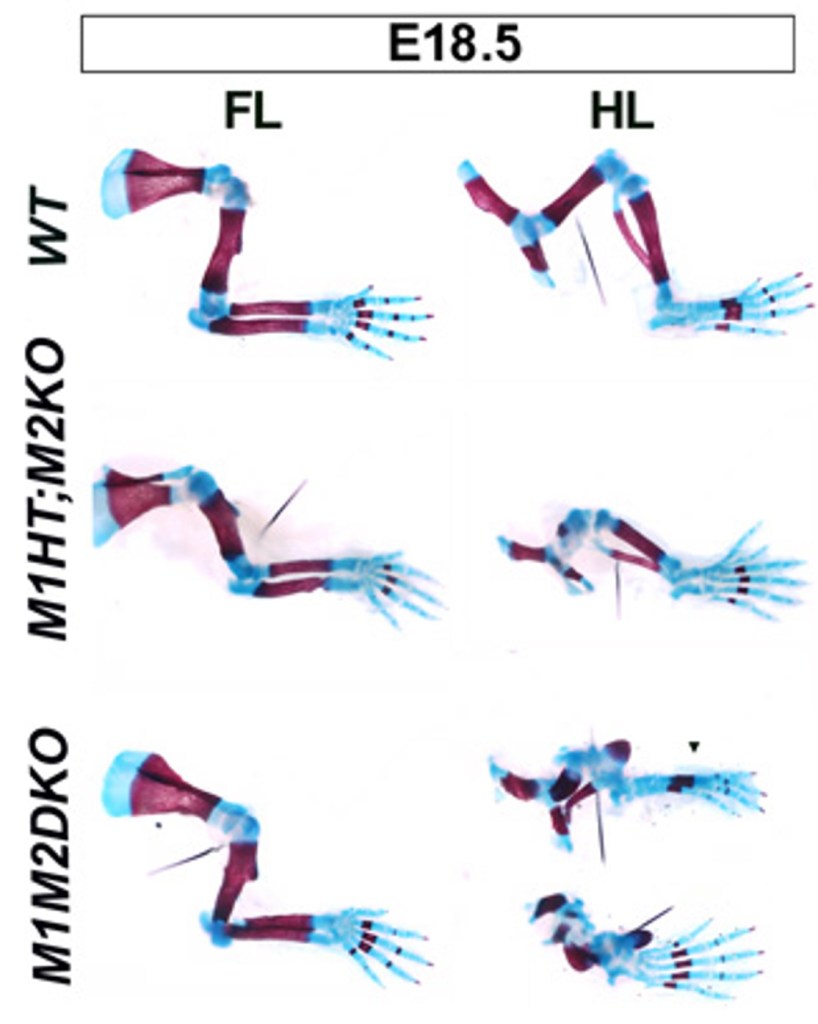
L’application d’acide rétinoïque (RA) peut favoriser les destins proximaux (Tamura et al., 1997). L’implantation de billes chargées de RA dans les bourgeons des membres active l’expression des régulateurs transcriptionnels Meis. Meis1 et Meis2 sont d’abord exprimés dans tout le mésenchyme du bourgeon de membre naissant et leur expression se restreint de manière proximale au cours de la croissance du bourgeon. L’expression ectopique de Meis1 dans les bourgeons des membres de poulet et de souris provoque des transformations de structures distales en structures proximales, tandis que l’implantation de billes chargées de FGF8 dans le mésenchyme proximal inhibe l’expression de Meis (Capdevila et al., 1999; Mercader et al., 2000). Ces résultats ont conduit au modèle à deux signaux pour la structuration de l’axe proximo-distal, avec RA provenant du flanc de l’embryon et la signalisation FGF venant de l’AER qui s’opposent pour spécifier les identités proximale et distale, respectivement (Mercader et al., 2000).
Comme l’AER ne se forme qu’après la formation du membre proximal, retardant ainsi la production de FGF distaux jusqu’après l’initiation du bourgeon de membre, cela entraîne une expression précoce de Meis1/2 dans tout le membre. Une fois l’AER établi, l’expression de Meis1/2 est réprimée par les FGF distaux, créant ainsi une limite d’expression de Meis1/2 qui la laisse dans une position proximale alors que le membre distal continue de croître sans expression de Meis1/2.
L’axe proximo-distal du bourgeon de membre est aussi sous le contrôle d’une partie des complexes des gènes Hox (les complexes A et D avec les parties les plus en 5′ du complexe incluant les gènes Hoxa9 à Hoxa13 et Hoxd9 à Hoxd13). La règle de colinéarité que l’on observe pour les complexes Hox et l’axe antéro-postérieur de l’embryon s’applique ici sur l’axe proximo-distal : les gènes les plus en 3′ spécifient les parties les plus proximales (humérus ou fémur) et les gènes les plus en 5′ spécifient les parties les plus distales (les doigts). De nombreuses malformations congénitales des doigts sont associées à des mutations dans HOXD13.

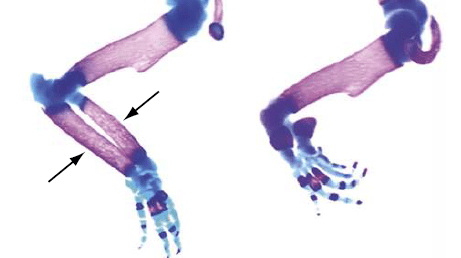
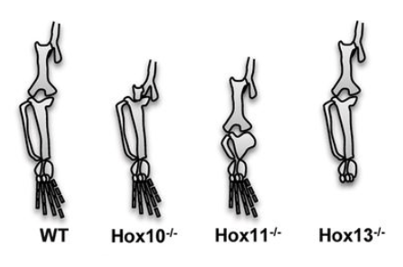
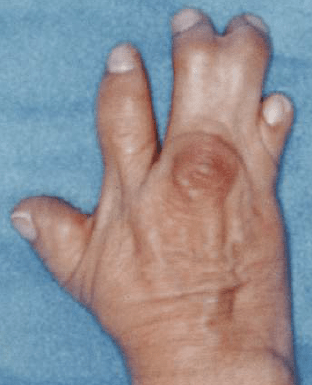
D’un côté du groupe de gènes Hox, une série d’enhancers (dans le domaine chromatinien appelé T-DOM) contrôlent l’expression proximale de Hoxd9 à Hoxd11 et de l’autre côté, une série d’enhancers (dans le domaine chromatinien appelé C-DOM) contrôlent l’expression distale de Hoxd12 à Hoxd13 (Montavon et al., 2011 ; Andrey et al., 2013). Une frontière de TAD (domaine d’activation topologique) avec des protéines CTCF attachées dessus entre les gènes Hoxd11 et Hoxd12 assurent une relative imperméabilité entre les deux séries d’enhancers, empêchant par exemple Hoxd13 d’être exprimé dans la région proximale (Rodriguez-Carballo et al., 2017).
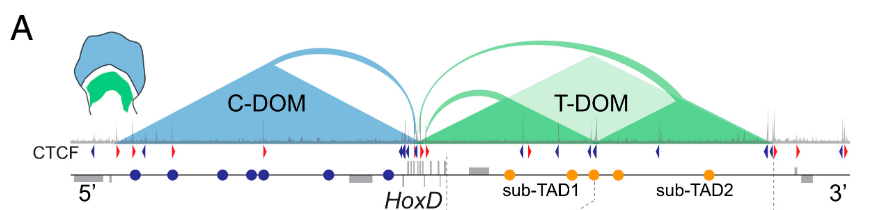
Un gradient d’un niveau de Meis1/2 élevé à un niveau faible (vu plus haut) est nécessaire pour une transition de la spécification d’une position proximale (Hoxa10 et Hoxd10 de l’humérus) vers la spécification d’une position intermédiaire (Hoxa11 et Hoxd11 de l’avant-bras). C’est donc un contrôle dépendant des signaux FGF et acide rétinoïque qui contrôlent l’expression de Meis1/2. La disparition de l’acide rétinoïque après le début de l’expression de Hoxa11 déclenche la transition vers la spécification de la position distale (Hoxa13 et Hoxd13 du poignet et des doigts) qui se fait de manière intrinsèque (dépendante du temps et non plus tellement des signaux) (Delgado et al., 2020).
L’axe antéro-postérieur et son contrôle
L’axe antéro-postérieur est contrôlé par la ZPA, qui est une région dans la partie postérieure du bourgeon de membre. Sa greffe dans la région antérieure d’un bourgeon de membre receveur entraîne une duplication des doigts avec une disposition en miroir.
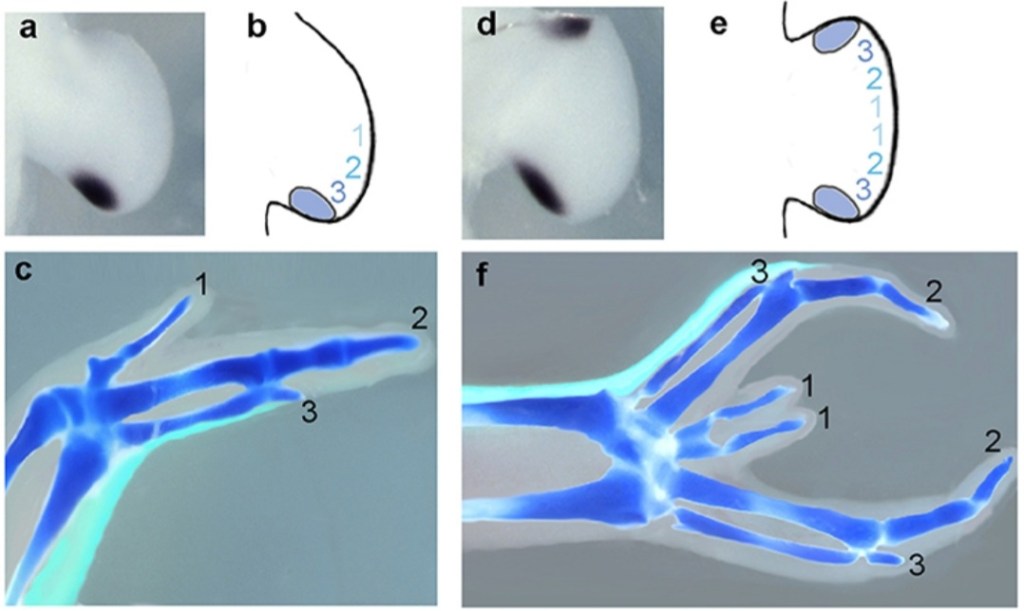
Source : https://www.frontiersin.org/articles/10.3389/fcell.2017.00014/full
La greffe d’une ZPA de souris dans la partie antérieure d’un bourgeon de membre de poulet provoque également une duplication en miroir des doigts (dont les cellules seront formées à partir des cellules de poulet et non de souris, ce qui démontre une fois de plus l’induction). Cela démontre que le signal en provenance de la ZPA est conservé chez tous les Vertébrés.
Il s’est écoulé 25 ans entre la découverte de l’activité ZPA par Saunders et Gasseling en 1968 et la preuve formelle que c’est Shh qui est le morphogène impliqué produit par la ZPA (Riddle et al., 1993). Un dosage de Shh dans des portions de bourgeons de membre à l’aide d’un test biologique a montré qu’il y a 5 fois plus de Shh dans les tissus postérieurs d’un bourgeon de membre que dans les tissus antérieurs. Une greffe de billes imprégnées de Shh dans la région antérieure a le même effet que la greffe de ZPA et des mutations perte-de-fonction partielles ou totales de Shh aboutissent à une antériorisation des doigts. Shh agit donc comme un morphogène, changeant le destin des cellules selon sa concentration : plus il est concentré, plus il induit un destin postérieur aux cellules.
Les pertes-de-fonction de Shh aboutissent aussi à une réduction du nombre de doigts ce qui est l’opposé de la multiplication par deux du nombre de doigts en cas d’expression ectopique de Shh dans la région antérieure. On constate donc qu’en plus de la fonction de polarisation selon l’axe antéro-postérieur, Shh joue un rôle dans l’induction de la formation des doigts en tant que telle.
L’expression de Shh dans la ZPA est contrôlée par un enhancer de 800 pb, la ZRS, qui se trouve 1 Mb (1 million de paires de bases) en amont du site de démarrage de la transcription de Shh.
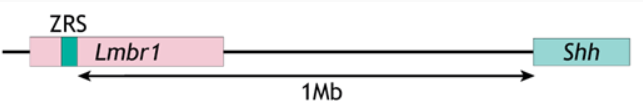
Des mutations ponctuelles dans cet enhancer provoque des malformations des doigts chez l’Homme comme la polydactylie préaxiale de type 2, la syndactylie de type IV ou le syndrome mésomélique de Werner (Lettice et al., 2003, 2008; Farooq et al., 2010; Furniss et al., 2008; Gurnett et al., 2007; Semerci et al., 2009; Wieczorek et al., 2010). Les limites du domaine d’expression de Shh sont contrôlées au cours du développement du bourgeon par les facteurs de transcription de type Ets, Etv4 et Etv5 (Lettice et al., 2012). Si on mute leurs sites de liaison dans la ZRS, une expression ectopique de Shh apparaît dans la région antérieure du bourgeon, ce qui aboutit à des malformations digitales. GATA6 intervient également pour éviter une expression antérieure de Shh (Kozhemyakina et al., 2014).
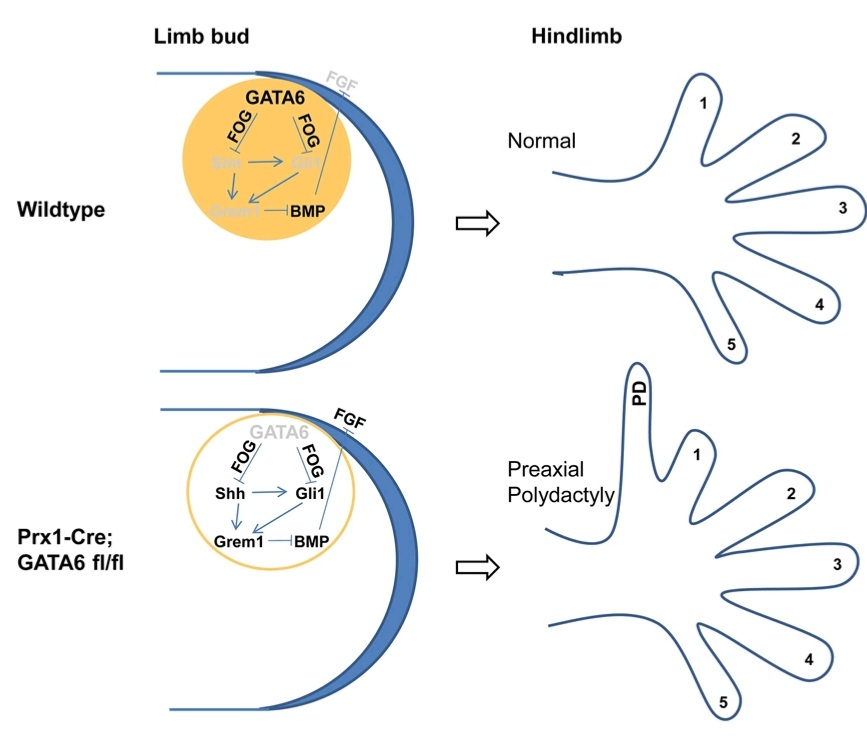
Cette région antérieure qui s’oppose à l’expression de Shh est mise en place par Irx3/5 au début du développement du bourgeon de membre (Li et al., 2014).
Pour en savoir plus sur les voies de signalisation activées par Sonic Hedgehog voir cette page.
Des 2 transducteurs nucléaires de Shh, Gli3 a la plus forte activité de répresseur en absence de Shh et Gli2 est l’activateur le plus puissant en présence de Shh (Sasaki et al., 1999). Gli1 n’est pas régulé par la protéolyse lors de la voie de transduction Shh comme Gli2 et Gli3, mais est lui-même une cible transcriptionnelle directe de la voie de signalisation Shh ainsi qu’un activateur transcriptionnel des cibles de Shh (Bai et al., 2002, Sasaki et al., 1999). Gli1 est en grande partie inutile pour le développement normal des membres, bien que des phénotypes de malformations subtiles des doigts se produisent chez les mutants nuls Gli1 dans le contexte d’autres mutations affectant la voie de signalisation (Park et al., 2000). Des analyses de mutants de souris ont démontré que Gli3 joue le rôle principal dans le membre, alors que Gli2 joue un rôle mineur (Bowers et al., 2012). La perte de Gli3 entraîne une polydactylie et une perte partielle de la régionalisation antéro-postérieure, suggérant qu’un gradient de Gli3 répresseur (Gli3R) peut à la fois restreindre le nombre de doigts et réguler leur identité AP (Wang et al. , 2000). De plus, Gli3 est épistatique à Shh. Le knock-out composé Shh-/-;Gli3-/- a un phénotype de membre polydactyle identique au mutant Gli3-/- seul, indiquant que le rôle majeur de Shh dans l’autopode est d’inhiber la formation de Gli3R (Litingtung et al., 2002; Welscher et al., 2002).
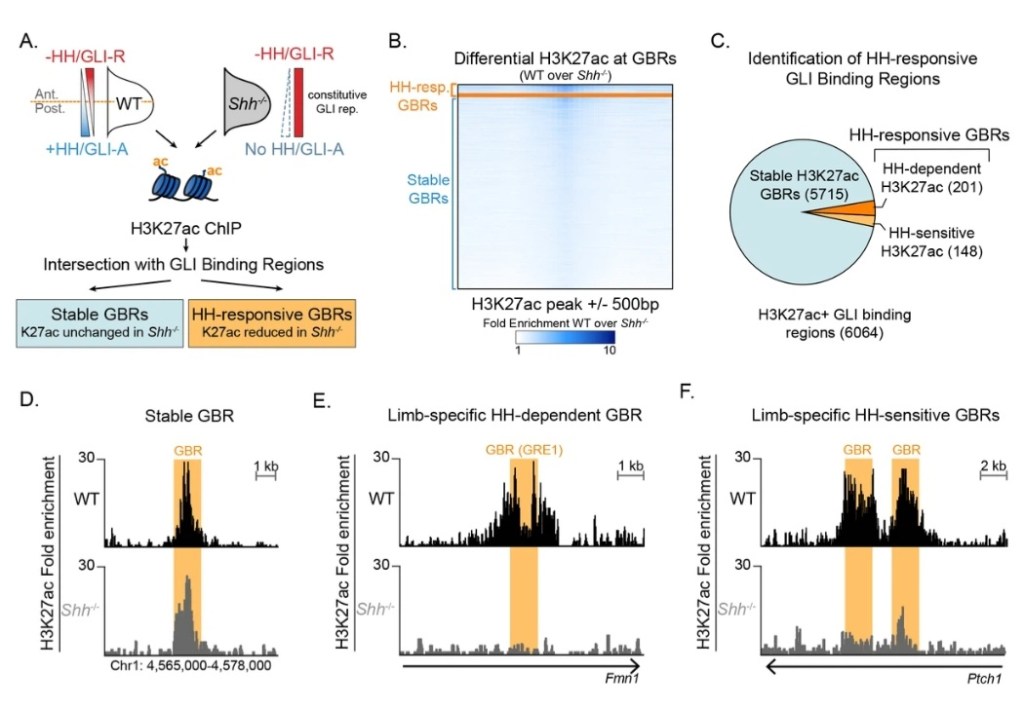
(A) Schéma expérimental permettant d’identifier différentes catégories de régions liées aux facteurs GLI (GBR). On compare les régions liées à GLI dépendant ou indépendant de la présence de Shh, en comparant les résultats des immunoprécipitations avec un anticorps reconnaissant la marque épigénétique H3K27 de bourgeons de membre de souris sauvage (WT) ou sans Shh (Shh-/-). Les bourgeons de membre utilisés proviennent de souris de E10,5. (B) Heatmap illustrant l’enrichissement différentiel en H3K27ac dans les bourgeons des membres WT et Shh-/- pour les GBR sensibles et insensibles (« stable ») à Shh. (C) Classification des catégories de GBR selon leur réponse obtenue en B (D-F) L’enrichissement en H3K27ac dans les bourgeons de membre WT et Shh -/- est montré dans une région génomique représentative près d’un GBR insensible (D) et des GBRs connus comme répondant à Shh : un GBR de GRE1 codant Gremlin1 (E) et un GBR de Ptch1 (F). Source : https://elifesciences.org/articles/50670
Les souris Shh-/- présentent des bourgeons de membre tronqués, réduits à
leur partie proximale. C’est la conséquence du fait que SHH a également un rôle de maintien de l’AER et de sa sécrétion de FGF. En retour, un défaut de
production de FGF de l’AER est nécessaire au maintien de la ZPA et de sa
sécrétion de SHH. Le tout constitue une boucle de rétrocontrôle positif. Le mécanisme par lequel Shh maintient FGF dans l’AER implique le contrôle par Shh des interactions entre la protéine Gremlin et les BMP. L’expression de Gremlin est initialement activée par le facteur de transcription bHLH dHand (ou Hand2) (te Welscher et al., 2002) mais c’est la voie de signalisation Shh qui le maintient. Gremlin empêche les BMP produits dans le mésenchyme mésodermique d’inhiber l’expression de FGF dans l’AER.
En effet, des études génétiques chez la souris ont révélé que la cible mésodermique de Shh, Gremlin (Grem1), un antagoniste sécrété des BMP, relaie le signal Shh à l’AER en modulant les effets négatifs des BMPs sur le maintien de l’AER (Zuniga et al., 1999). La caractérisation de l’enhancer Grem1 a révélé une régulation complexe par la voie Shh, impliquant un rôle potentiel pour GliA en plus d’un effet majeur de dérépression de Gli3R (Benazet et al., 2009, Li et al., 2014, Nissim et al., 2006, Vokes et al., 2008, Zuniga et al., 2012).
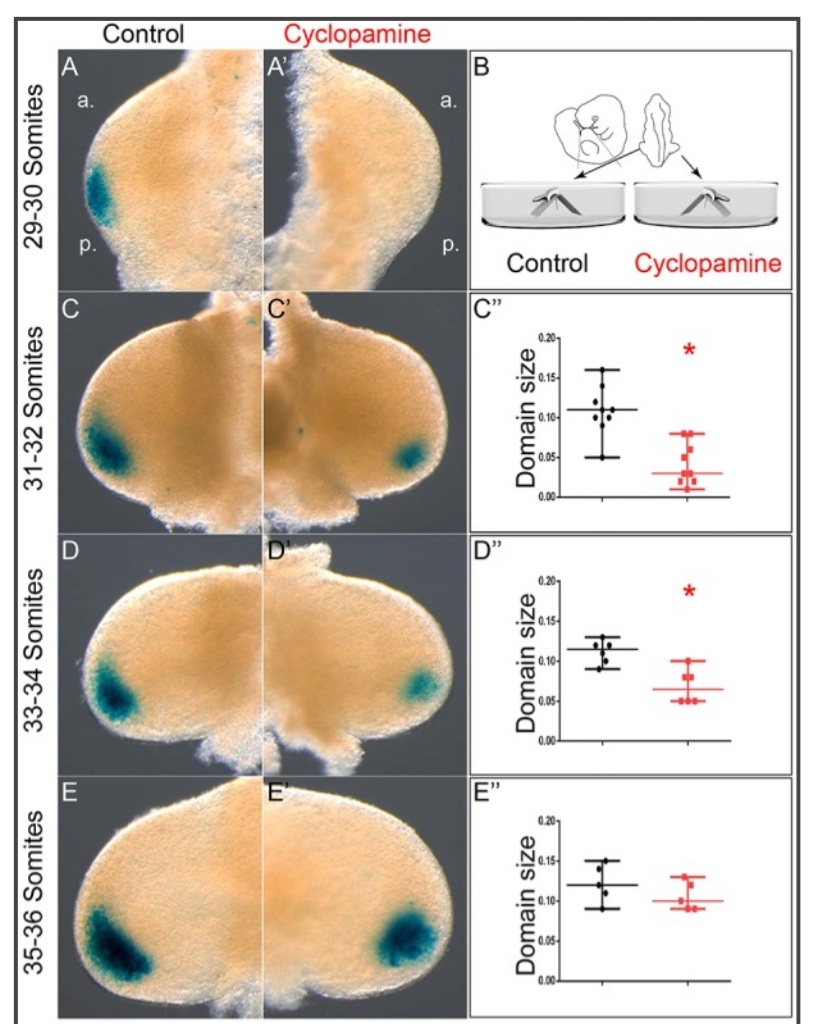
La manipulation de l’AER chez l’embryon de poulet a établi que l’AER est nécessaire pour induire l’expression de Shh.

Une ablation de l’AER peut être remplacée par l’ajout de Fgf4 (Laufer et al., 1994, Niswander et al., 1994). Shh, à son tour, induit l’expression de Fgf4 dans l’AER postérieur, formant une boucle de rétroaction positive entre ZPA et AER. La suppression des deux Fgf4;Fgf8 chez la souris a définitivement montré que les AER/FGFs sont essentiels pour l’initiation de l’expression de Shh dans le membre (Sun et al., 2002). Les facteurs de transcription de la famille Ets, effecteurs nucléaires des signaux FGF, sont des régulateurs clés de l’enhancer du membre ZRS de Shh (Lettice et al., 2012).
BILAN :
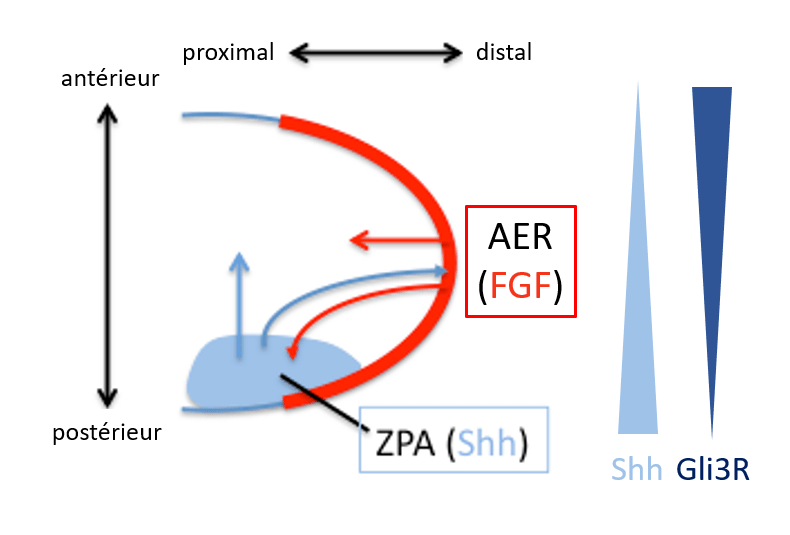
Au fur et à mesure que le bourgeon de membre s’allonge, la ZPA (et l’expression de Shh) persiste distalement dans le mésenchyme postérieur sous-jacent à l’AER. L’expression de Shh dans les cellules mésodermiques postérieures plus proximales diminue à mesure que les cellules se déplacent au-delà de l’influence des FGF sécrétés par l’AER.
La boucle de régulation de maintien mutuel entre les FGF et Shh se termine lorsque le facteur de transcription Tbx2 inhibe l’expression de Gremlin (Farin et al., 2013).
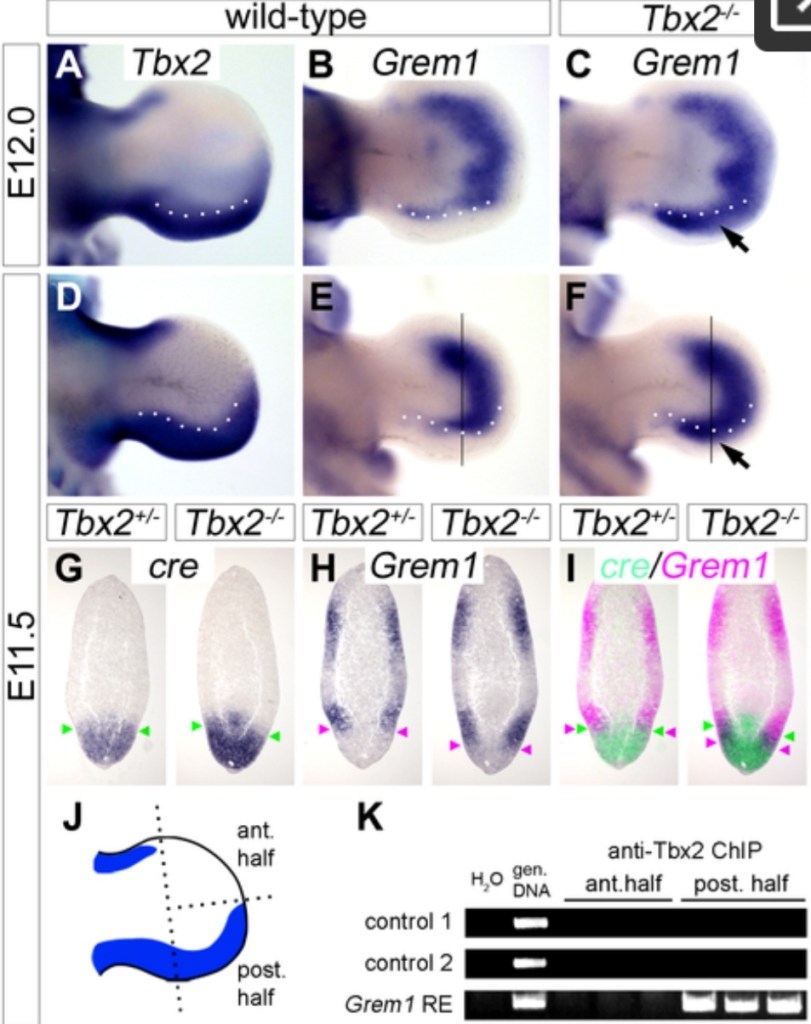
(A–F) Analyse en hybridation in situ de l’expression de Tbx2 et de Grem1 dans les membres postérieurs d’embryons à E12.0 et E11.5 sauvages ou Tbx2−/−. Les flèches (C, F) indiquent l’expansion postérieure de l’expression de Grem1 dans les bourgeons Tbx2−/−. Des lignes pointillées blanches délimitent la limite antérieure de l’expression de Tbx2. (G–I) Analyse comparative de l’expression de cre, contrôlée par les régions régulatrices de Tbx2, et de Grem1 par hybridation in situ sur des sections sagittales adjacentes des membres postérieurs d’embryons E11.5 Tbx2cre/+ (contrôle) et Tbx2cre/cre (mutant). Les plans de coupe sont indiqués par des lignes noires en E et F. Les pointes de flèches marquent la limite antérieure de l’expression cre (en vert) et la limite postérieure de l’expression Grem1 (en rose). Les superpositions de fausse couleur dans (I) montrent l’expansion postérieure de Grem1 dans les membres postérieurs de Tbx2−/−. (J–K) Analyse en ChIP (immunoprécipitation de la chromatine) utilisant la chromatine des moitiés antérieure ou postérieure des membres postérieurs de type sauvage E11.5. Le schéma (J) montre l’expression de Tbx2 (bleu) exclusivement dans la moitié postérieure du membre. (K) Détection par ChIP-PCR des régions d’ADN liées à Tbx2. L’ADN génomique total a été utilisé comme témoin positif. Dans les moitiés postérieures des membres, Tbx2 se lie à l’enhancer qui contrôle l’expression dans le membre de Grem1 mais pas aux autres régions génomiques qui servent de contrôle. Source : https://journals.plos.org/plosgenetics/article?id=10.1371/journal.pgen.1003467
Les cibles de la voie Shh dans le membre ont été identifiées d’une part à partir d’une analyse à l’échelle du génome des sites de liaison directs de Gli3 dans les bourgeons de membre de souris par ChIP avec un transgène Gli3 marqué avec un tag (Vokes et al., 2008) et d’autre part à partir de plusieurs analyses d’expression génique à la suite d’activations et inhibitions de la voie Shh (Lewandowski et al., 2015, McGlinn et al., 2005, Probst et al., 2011). L’identification des sites de liaison des Gli in vivo a révélé plus de 200 gènes cibles avec des séquence de liaison aux Gli (GBR) ainsi qu’un ensemble de cibles tout aussi large dépourvu de GBR, qui restent moins bien caractérisés (Vokes et al., 2008). La majorité des gènes cibles de GBR+ qui sont exprimés dans un domaine postérieur sensible à Shh sont régulés principalement par la dé-répression (c’est-à-dire la libération de Gli3R du site).
Les cibles Shh comprennent trois classes fonctionnelles principales : 1) les cibles qui fournissent directement des informations de position conduisant à des identités spécifiques et/ou à des relais d’indices de position (par exemple, les différentes zones antéro-postérieures) vers d’autres signaux en aval ; et 2) des cibles jouant un rôle dans l’expansion des bourgeons des membres – qui comprend à la fois des cibles directes agissant dans le mésoderme et des relais vers l’ectoderme pour moduler la fonction de l’AER et des FGFs qu’il produit. Un troisième groupe est constitué de cibles directes impliquées dans la transduction ou la régulation de la voie Hh elle-même, contribuant à de vastes circuits de rétroaction interconnectés. La régulation croisée et de rétroaction élaborée entre Shh lui-même, l’expression de Gli3 et les cibles « en aval » a rendu difficile la séparation nette des contributions fonctionnelles des différents composants du réseau de régulation génique. Ces cibles incluent plusieurs régulateurs de l’expression de Shh tels que Prdm1 (Robertson et al., 2007).
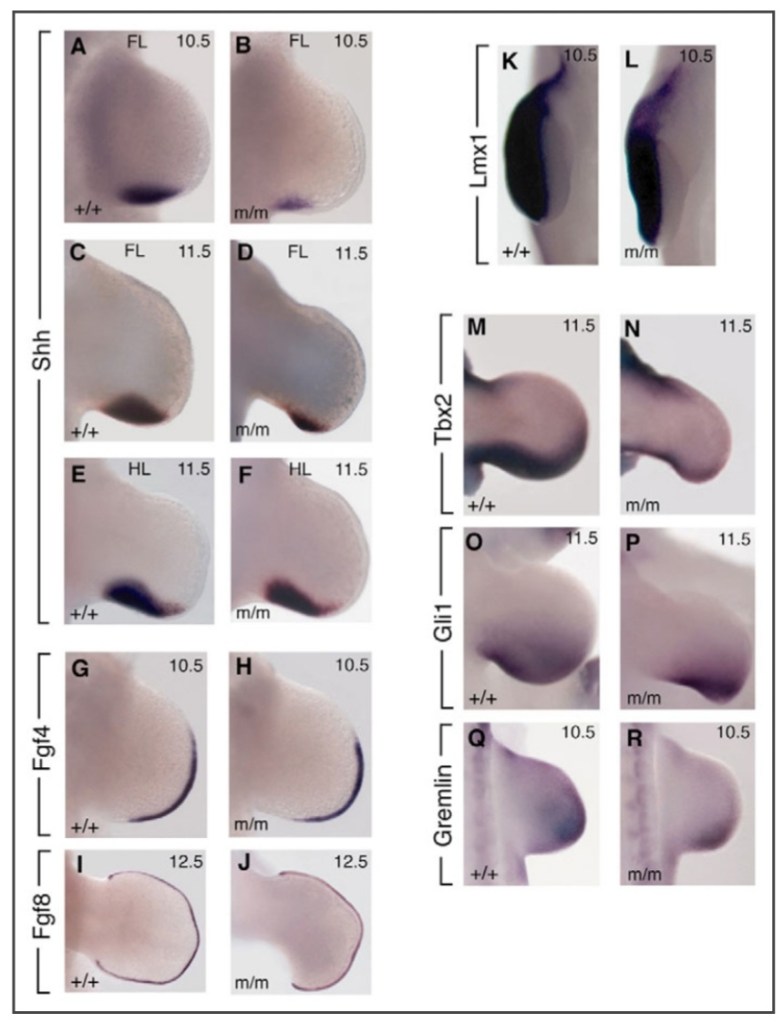
Parmi les cibles de la voie de signalisation Shh potentiellement régulatrices de l’identité des doigts, les gènes de la partie 5′ des complexes Hoxd et Hoxa ont été les plus fortement impliqués sur la base des phénotypes des mutants simples et composés (Davis et Capecchi, 1996, Zakany et al., 1997). Cependant, il n’y a pas de « code Hox » ; leurs cibles sont encore mal comprises et les mécanismes par lesquels ils transmettent des indices de position précoces restent peu caractérisés.
Polarité dorso-ventrale du bourgeon de membre
La polarité dorso-ventrale correspond par exemple à la différence entre le dos et la paume de la main. C’est l’ectoderme qui contrôle l’identité dorso-ventrale du mésenchyme mésodermique du bourgeon de membre car si, avec des excisions et des greffes, on inverse les positions de l’ectoderme dorsal et de l’ectoderme ventral, l’ensemble du membre aura une polarité inversée. Cela amène à penser qu’un signal inducteur est envoyé de l’ectoderme au mésoderme sous-jacent. Ce signal inducteur a été identifié comme Wnt7a et il est sécrété par les cellules de l’ectoderme dorsal (et pas par les cellules de l’ectoderme ventral) (Parr et McMahon, 1995). Il induit l’expression du facteur de transcription Lmx1b dans le mésoderme dorsal (Riddle et al., 1995).
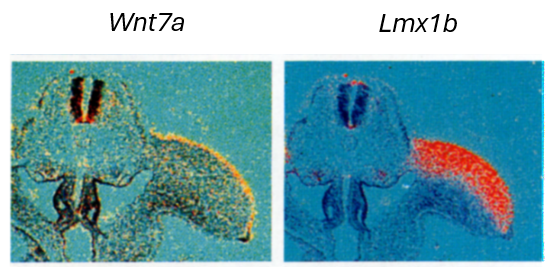
Un commentaire plus détaillé de cette figure est disponible cette vidéo.
Source : https://www.sciencedirect.com/science/article/pii/0092867495901035
Les souris knock-out Lmx1b-/- présentent des membres avec uniquement des structures ventrales. Des patients avec des mutations perte-de-fonction de LMX1B n’ont pas d’ongle à leurs doigts et pas de rotule à leur genoux (ongles et rotules sont typiquement des structures dorsales).
Les structures ventrales ne sont cependant pas produites par défaut. Elles nécessitent l’expression de Engrailed-1 dans l’ectoderme ventral (Loomis et al., 1996).
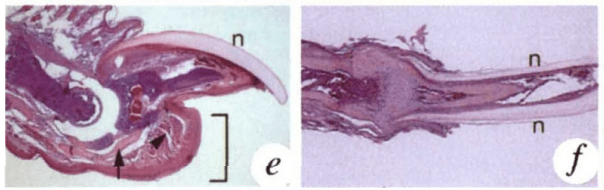
Cette expression est induite par des BMP en provenance du mésenchyme mésodermique (Pizette et al., 2001). Engrailed-1 réprime alors l’expression de Wnt7a dans l’ectoderme ventral permettant à ce que son expression soit strictement cantonnée à l’ectoderme dorsal.
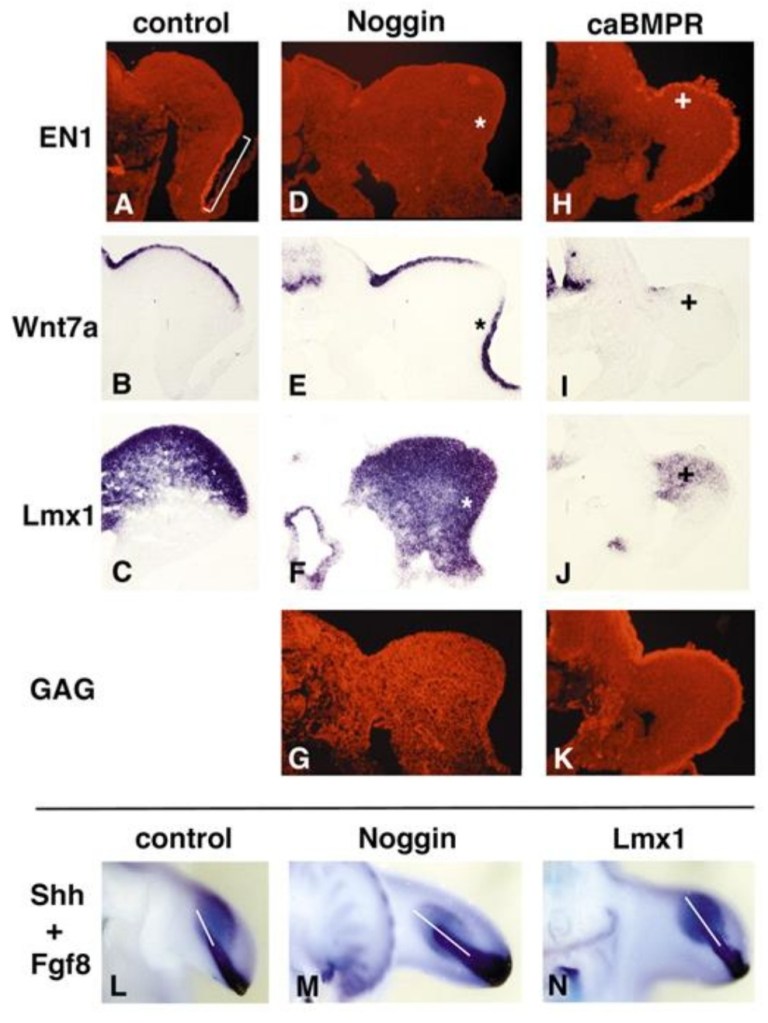
Comme nous l’avons vu avec la coordination entre le développement de l’axe proximo-distal et antéro-postérieur, l’axe dorso-ventral ne se met pas en place de manière isolée. Par exemple, l’absence de Wnt7a aboutit non seulement à des membres ventralisés mais aussi à un manque de doigts postérieurs. Cela vient du fait que Wnt7a participe au maintien de l’expression de Shh dans la ZPA en synergie avec FGF4 venant de l’AER.
SCHEMA-BILAN
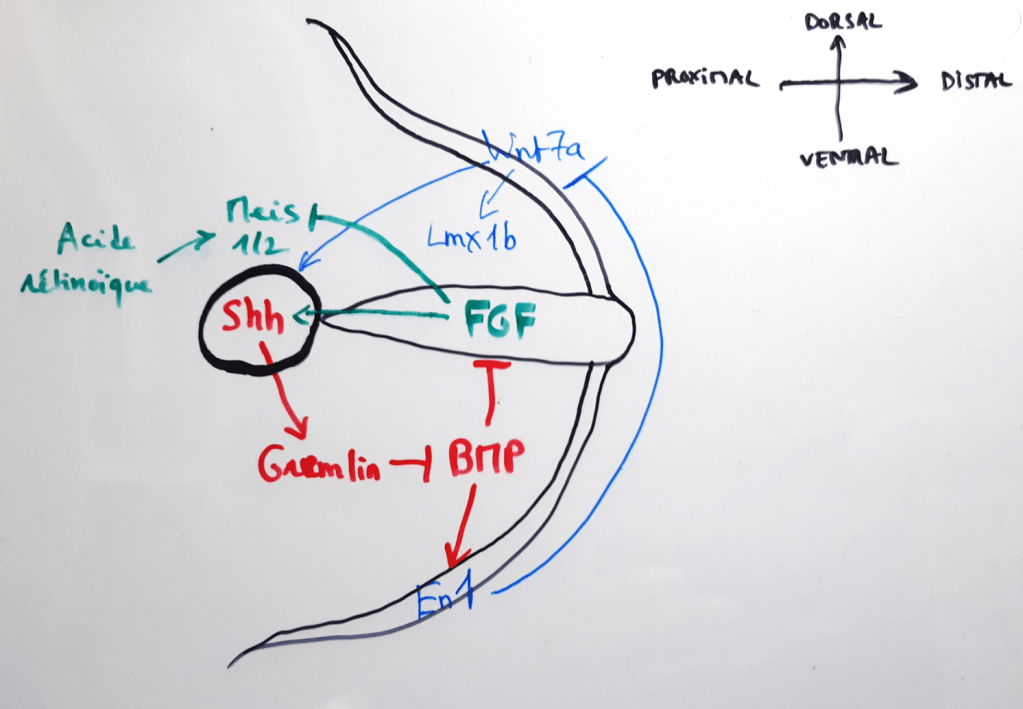
Contrôle de l’apoptose interdigitale
Pour revoir les concepts fondamentaux concernant l’apoptose, voir cette page.
L’apoptose dans le mésenchyme interdigital est indispensable à la morphogenèse des doigts. Elle est induite par les BMP (Kaltcheva et al., 2016)
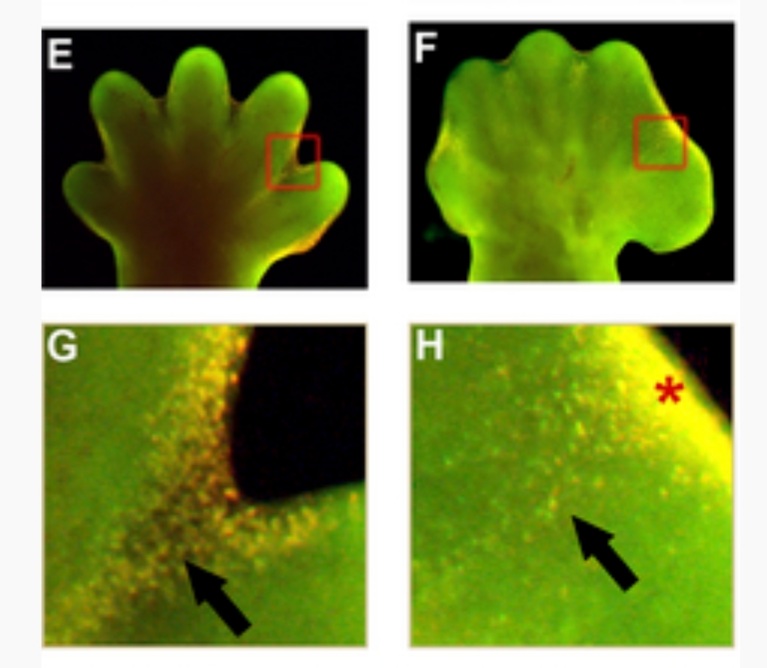
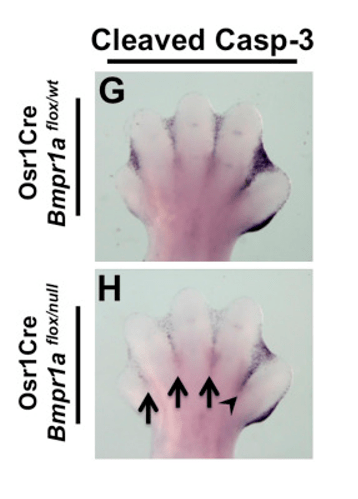
L’un des gènes cibles de la voie BMP dans la zone interdigitale pour le déclenchement de l’apoptose est celui codant le facteur de transcription Msx2.
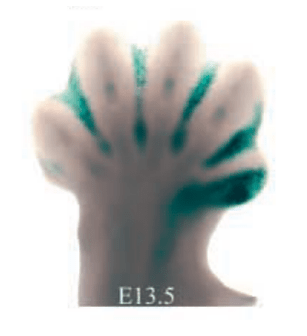
Les doigts sont protégés de l’action des BMP par l’expression de Noggin (Merino et al., 1998).
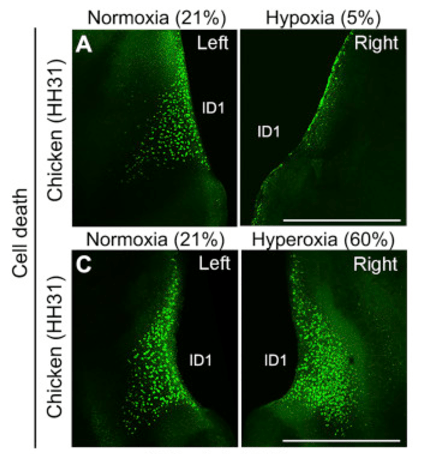
Dans la future aile de la chauve-souris ainsi que dans la future patte postérieure de canard, on n’observe pas d’apoptose contrairement aux futures pattes de la souris ou du poulet.

Les mécanismes moléculaires de ces différences ont été étudiés. Dans la zone interdigitale de la future aile de la chauve-souris ainsi que de la future patte postérieure de canard, un ligand Gremlin est produit et inhibe l’action des BMP. Dans la future aile de la chauve-souris des ligands FGF agissent en complément pour maintenir en vie les cellules de la zone interdigitale et en plus activer leur prolifération ce qui permet de créer la grande surface portante interdigitale.
Signalons que paradoxalement, une bonne vascularisation de la zone interdigitale est nécessaire pour que l’apoptose y soit activée et cela est sans doute lié au fait que des espèces réactives de l’oxygène (ROS) et donc le stress oxydatif sont nécessaires pour l’apoptose interdigitale (une bonne vascularisation assure un bon apport en O2 permettant de produire des ROS) (Eshkar-Oren et al., 2015).