Par Patrick Pla, Université Paris-Saclay

Le poisson zèbre ou Danio rerio appartient à la famille des Cyprinidés et il vit dans les eaux douces de l’Inde et du Bangladesh. Il est prisé des aquariophiles… et des chercheurs en biologie du développement !
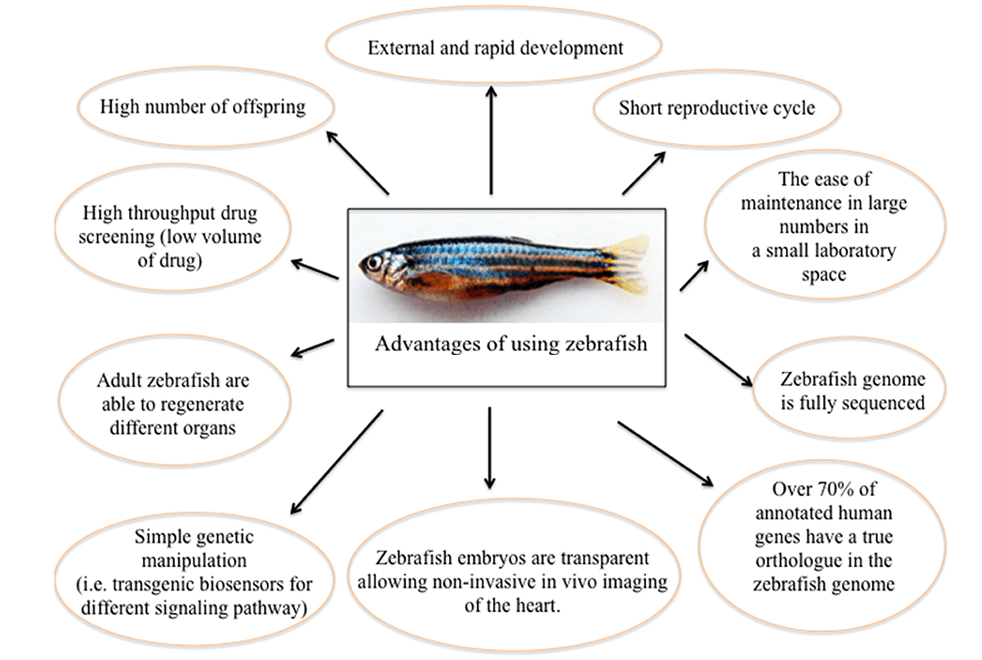
Son utilisation en recherche a été popularisé dans les années 1970 par Georges Streisinger de l’Université d’Oregon (Etats-Unis). Le poisson-zèbre est omnivore et vit 5 ans environ en laboratoire. Son cycle de vie est de 90 jours donc on peut avoir une nouvelle génération tous les 3 mois. L’embryon est mince et transparent ce qui facilite son étude.
Son développement embryonnaire est très rapide et en 24h, une grande partie des étapes du développement ont été franchies.
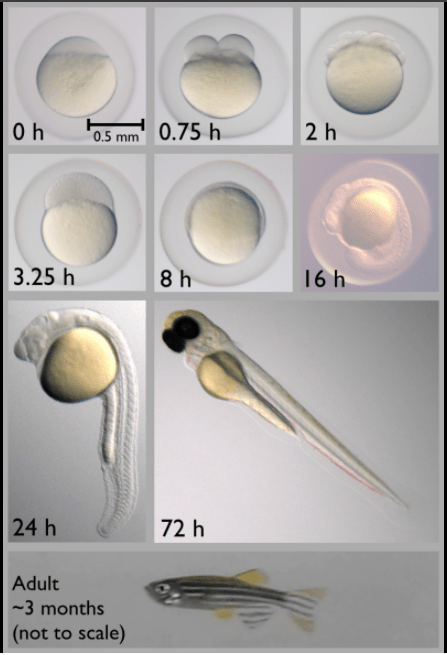
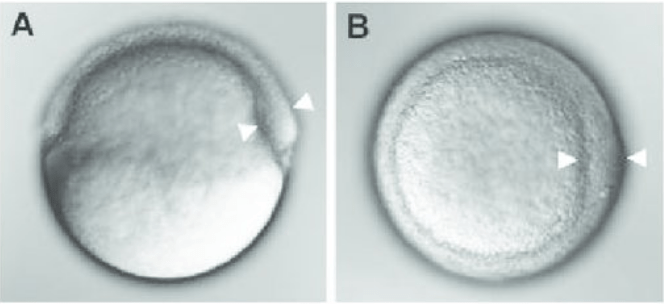
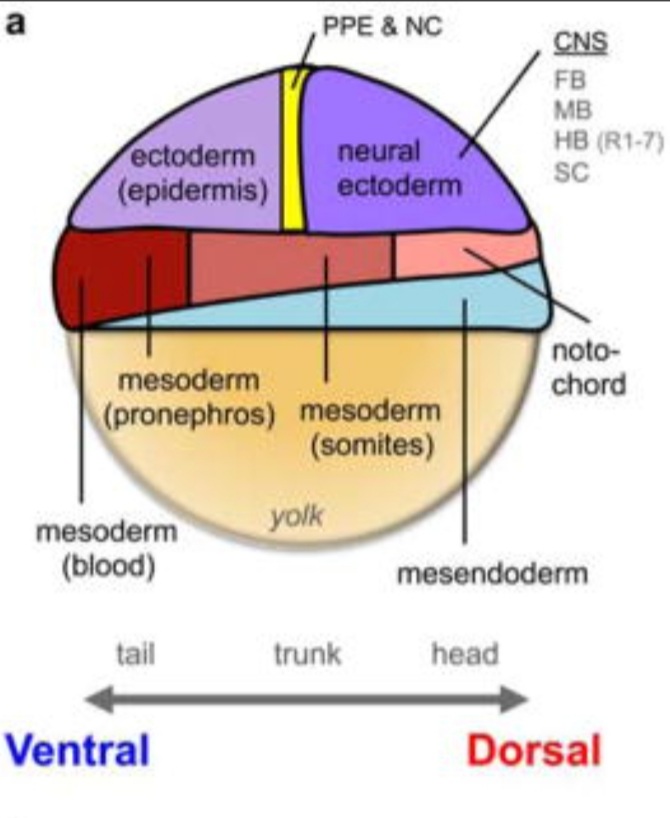
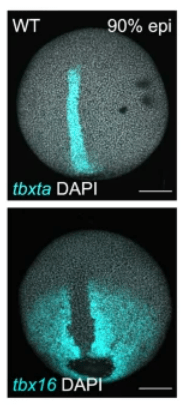
Le génome du poisson-zèbre a été entièrement séquencé en 2009. Il fait 1,4 milliards de paires de bases et il contient 26.000 gènes. Le poisson-zèbre est un outil génétique puissant et près de 30.000 allèles sont connus et répertoriés par le ZIRC (Zebrafish International Research Center). Le poisson-zèbre a souvent 2 gènes orthologues pour chaque gène humain à cause d’une duplication générale du génome chez les Téléostéens.
On peut faire facilement des lignées transgéniques chez le poisson zèbre.
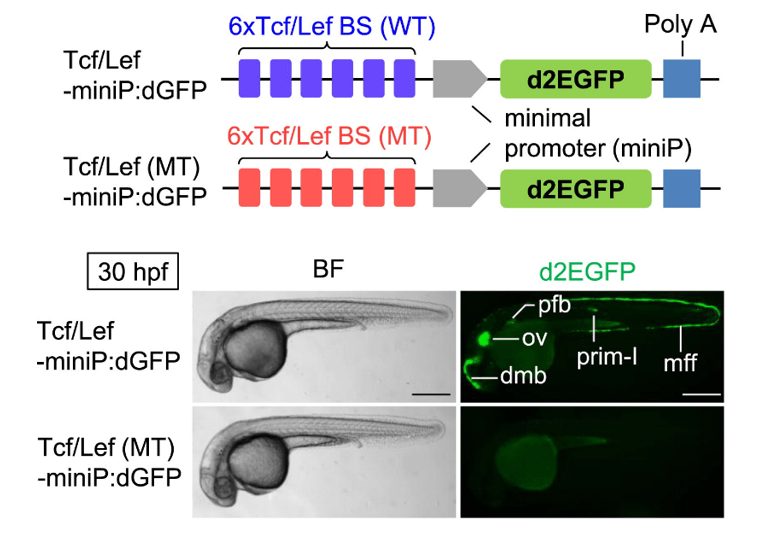
De très nombreuses lignées rapportrices existent comme par exemple une lignée qui exprime GFP sous le contrôle des éléments de réponse à la signalisation Wnt où se fixent LEF/TCF et que vient rejoindre la β-caténine lorsque la voie Wnt est activée (Shimizu et al., 2012).
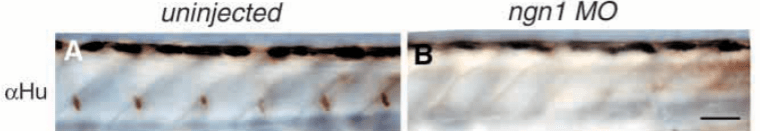
On peut injecter des morpholinos dans le poisson-zèbre, des oligonucléotides synthétiques anti-sens qui inhibent la production d’une protéine et permettent ainsi des études de perte-de-fonction.
On peut également réaliser des expériences de perte- ou gain-de-fonction grâce à la méthode CRISPR-Cas9.
Le poisson zèbre a le potentiel de régénérer complètement plusieurs organes adultes et embryonnaires, notamment le cœur (régénération possible de 20% de cet organe), les nageoires et de nombreux composants du système nerveux (comme la rétine), ce qui peut en faire un modèle intéressant de thérapie régénérative : il s’agirait d’activer les mêmes mécanismes chez les Mammifères (et notamment les humains).
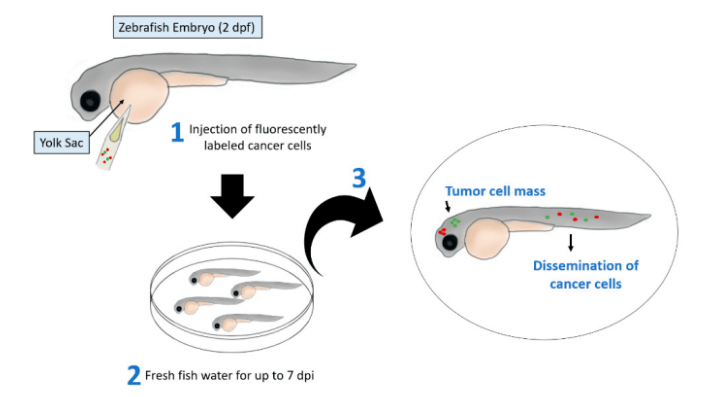
Le poisson-zèbre peut aussi servir pour tester les capacités de migration de cellules métastatiques.
QUELQUES SITES DE REFERENCE :
Le développement post-embryonnaire du poisson zèbre
Zebrafish International Ressource Center
Compte Twitter @ZebrafishRock
ON EN PARLE :
Le poisson-zèbre, précieux allié des chercheurs
QUELQUES EQUIPES FRANCOPHONES QUI TRAVAILLENT SUR CE MODELE :
Neurogénétique du poisson-zèbre – Institut Pasteur, Paris
Calcifications cardio-vasculaires : mécanismes et thérapies – Marseille Medical Genetics
- Adhérences cellule-cellule
- Arabidopsis thaliana
- Axe antéro-postérieur chez la drosophile
- Biomécanique du développement
- Caenorhabditis elegans
- Concepts principaux
- Contrôle de la traduction
- Contrôle de la transcription
- Contrôle génétique et épigénétique
- Croissance du tube pollinique et double fécondation chez les Angiospermes
- Croissance et guidage axonal
- Des modèles animaux moins classiques
- Développement de l’oeil des Vertébrés
- Développement et évolution
- Et l’Humain ?
- Exercices sur l’ovogenèse, la spermatogenèse et la fécondation
- Exercices sur le contrôle de l’expression des gènes
- Exercices sur le développement des bourgeons de membre
- Exercices sur le développement des muscles striés squelettiques
- Exercices sur le développement des végétaux et les hormones végétales
- Exercices sur les cycles et les divisions cellulaires
- Exercices sur les étapes du développement, les inductions embryonnaires et la mise en place des axes de polarité
- Exercices sur les matrices extracellulaires, le cytosquelette et les adhérences cellule-cellule
- Exercices sur les voies de signalisation
- Glossaire
- Glossaire des termes liés à la génétique
- Glossaire des termes liés au cytosquelette, la matrice extracellulaire, l’adhérence et la migration cellulaire
- Hématopoïèse et développement des cellules du système immunitaire
- Histoire de la biologie cellulaire et de la biologie du développement
- L’acide rétinoïque
- L’apoptose
- L’autophagie
- L’organogenèse
- L’ovogénèse prépare le développement embryonnaire
- La drosophile
- La fécondation
- La formation des somites
- La gastrulation
- La gastrulation (version allégée)
- La métamorphose chez les Hexapodes et les Amphibiens
- La neurogénèse chez les mammifères adultes
- La neurulation
- La poule
- La signalisation calcique
- La souris
- La superfamille TGFβ et ses voies de signalisation
- La voie de signalisation de l’auxine et ses rôles
- La voie de signalisation Hedgehog
- La voie de signalisation Hippo et ses composants YAP/TAZ
- La voie de signalisation Notch
- Le clivage
- Le cytosquelette
- Le destin des cellules et les réseaux de régulation génique
- Le développement des bourgeons de membre
- Le développement des muscles striés squelettiques
- Le développement des organes génitaux et des cellules germinales
- Le développement du cortex
- Le méristème apical caulinaire en phase végétative et lors de la formation d’une fleur
- Le xénope
- Les cellules des crêtes neurales
- Les cellules et les gènes en action dans le développement
- Les cellules souches
- Les cellules tumorales
- Les cycles et les divisions cellulaires
- Les étapes du développement
- Les étapes du développement embryonnaire d’Arabidopsis thaliana et leur contrôle
- Les inductions embryonnaires et les gradients de morphogène
- Les matrices extracellulaires animales
- Les organismes modèles
- Les outils pour étudier l’expression et la fonction des gènes
- Les parois des cellules végétales
- Les techniques et les outils pour la biologie cellulaire
- Les transitions épithélio-mésenchymateuses et les migrations cellulaires
- Les vésicules extracellulaires
- Les voies de signalisation
- Les voies de signalisation FGF
- Mise en place des axes chez les Vertébrés
- Structures et processus cellulaires
- Voies de signalisation WNT
