Par Patrick Pla, Université Paris-Saclay
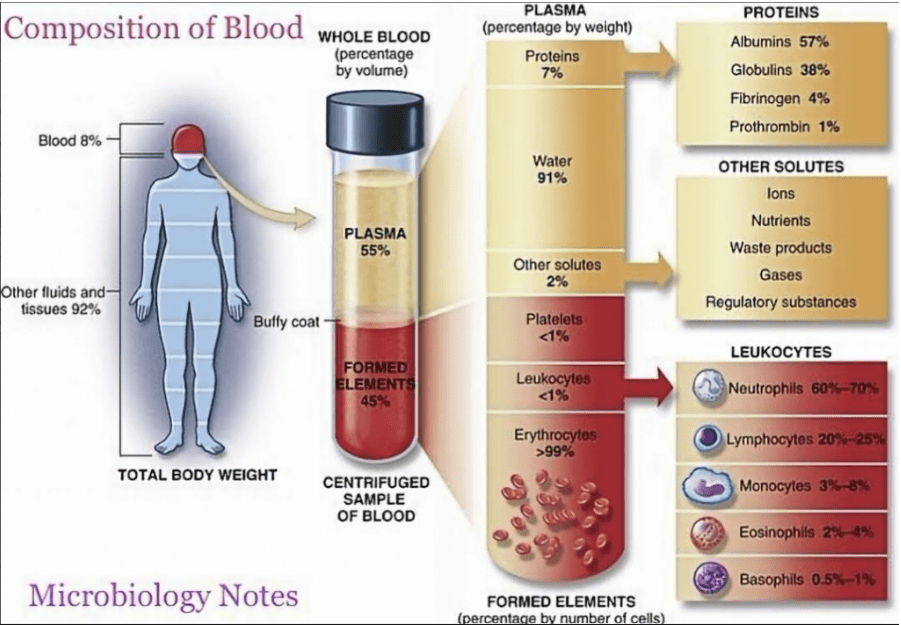
L’hématopoïèse est la formation de cellules sanguines. Les premières étapes sont communes aux globules rouges et aux cellules du système immunitaire mais pour les étapes tardives nous nous intéresserons essentiellement à ces dernières.
Le système immunitaire permet la protection de l’individu contre les éléments étrangers et notamment les pathogènes que ce soit des petits virus, des bactéries ou des grands vers parasites.
Nous nous restreindrons au système immunitaire des Mammifères.
Bien que présenté habituellement dans des livres spécialisés en immunologie, le développement des diverses cellules du système immunitaire n’en reste pas moins un problème de développement : les cellules acquièrent une identité, prolifèrent, migrent et se différencient. La particularité des cellules du système immunitaire vient simplement du fait qu’une partie de leur différenciation et de leur fonctionnement dépend de la présence de molécules reconnues comme appartenant à un pathogène (ou à du non-soi).
- L’hématopoïèse embryonnaire
- L’hématopoïèse post-natale
- Les cellules NK
- Macrophages et monocytes
- Les lymphocytes T
- Les lymphocytes B
- Les leucémies et les myélomes
L’hématopoïèse embryonnaire
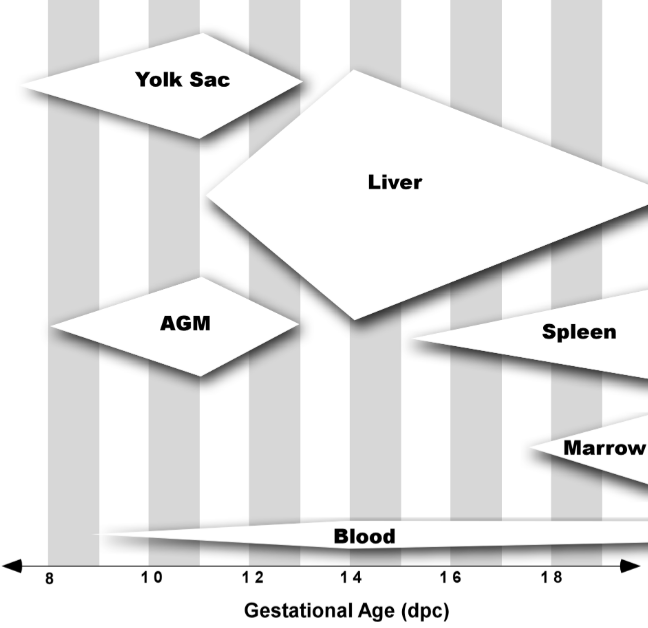
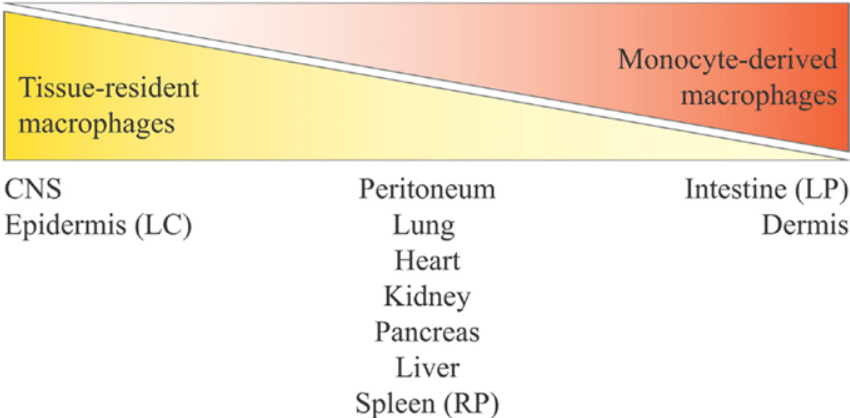
L’hématopoïèse embryonnaire chez les Mammifères se déroule à différents endroits et se produit en trois étapes successives (« vagues »). Les deux premières vagues ont lieu dans le sac vitellin extra-embryonnaire (à partir de 16 jours après la fécondation chez l’Homme et E7,5 chez la souris), avec la formation de populations hématopoïétiques transitionnelles (hématopoïèse mégaloblastique). Certaines cellules apparentées aux macrophages formées lors de cette vague sont maintenues chez l’adulte dans des tissus qu’elles colonisent lors du développement embryonnaire (cellules microgliales dans le système nerveux central, cellules de Langerhans dans la peau et cellules de Kupffer dans le foie) (Mirshekar et al., 2014).
La troisième vague apparaît à l’intérieur de l’embryon dans la région de l’aorte-gonade-mésonéphros (AGM) (à partir du 21ème jour post-fécondation chez l’Homme et E9,5 chez la souris). Elle est à l’origine de l’hématopoïèse adulte (hématopoïèse normoblastique), entraînant la formation de cellules souches hématopoiétiques (HSC) qui fournissent à l’organisme une production continue de cellules sanguines. Cependant, les HSC produites dans l’AGM ne peuvent pas remplacer directement des HSC de la moelle osseuse post-natale et elles doivent passer par une étape de maturation dans le foie.
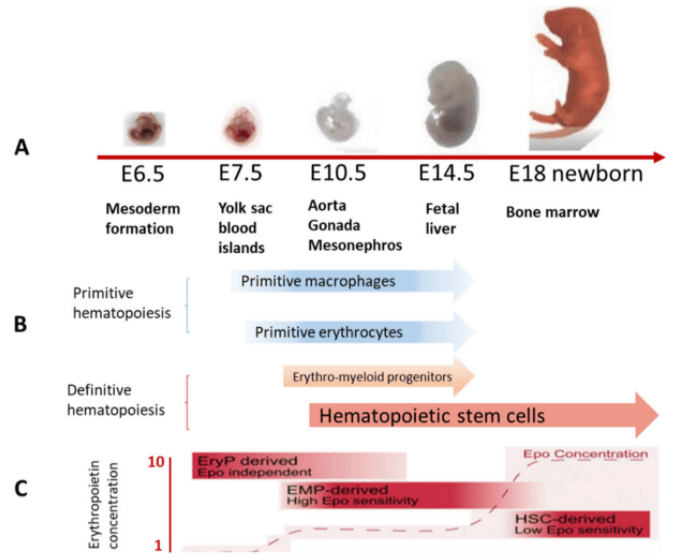
Lors de la première vague d’hématopoïèse, trois types de cellules sanguines sont produites : les érythrocytes primitifs exprimant des globines embryonnaires, les mégacaryocytes et les macrophages.
Dans les deuxième et troisième vagues embryonnaires, des cellules multipotentes définitives sont formées : des progéniteurs érythromyéloïdes (EMP) dans les îlots sanguins du sac vitellin et des cellules souches hématopoïétiques (HSC) dans l’aorte dorsale. Dans ces vagues, un type d’endothélium hautement spécialisé appelé endothélium hémogénique se forme. Les précurseurs hématopoïétiques sont alors générés par une transition endothéliale à hématopoïétique (Swiers et al., 2013).
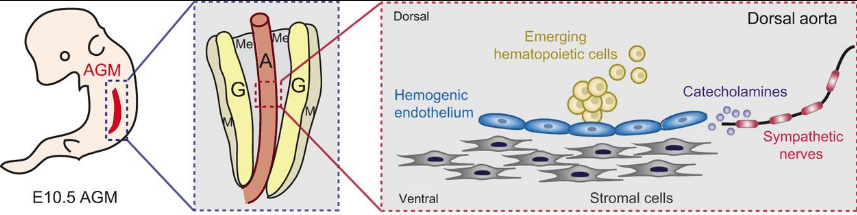
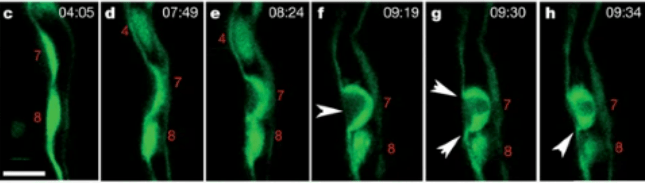
Dans l’aorte dorsale, la niche où sont produites les HSC est mise en place sous le contrôle des signaux BMP produits par le mésenchyme sous-aortique. Une population de cellules endothéliales de l’aorte dorsale dérivant des somites (endotome) et exprimant le gène Meox1 produit également des signaux nécessaires à la genèse de cette niche (Nguyen et al., 2014). La région hématopoïétique est néanmoins restreinte à la moitié ventrale de l’aorte dorsale par la présence de Noggin (un inhibiteur de BMP) qui est produit par les somites en position dorsale par rapport à l’aorte. Les catécholamines (probablement la noradrénaline) produites par les neurones sympathiques qui se trouvent à proximité sont également importantes pour la formation et le maintien de la niche des HSC (Fitch et al., 2012).
La voie NOTCH intervient ensuite : la signalisation DLL4/NOTCH1 active le programme endothélial, tandis que la signalisation JAG1/NOTCH1 le bloque pour déclencher la spécification hémogénique.
Les cellules endothéliales du sac vitellin et de l’aorte dorsale expriment les gènes Tek ou Ly6a. La formation à la fois d’EMP dans le sac vitellin et de CSH dans l’aorte dorsale nécessite la participation du facteur de transcription Runx1 et de son partenaire, CBFb. De plus, l’expression du facteur de leucémie hépatique (HLF) marque spécifiquement le développement des HSC dans l’embryon et n’est pas exprimé dans les EMP. HLF reste un marqueur important des HSC par la suite, y compris chez l’adulte (Lehnertz et al., 2021).
Parmi les nombreux facteurs de transcription impliqués dans le système hématopoïétique, TAL1/SCL est un régulateur essentiel. Cette protéine hélice-boucle-hélice basique est non seulement au sommet de la hiérarchie des facteurs de transcription impliqués dans la spécification hématopoïétique, mais est également essentielle pour la fonction des cellules souches hématopoiétiques adultes et pour la maturation terminale des lignées individuelles de différenciation hématopoïétique. Les embryons avec knock-out SCL meurent au 9,5ème jour de développement en raison de l’absence d’érythropoïèse primitive et de myélopoïèse dans le sac vitellin (Robb et al., 1995). L’expression d’un autre facteur de transcription, Runx1, joue un rôle important dans l’embryogenèse, en particulier au moment de la formation des premières cellules sanguines, son expression précédant légèrement leur apparition (Nottingham et al., 2007).
L’entrée dans la circulation des HSC leur permet de migrer vers les futurs sites hématopoïétiques (Horton et al., 2021). Après une brève période d’expansion des HSC dans le placenta (Gekas et al., 2005), le foie fœtal devient le site principal de l’hématopoïèse définitive jusqu’à ce que les HSC migrent vers la rate (Christensen et al., 2004) et la moelle osseuse juste avant la naissance. L’hématopoïèse splénique reste active jusqu’à environ 2 semaines après la naissance. Puis ensuite, la moelle osseuse est le siège primaire des HSC et de l’hématopoïèse (Rowe et al., 2016).
L’hématopoïèse post-natale
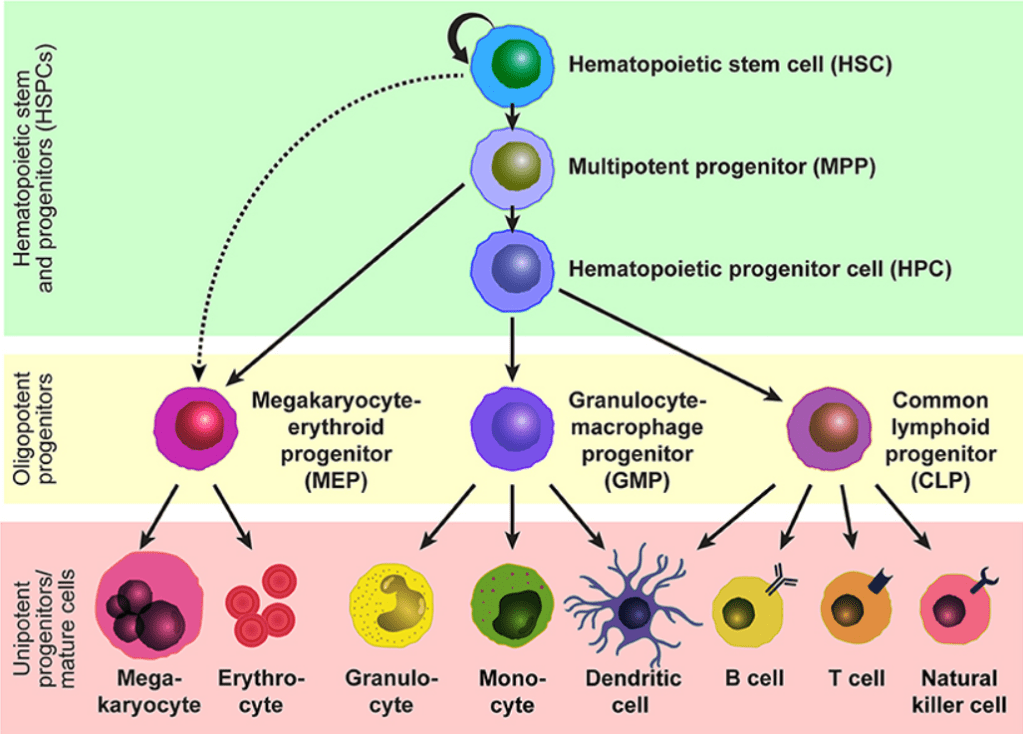
Les cellules souches hématopoïétiques (HSC) soutiennent la production de sang tout au long de la vie et sont les unités fonctionnelles lors de la greffe de moelle osseuse. L’énorme quantité de cellules sanguines produites chaque jour chez l’homme (environ un milliard) repose sur un nombre suprenamment petit de HSC (quelques dizaines de milliers à quelques centaines de milliers chez l’Homme selon diverses estimations). Les HSC sont capables de s’auto-renouveler pour maintenir leur pool tout en produisant toutes les cellules sanguines matures par différenciation en progéniteurs multipotents (MPP) et en cellules progénitrices hématopoïétiques (HPC) avec des potentiels de différenciation plus limités. La population des HSC est fonctionnellement hétérogène en termes : (i) de cinétique du cycle cellulaire (avec certaines HSC se divisant seulement 5 fois durant les 2 ans de vie d’une souris (Cabezas et al., 2017)), (ii) de capacité d’auto-renouvellement et (iii) de potentiel de différenciation, et ces sous-types peuvent être distingués par des marqueurs tels que CD229 et le facteur von Willebrand. Toutes ces populations sont cependant multipotentes mais restreintes en potentialité aux lignées hématopoïétiques : par exemple des HSC transplantées dans un coeur ne peuvent pas générer de nouveaux cardiomyocytes (Murry et al., 2004).
Signalons que, remarquablement, les HSC injectées dans la circulation sanguine peuvent coloniser les compartiments du stroma de la moelle osseuse que l’on a déplété en HSC précédemment, permettant des thérapies contre les tumeurs lymphoïdes et des études expérimentales sur les HSC.
Chez les adultes, les HSC sont essentiellement quiescentes (on les appelle les LT-HSC pour cellules souches hématopoïétiques à long terme), ce qui les protège de stress d’origine externe et limite les risques de mutations (Biechonski et al., 2017). Leur nombre est étroitement régulé dans des conditions d’équilibre, consistant en <0,01 % des cellules de la moelle osseuse chez la souris. En réponse aux demandes hématopoïétiques aiguës telles qu’une grande perte de sang, une myéloablation, une infection ou une grossesse, les HSC modifient deux aspects de leurs comportements à l’état d’équilibre afin d’augmenter la production des cellules hématopoïétiques nécessaires (Wilson et al., 2008). Premièrement, les HSC quiescentes réintègrent le cycle cellulaire pour proliférer ou se différencier par des divisions cellulaires symétriques ou asymétriques, et deuxièmement, elles se déplacent de la moelle osseuse vers les tissus extramédullaires, tels que la rate. L’acide rétinoïque s’oppose à cette activation des HSC (Cabezas et al., 2017). Le rythme circadien peut aussi influencer les capacités de prolifération des HSC via le système nerveux sympathique qui transmet l’activité du noyau suprachiasmatique de l’hypothalamus (le centre régulateur du rythme circadien) vers le microenvironnement des HSC (Mendez-Ferrer et al., 2009).
Les cellules souches hématopoïétiques à long terme (LT-HSCs) en quiescence dans la moelle osseuse possèdent des mitochondries courtes et fragmentées, une activité mitochondriale réduite ainsi qu’un faible niveau d’espèces réactives de l’oxygène (ROS). En revanche, la sortie de cet état de quiescence est caractérisée par une augmentation de l’activité mitochondriale et de la biogenèse mitochondriale, marquant ainsi la reprise de l’activité cellulaire (Papa et al., 2019).
Si trop de ces HSC sortent de quiescence, leur population diminue après une phase d’expansion initiale car de la différenciation précoce est induite. Des études d’ablation génique chez la souris ont montré que les inhibiteurs du cycle cellulaire, en particulier les inhibiteurs des CDK, à savoir p21, p27 et p57, sont essentiels au maintien des HSC adultes (Cheng et al., 2000; Zou et al., 2011). La kinase dépendante des cyclines CDK6 est également impliquée : les HSC en quiescence profonde n’expriment pas CDK6, contrairement aux HSC capables de se remettre à proliférer plus rapidement lors d’une stimulation mitogène. L’expression forcée de CDK6 dans les HSC à quiescence profonde accélère leur sortie de quiescence (Laurenti et al., 2015). Le facteur de transcription Prdm16 a aussi été impliqué dans ce contrôle car sa perte dans les HSC adultes entraîne une sortie de quiescence et une perte progressive des cellules au fil du temps (Gumundsson et al., 2020).
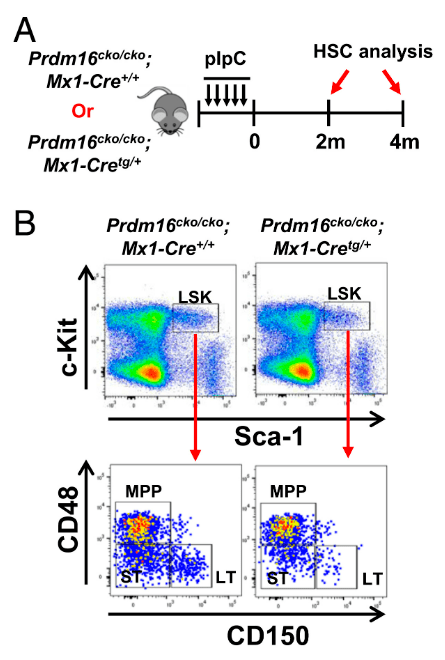
Les HSC doivent aussi exprimer le facteur de transcription Bmi-1. En absence de ce facteur, les souris meurent en 2 mois faute d’avoir renouvelé leurs globules rouges et blancs. Les fonctions de PTBP1, une protéine se liant aux ARN et importante pour l’épissage et la biogenèse des ribosomes sont également indispensables au maintien des HSC (Rehn et al., 2022).
Les HSC ont des taux de synthèse protéique inférieurs à ceux des progéniteurs aux potentialités plus restreintes qu’elles génèrent. Les HSC sont particulièrement sensibles aux altérations de la synthèse des protéines et une augmentation même modeste de la synthèse des protéines entraîne une altération de l’auto-renouvellement (Signer et al., 2016). Cela vient notamment d’une hypophosphorylation des facteurs d’initiation de la traduction 4E-BP1 et 4E-BP2. Une concentration élevée de calcium intracytoplasmique joue aussi un rôle dans l’activation et le maintien de la quiescence (Fukushima et al., 2019).
Le maintien de la capacité d’auto-renouvellement des HSC nécessite que de multiples paramètres soient maintenus dans leur niche. L’auto-renouvellement et l’homéostasie des HSC repose ainsi par exemple sur la liaison de la cytokine thrombopoïétine à son récepteur Mpl (Tong et al., 2007). La thrombopoïétine nécessaire est produite localement dans la moelle osseuse mais aussi plus à distance dans le foie (Decker et al., 2018).
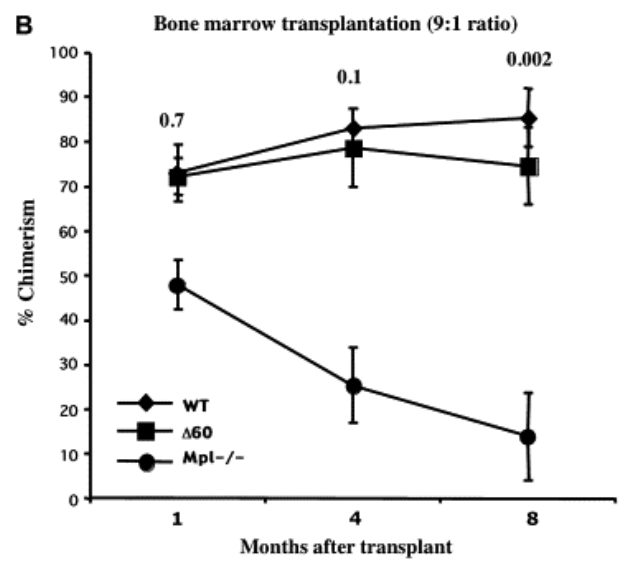
Mpl est dépourvue de toute activité kinase et recrute en présence de thrombopoïétine la kinase Jak2 pour activer plusieurs cascades intracellulaires (voies Mapk, Akt et Stat) (Bersenev et al., 2008). L’inactivation génétique de Mpl (Kimura et al., 1998), Jak2 (Akada et al., 2014) et Stat5 (Wang et al., 2009) entraîne une altération de l’homéostasie des HSC et une défaillance progressive de l’hématopoïèse.
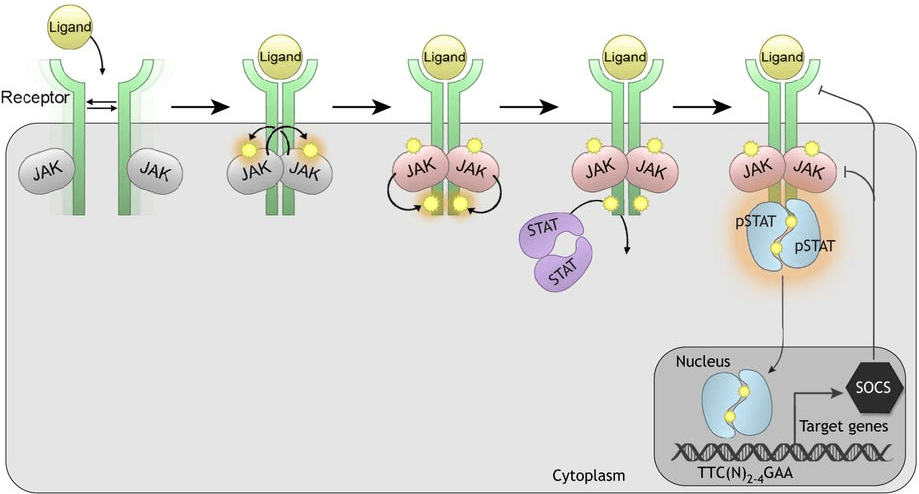
En plus de ces signaux activateurs, Jak2 est également inhibé par les protéines Socs (Kershaw et al., 2013) et Lnk. L’inactivation de Lnk augmente l’activité de Jak2 et la taille du pool de HSC dans le moelle osseuse (Bersenev et al., 2008). En conclusion, Jak2 joue un rôle central dans la régulation de la taille du pool de HSC et un équilibre des régulateurs positifs et négatifs de l’activité de Jak2 contrôle l’homéostasie des HSC dans la moelle osseuse.
La voie Notch qui est active dans les HSC est nécessaire pour maintenir leur capacité d’auto-renouvellement et éviter une différenciation trop importante (Duncan et al., 2005). On retrouve pour Notch le même rôle que dans les cellules souches neurales.
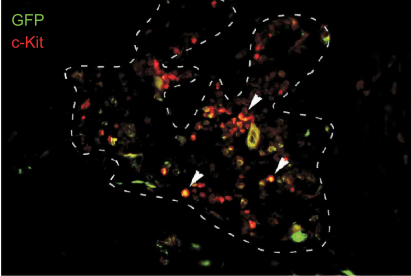
Les cellules souches hématopoïétiques interagissent aussi avec les cellules stromales voisines et les intégrines participent à ces jonctions.

Si on utilise des anticorps bloquant l’interaction intégrine α4β1/VCAM-1, les cellules souches hématopoïétiques finissent par s’échapper dans la circulation sanguine (Papayonnoupoulou et al., 1995). L’interaction entre l’intégrine α4β7 et MadCam-1 est essentielle pour le recrutement des cellules souches hématopoïétiques dans la moelle osseuse soit au cours du développement, soit au cours de transfusions (Katayama et al., 2004). Chez les patients atteints de leucémie myéloïde aigue, l’interaction intégrine α4β1/VCAM-1 est un élément important de la résistance à la chimiothérapie parce que cette interaction active la signalisation NF-kB dans les cellules stromales qui en retour envoient des signaux favorisant la survie des cellules tumorales (Jacamo et al., 2014).
Les fibroblastes de la moelle osseuse contribuent également au maintien de la niche des HSC via la production de CXCL12 (qui se fixe sur le récepteur CXCR4 sur les HSC) et de SCF (Stem Cell Factor) (Sugiyama et al., 2006; Omatsu et al., 2010; Nakatani et al., 2023).
Il existe aussi des mécanismes rétroactifs de contrôle de la quiescence des HSC. Les mégakaryocytes (les cellules qui génèrent les plaquettes) ont un effet stimulant sur cette quiescence via des sécrétions de CXCL4, de TGFβ1 ou de thrompoïétine. Si on déplète la population de mégakaryocytes dans la moelle osseuse, il y a réveil des HSC avec une prolifération aboutissant à leur expansion (Zhao et al., 2014; Nakamura-Ishizu et al., 2015).
La population de HSC, malgré leur apparente homogénéité phénotypique, est néanmoins hétérogène et constituée de cellules biaisées en différenciation lymphoïde ou myéloïde.
Fait intéressant, les lignées hématopoïétiques diffèrent par leur sensibilité au stress génotoxique. Dans plusieurs lignées de souris présentant des déficiences dans les enzymes de réparation de l’ADN, les lignées hématopoïétiques sont globalement épuisées, mais les progéniteurs myéloïdes restent dans des proportions plus élevées que leurs homologues lymphoïdes. Après irradiation γ ou raccourcissement des télomères, l’épuisement global des HSC et la plus grande réduction des progéniteurs lymphoïdes sont causés par le facteur de transcription BATF. Lors de l’activation des médiateurs du point de contrôle de la phase G1 / S, BATF provoque la spécification et la différenciation lymphoïde, réduisant ainsi les pools de CSH auto-renouvelées biaisées vers les lymphoïdes (Wang et al., 2012). Cela préserve des CSH à biais myéloïdes, maintenant ainsi un pool de cellules souches qui peuvent produire des érythrocytes et des plaquettes essentiels. Ce système permet d’éliminer les cellules souches qui pourraient être entrées dans les premiers stades de la tumorigénèse lymphoïde (mais au prix de l’épuisement de la réponse immunitaire adaptative).
Les ostéocytes peuvent également intervenir dans l’hématopoïèse. Ils régulent le développement des neutrophiles par sécrétion de facteurs solubles comme IL19 (Xiao et al., 2021) et ils peuvent également réguler la myélopoïèse (Fulzele et al., 2013). La diminution forcée de la population d’ostéocytes chez la souris par l’expression d’une toxine diphtérique dans leur lignage aboutit à une quantité de progéniteurs myéloïdes plus importante au détriment des progéniteurs lymphoïdes (Ding et al., 2022).
Il existe un dimorphisme sexuel en ce qui concerne l’hématopoïèse adulte. Chez les souris, les HSC des femelles se divisent plus fréquemment et s’auto-renouvellent plus efficacement que les HSC des mâles. Les femmes ont une incidence plus faible de cancers hématologiques que les hommes. Les patientes pédiatriques et les jeunes femmes atteintes de leucémie myéloïde aiguë ont une survie plus importante que les hommes. De plus, les patientes atteintes de leucémie ont une meilleure récupération après une greffe de HSC. Les œstrogènes jouent un rôle dans la régulation de l’hématopoïèse féminine et sont en partie responsables de la division plus fréquente des HSC chez les femmes (Nakada et al. 2014, Heo et al., 2015). Cela joue un rôle important lors de la grossesse. Il existe aussi des réponses immunitaires spécifiques au sexe dans lesquelles les femmes ont tendance à avoir une réaction immunitaire plus forte.
Les HSC sont sensibles à la situation immunitaire générale de l’individu et des infections bactériennes ou virales peuvent changer leur comportement, le plus souvent en stimulant leurs divisions, ce qui stimule la production de progéniteurs puis de cellules du système immunitaire qui pourront combattre l’infection. Cet effet est médié par exemple par l’IFN-γ (Baldridge et al., 2010).
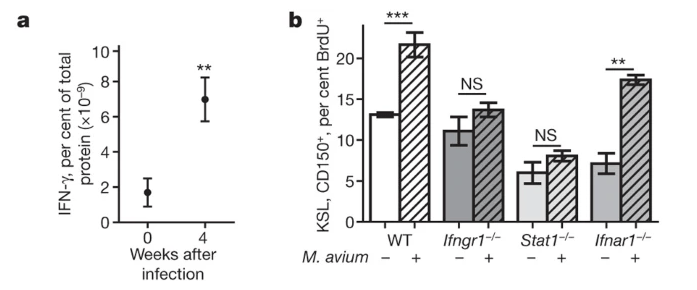
Au fil du temps, les HSC perdent progressivement leur capacité de régénération. Les organismes âgés présentent une régénération lymphoïde atténué, contrebalancé seulement en partie par une régénération myéloïde accrue. Cela contribue à la réduction des cellules immunitaires adaptatives et à l’immunosénescence chez les personnes âgées (Pang et al., 2011; de Haan et al., 2018). Des méthodes de traçage cellulaire in vivo montrent que ce biais ne provient pas d’une évolution des HSC elle-mêmes mais des progéniteurs des différents lignages (Jang et al., 2023). Avec l’âge, l’hématopoïèse dépend de moins en moins des HSC qui s’épuisent et de plus en plus des progéniteurs en aval.
Le « biais myéloïde » favorise la production de monocytes/macrophages et de granulocytes qui ont une durée de vie faible mais empêche la bonne reconstitution des lymphocytes périphériques et la régénération du compartiment lymphoïde, notamment après une transplantation (Lin et al., 2021). Cela provoque aussi une prédisposition aux troubles myéloprolifératifs et à la leucémie myéloïde, dont l’incidence augmente régulièrement avec l’âge (Verovskaya et al., 2019).
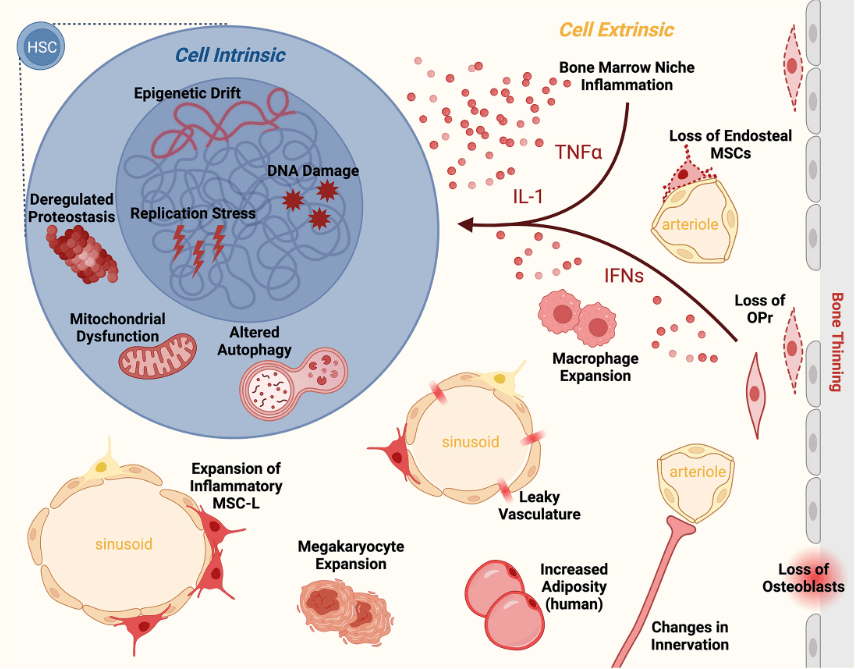
Une grande partie des HSC âgées présentent des niveaux d’autophagie diminués. L’autophagie est généralement associée au recyclage des organites, et l’autophagie altérée dans les HSC âgées entraîne l’accumulation de mitochondries, ce qui à son tour induit un stress métabolique. Des niveaux élevés d’espèces réactives de l’oxygène, générées par les mitochondries, s’accumulent dans les HSC et compromettent leur fonctionnement (Ito et al., 2006, Mohrin et al., 2016). Egalement, une exposition chronique à des PAMP (Pathogen Associated Molecular Patterns) tels que le LPS (lipopolysaccharide de la paroi des bactéries Gram-) ou à des cytokines tels IL-1 peut accélérer le processus de perte de régénération et favoriser la différenciation au détriment de l’auto-renouvellement (Esplin et al., 2011, Pietras et al., 2016).
Certaines cellules immunitaires ne sont pas dérivées des HSC de la moelle osseuse, y compris chez l’adulte et se maintiennent indépendamment d’elles : c’est le cas des cellules microgliales du cerveau, des cellules de Langerhans dans la peau et des cellules de Kupffer dans le foie (Mirshekar et al., 2014), ainsi que d’une bonne partie des lymphocytes B de type B-1a dans les cavités pleurales et péritonéales et qui proviennent des phases embryonnaires de l’hématopoïèse et persistent chez l’adulte (Kobayashi et al., 2023).
Les cellules NK
Les cellules tueuses naturelles (NK) font partie du système immunitaire dit inné composé de cellules qui ne subissent pas de sélection clonale et de réarrangements génomiques contrairement aux lymphocytes B et T. Les cellules NK sont équipées d’une large gamme de récepteurs de surface activateurs ou inhibiteurs, leur permettant de reconnaître et de tuer les cellules tumorales ou infectées grâce à la cytotoxicité à médiation cellulaire dépendante des anticorps (ADCC). Elles détectent notamment les cellules qui présentent une expression trop basse du CMH de classe I (MHC-I), ce qui est le cas des cellules infectées par un virus ou de certaines cellules tumorales. Elles ont également un récepteur NKG2D qui reconnait le ligand NKG2D-L dont la présence à la surface des cellules est augmentée si elles sont infectées ou tumorales. Le virus SARS-CoV-2 (Covid-19) est capable d’échapper aux cellules NK en inhibant l’expression de NKG2D-L à la surface des cellules qu’il a infectées (Lee et al., 2022).
De plus, les cellules NK contribuent également à l’initiation et au développement de la réponse immunitaire adaptative, sécrétant plusieurs classes de cytokines, notamment l’IFN-γ pro-inflammatoire. Les cellules NK peuvent même maintenir une forme de mémoire immunologique (Bautista De Sanctis, 2022). La réponse fonctionnelle des cellules NK est précisément régulée par un équilibre entre les signaux d’activation et d’inhibition et par leur « éducation » au cours du développement.
Les cellules NK se développent à partir de cellules progénitrices lymphoïdes communes (CLP) dérivées de cellules souches hématopoïétiques CD34+. Les CLP sont les précurseurs communs des NK, des lymphocytes T et B et d’autres cellules lymphoïdes. Elles expriment différents marqueurs, notamment CD38, CD7, CD10, CD127 et CD122. L’expression de CD122 (IL-2Rβ/IL-15R) marque la détermination des CLP en cellules NK. Cette détermination dépend de l’expression de Eomesodermine et de T-bet (Daussy et al., 2014) ainsi que de Id2 qui réprime l’action des protéines E, notamment Socs3, E2A, E2-2 et HEB (en se dimérisant avec eux et en les empêchant de se fixer sur des séquences de type boîte E (CANNTG) sur l’ADN). Ces protéines auraient déterminé les cellules en lymphocytes B ou T. Id2 stimule aussi l’expression des récepteurs à l’IL-15 activant une voie de signalisation essentielle pour la survie des NK (Delconte et al., 2016). Cette voie maintient l’expression de la protéine anti-apoptotique MCL1 et inhibe l’expression de la protéine apoptotique BIM (Huntington et al., 2007).
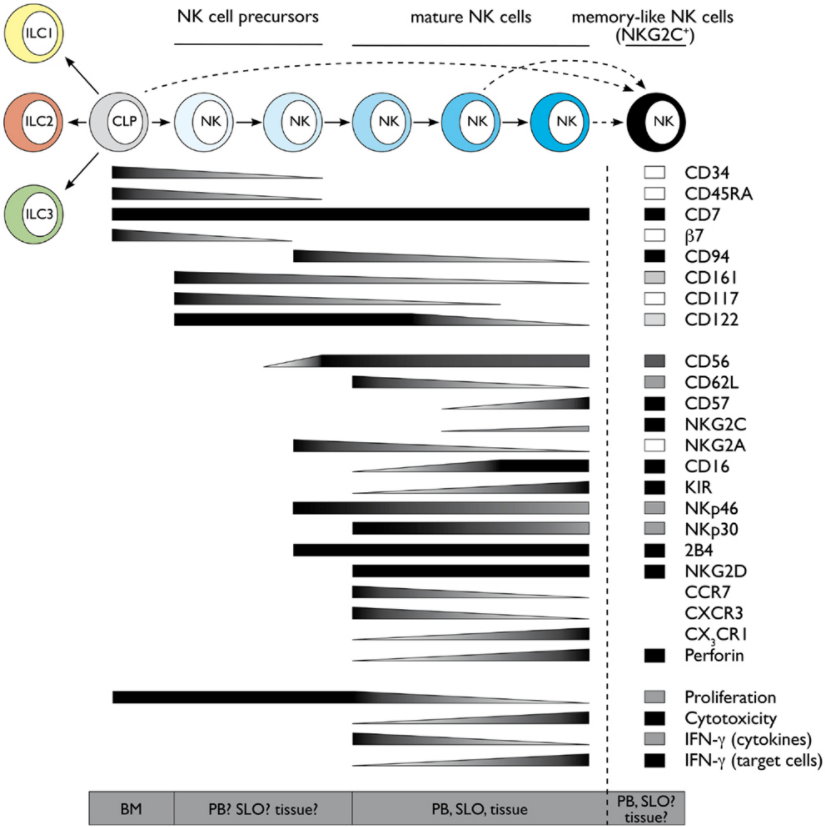
IL-15 joue un rôle crucial dans le contrôle de la prolifération et de la différenciation des cellules NK (Huntington et al., 2008).
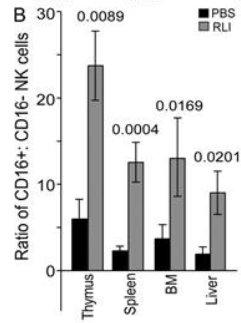
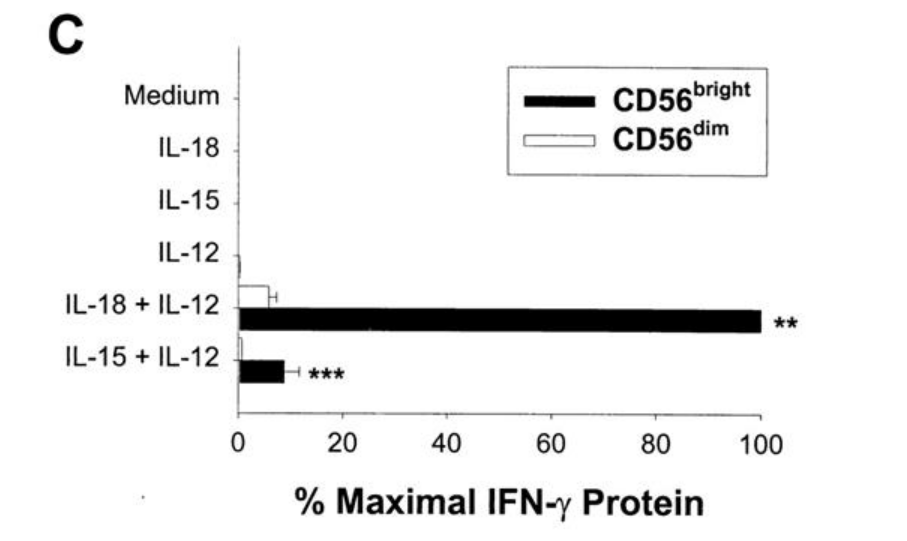
Lors des infections virales, l’activation des cellules NK cytotoxiques et sécrétoires est stimulée par des cytokines spécifiques dont l’expression est activée lors de la réplication virale. Par exemple, les interférons de type I (IFN-α/β), sécrétés par les cellules infectées, induisent la cytotoxicité des cellules NK dites à CD56 faible; l’expression d’IL-12 (interleukine-12) stimule la sécrétion d’IFN-γ (interféron-γ) par les cellules NK dites à CD56 fort mais il faut la présence concommitante d’IL-15 ou d’IL-18 (Fehninger et al., 1999).
L’IFN-γ peut activer plusieurs voies importantes associées à des fonctions antivirales directes et/ou des effets immunorégulateurs sur la réponse immunitaire en aval. Pendant ce temps, les cellules NK peuvent également produire du TNF-α qui médie les effets antiviraux et immunorégulateurs.
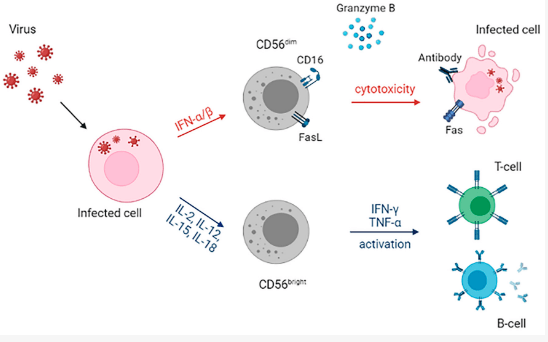
Les cellules NK peuvent agir comme un pont entre l’immunité innée et adaptative, car elles peuvent interagir avec les cellules T et B via leurs ligands costimulateurs, tels que CD40L et OX40L, qui favorisent la différenciation des cellules NK.
ADAM17 est une métalloprotéinase qui est capable de cliver CD16 de la surface des NK et ainsi de modérer leur activation (Romee et al., 2013). Des souris sans ADAM17 résistent mieux aux infections bactériennes.
Macrophages et monocytes
Il s’agit de cellules phagocytaires qui résident dans la majorité des tissus dont ils maintiennent l’homéostasie en éliminant les cellules mortes (par efferocytose) et les débris et dont ils assurent l’intégrité en éliminant les pathogènes. Ce sont à la fois des sentinelles et des effecteurs. Les macrophages sont des cellules très mobiles et émettent de longs prolongements qui explorent leur environnement. Outre leurs propriétés de phagocytose, ils peuvent aussi sécréter des facteurs angiogéniques (qui favorisent le développement des vaisseaux sanguins). L’identité et la fonction spécifiques d’un macrophage dépendent à la fois de son origine et des signaux qu’il reçoit du tissu où il est en résidence. Ces facteurs entraînent une large hétérogénéité de macrophages, souvent avec des réponses et des activités spécifiques aux tissus (Bleriot et al. 2020).
Les macrophages dans les tissus ont deux origines possibles : soit ils développent au cours du développement embryonnaire (notamment dans la vésicule vitelline ou sac vitellin), soit ils se développent plus tard à partir de monocytes issus de l’hématopoïèse dans la moelle osseuse. La première population se développe à E7,5-E8,5 chez la souris (Hoeffel et al., 2018). Certaines de ces cellules pénètrent dans le cerveau à E9,5 et deviennent des microglies. D’autres maturent en dehors du cerveau (devenant CD206+) mais certaines d’entre elles forment une deuxième population de microglies vers E12,5 après entrée dans le système nerveux via les ventricules cérébraux (et redeviennent CD206–) (Hattori et al., 2023). Ces macrophages se développent et se maintiennent indépendamment de la moelle osseuse, ce qui peut se montrer chez les souris mutantes perte-de-fonction pour le gène codant le facteur de transcription Myb qui est indispensable au développement des macrophages issus des monocytes mais par pour le développement des macrophages d’origine embryonnaire (Schulz et al., 2012). Selon les tissus, les proportions des macrophages des deux origines varient.
Les monocytes constituent une population hétérogène de cellules immunitaires innées circulant dans le sang, peuvent être recrutés à partir du système sanguin et se différencier en macrophages (Italiani et al., 2014). Les monocytes pro-inflammatoires classiques CD14+ (qui constituent 90% des monocytes) roulent le long des endothéliums activés avant leur émigration dans les sites des tissus en inflammation. Les monocytes non classiques CD16+ rampent constamment le long de l’endothélium vasculaire dans des conditions d’état d’équilibre. De ce fait, ils présentent un comportement de patrouille qui est essentiel pour leur rôle de piégeage des microparticules de la surface luminale des vaisseaux sanguins (Auffray et al. 2007, Carlin et al. 2013). Les monocytes qui n’ont pas été recrutés au bout de 2 jours environ meurent par apoptose.
Les étapes de détermination successives dans la moelle osseuse pour obtenir des monocytes et des macrophages comprennent les progéniteurs myéloïdes communs (CMP), les précurseurs des granulocytes-macrophages (GMP) et les progéniteurs des macrophages/cellules dendritiques (MDP). Le progéniteur déterminé des monocytes se reconnait à sa perte du marqueur CD135 (Hettinger et al., 2013).
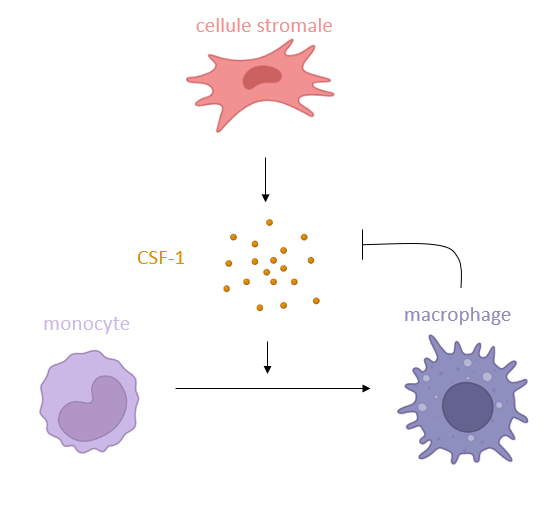
Le contrôle homéostatique du développement des monocytes/macrophages est principalement influencé par le CSF-1 (également connu sous le nom de M-CSF), produit par les cellules stromales dans les tissus. Les macrophages matures expriment à leur tour un excès de récepteurs du CSF-1 (CSF-1R) et éliminent le CSF-1 circulant, permettant une boucle de rétroaction qui cause d’une diminution de la prolifération des monocytes (Bartocci et al., 1987).
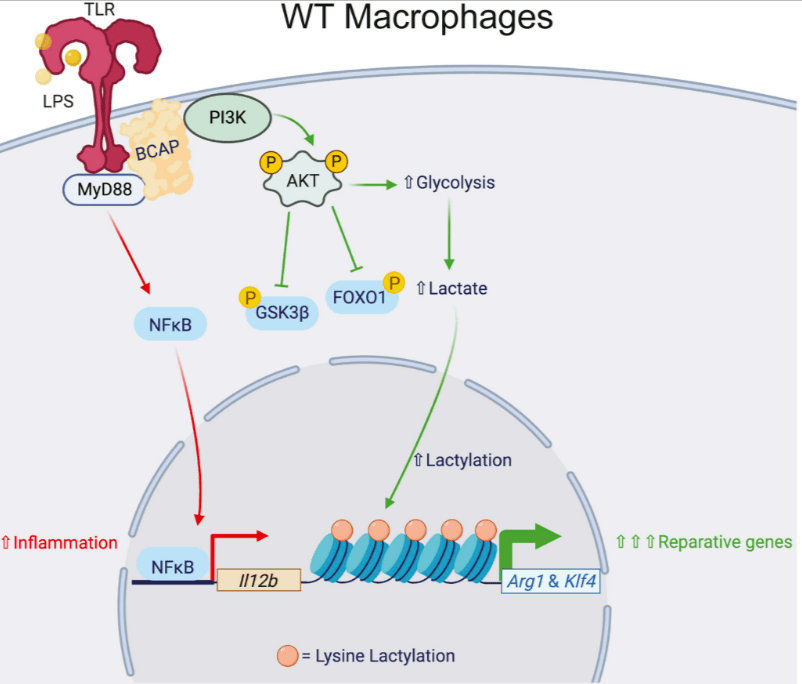
Les macrophages expriment un ensemble diversifié de récepteurs de type PRR (pour Pattern Recognition Receptors) qui reconnaissent des molécules « étrangères » (comme le LPS (LipoPolySaccharides) de la paroi des bactéries Gram-) qui leur permettent de déclencher une réponse inflammatoire appropriée (Fitzgerald et al., 2020). La stimulation de ces PRR, tels que les récepteurs de type Toll (TLR), conduit à l’activation des macrophages et à la production de cytokines pro-inflammatoires dépendantes de NF-κB et AP1 comme le TNF-α, l’IL-6 et l’IL-12.
Alors que dans un premier temps, les macrophages activés stimulent l’inflammation, ils modifient leur fonction pour limiter l’inflammation pendant la cicatrisation des plaies et se concentrent plutôt sur l’élimination des débris et l’assistance à une cicatrisation efficace (Das et al., 2015). Les macrophages dans cet état expriment des molécules telles que l’arginase-1 (ARG1) et Krüppel like factor-4 (KLF4), qui contribuent à leur fonction : ARG1 est une enzyme qui peut supprimer la formation d’oxyde nitrique et est nécessaire pour fournir des métabolites essentiels à une cicatrisation efficace des plaies, tandis que KLF4 est un facteur de transcription qui stimule l’expression d’ARG1 et d’autres gènes réparateurs, comme CD206 (Liao et al., 2011).
Les lymphocytes T
Les lymphocytes T sont des cellules du système immunitaire adaptatif qui combattent les menaces externes (infections) et internes (tumeurs).
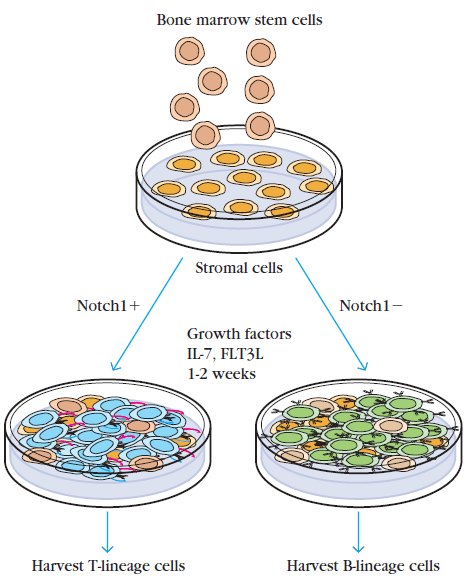
Tous les lymphocytes (B et T) naissent à partir d’un progéniteur lymphoïde commun dans la moelle osseuse. À ce stade, la cellule est multipotente et n’a pas encore acquis de caractéristiques propres aux cellules B ou T. Contrairement aux lymphocytes B, les lymphocytes T ne terminent pas leur maturation dans la moelle osseuse mais se déplacent via la circulation sanguine dans le thymus où ils trouvent un microenvironnement adéquat (notamment le ligand qui active la voie Notch nécessaire à la différenciation en lymphocyte T). Le thymus est ainsi considéré comme un organe lymphoïde primaire, tout comme la moelle osseuse. Si on fait artificiellement exprimé le ligand de la voie Notch dans des cellules stromales de moelle osseuse, on peut obtenir des lymphocytes T au détriment des lymphocytes B, de même si on exprime dans le progéniteur myéloïde commun une forme constitutivement activée de Notch. Des cytokines jouent un rôle d’accompagnement, notamment l’interleukine-7 (IL-7), sécrétée par le stroma thymique, qui soutient la prolifération et la survie des précurseurs T au cours de leur maturation.
Le thymus est nécessaire au bon développement des lymphocytes T comme le montre l’exemple des souris nude. Il s’agit d’une lignée comportant une délétion du gène Foxn1 qui aboutit à un thymus très malformé ou absent. Les souris ne présentent également presque pas de poils, ce qui explique leur nom. Elles n’ont pas de lymphocytes T et donc ne peuvent rejeter des greffes. Elles sont donc utilisées comme modèle pour des greffes de cellules humaines, notamment tumorales et le test de leur capacité à proliférer et à former des métastases.

Les lymphocytes T CD4+ et CD8+ expriment le récepteur des lymphocytes T (TCR) qui reconnaît les antigènes présentés par les cellules présentatrices d’antigène (APC) exprimant respectivement CMH‐II ou CMH‐I. Généralement, les molécules de CMH-II présentent des antigènes d’origine externe à la cellule présentatrice d’antigènes (dérivant de bactéries extracellulaires par exemple) et les molécules de CMH-I des antigènes d’origine interne (dérivant de bactéries internes ou de virus ou d’anomalies tumorales). Certaines exceptions ont été caractérisées : des lymphocytes T CD4+ peuvent exprimer des TCR qui reconnaissent des antigènes présentés sur du CMH-I et inversement des lymphocytes T CD8+ peuvent exprimer des TCR qui reconnaissent des antigènes présentés sur du CMH-II (Singh et al., 2022).
Les TCR sont très sélectifs et très sensibles : on estime qu’entre 1 et 10 exemplaire(s) de l’antigène est capable d’activer un lymphocyte T et avec une affinité à peine supérieure à des molécules qui ne suscitent pas ou peu de réponses des cellules (Sykulev et al., 1996; Huang et al., 2013).
La diversité des TCR présents à l’échelle de chaque individu est produite par des recombinaisons somatiques qui sont détaillées plus loin pour les BCR des lymphocytes B mais les principes généraux restent valables pour les TCR des lymphocytes B.
Au cours de leur développement, les lymphocytes T (tout comme les lymphocytes B) qui reconnaissent les molécules du CMH du soi sont conservés mais ceux qui reconnaissent en plus des antigènes du soi sont éliminés. Cette série de sélection a lieu dans le thymus pour les lymphocytes T encore immatures appelés thymocytes. Puis une fois cette étape terminée, les lymphocytes qui rencontrent l’antigène correspondant à leur récepteur TCR (pour les lymphocytes T) et BCR (pour les lymphocytes B) sont « activés » et font l’objet d’une sélection clonale positive qui mène à leur amplification par prolifération et à leur différenciation complète.
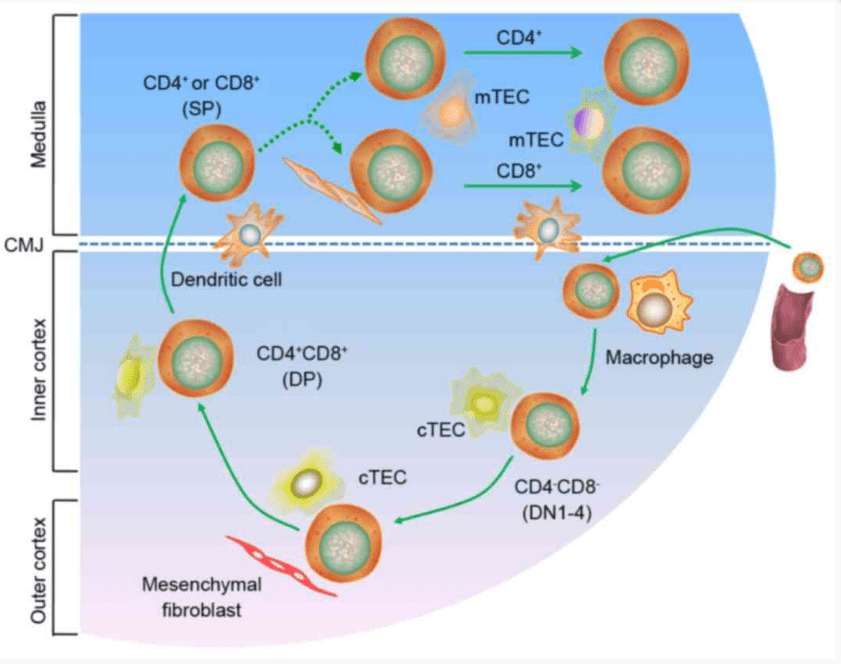
Les cellules du thymus créent un microenvironnement favorable à la sélection positive des lymphocytes T. Les cellules épithéliales du cortex thymique (cTEC) expriment par exemple des composants particuliers du protéasome ce qui leur permet de présenter sur leur CMHI des peptides différents de ceux habituellement présentés par les autres cellules. Ainsi, la sous-unité β5t du protéasome, qui n’est exprimé que dans les cTEC, est nécessaire à l’obtention de lymphocytes T CD8+ en quantité suffisante (Murata et al., 2007).
Des facteurs de transcription spécifiques orientent la différenciation des thymocytes vers un profil CD4+ ou CD8+. Par exemple, l’expression du facteur de transcription ThPOK favorise la différenciation en lymphocytes CD4+.
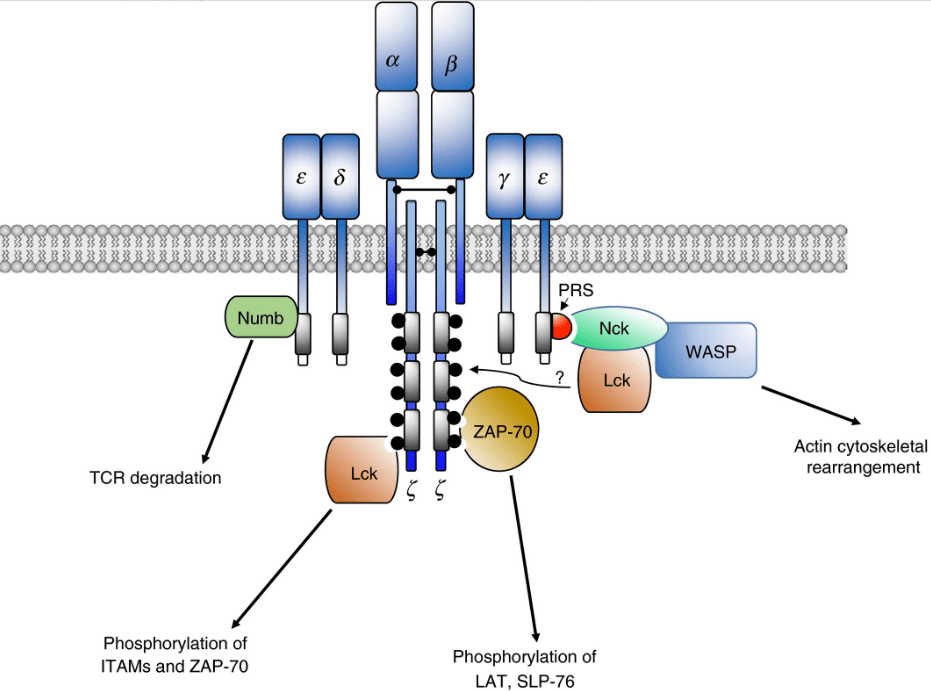
Les TCR sont composés de sous-unités αβ présentant des domaines variables de type immunoglobuline et sont associés au complexe CD3 formé par les sous-unités γ, δ, ε et ζ.
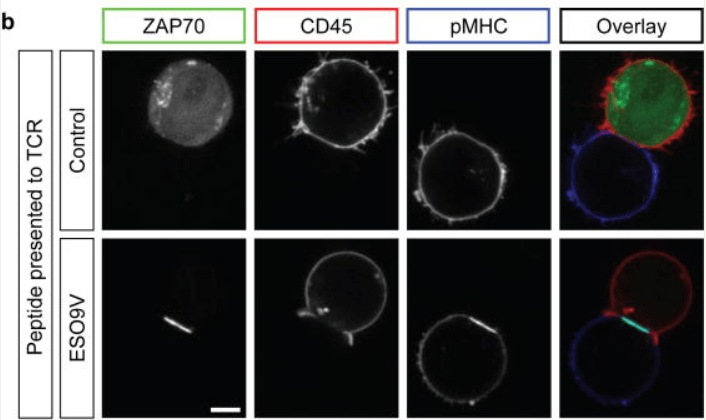
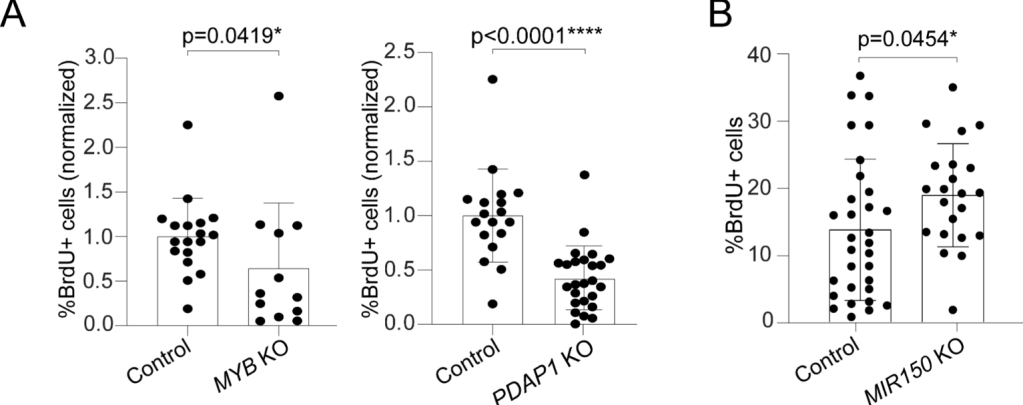
Lors de l’activation des lymphocytes T via le TCR des modifications importantes de l’expression des gènes ont lieu. Par exemple, l’expression du microARN miR-125b est diminuée alors qu’il a un rôle dans le maintien des lymphocytes T dans un état naïf (Rossi et al., 2011). Le microARN miR-150 voit son expression également diminuée en relation avec une baisse d’expression des facteurs de transcription RFX qui sont nécessaires pour son expression (Chiricella et al., 2022). Les cibles de ce microARN, MYB (un facteur de transcription) et PDAP1 (une protéine se liant à des ARN) voient logiquement leur expression augmenter lorsque les lymphocytes T sont activés. L’expression de MYB est nécessaire à la prolifération des lymphocytes T. L’expression de miR-150 est largement diminuée dans les lymphomes (Ito et al., 2014).
L’activation des cellules T auxiliaires naïves CD4+ nécessite la présentation de l’antigène par des cellules présentatrices d’antigène (APC) exprimant le CMH-II (les cellules dendritiques, les lymphocytes B et les macrophages), et aboutit à leur différenciation en plusieurs sous-ensembles effecteurs qui ont des fonctions spécifiques et complémentaires.
La différenciation dans chaque sous-ensemble T auxiliaire est principalement contrôlée par les cytokines présentes dans leur microenvironnement. Ces sous-ensembles d’auxiliaires CD4+ sont les suivants : Th1 sous l’influence de IL-12 ; Th2 sous l’influence de IL-4 ; Th9 sous l’influence de IL-4 et de TGF-β ; Th17 sous l’influence de IL-6 et de TGF-β ; Th22 sous l’influence de IL-6 et de IL-23 ; et Treg sous l’influence de TGF‐β et de IL‐2.
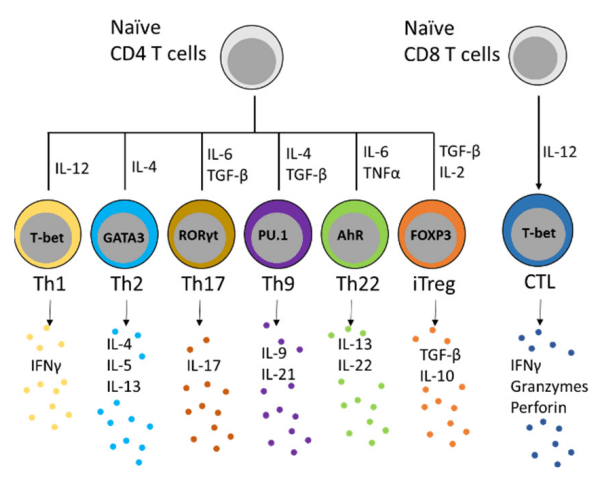
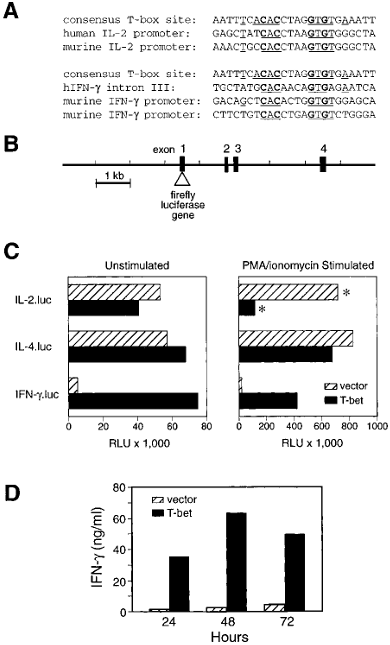
Les cytokines qui interviennent dans la différenciation des lymphocytes T auxiliaires activent les voies de signalisation en aval et conduisent à l’activation de l’expression d’un facteur de transcription maître. Chacun de ces facteurs maîtres de transcription est responsable de la définition des programmes de transcription pour chaque sous-ensemble T auxiliaire et affine l’expression des cytokines appropriées pour contrôler la réponse immunitaire. Par exemple, T-bet contrôle la différenciation des cellules Th1 en activant l’expression d’IFNγ tout en supprimant l’expression des cytokines typiques de Th2, tels que IL4 (Szabo et al., 2000).
Les lymphocytes T régulateurs (Treg) suppriment l’excès d’immunité contre les antigènes du soi et les antigènes dérivés des bactéries commensales. Comme les Th, ils expriment CD4 mais ils sont aussi caractérisées par l’expression du facteur de transcription Forkhead box P3 (Foxp3) (codé par un gène sur le chromosome X) qui joue un rôle crucial dans la différenciation, le maintien et la fonction des cellules Treg. Les patients et les modèles animaux qui ont des mutations perte-de-fonction dans Foxp3 succombent à des maladies autoimmunes (Bennett et al., 2001). Le microARN miR-142 est aussi essentiel à la fonction des cellules Treg (Wang et al., 2022).
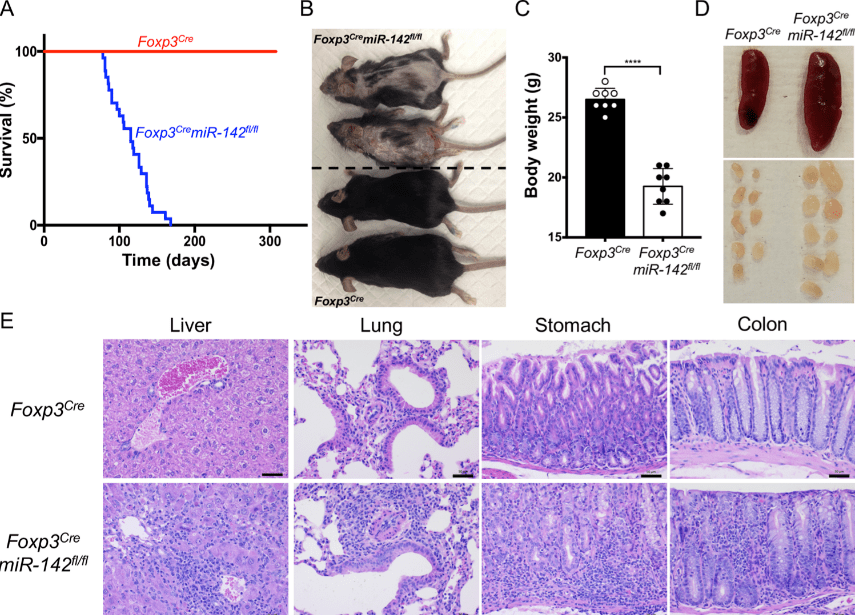
(A) Courbes de survie de Kaplan-Meier des souris Foxp3Cre et Foxp3Cre;miR-142fl/fl (B) Photographie de souris femelles Foxp3Cre (2 souris en bas) et Foxp3Cre;miR-142fl/fl (2 souris en haut) âgées de 14 semaines. Les souris Foxp3Cre;miR-142fl/fl sont plus petites et ont une dermatite sévère (C) Comparaison du poids corporel des souris Foxp3Cre et Foxp3Cre;miR-142fl/fl mâles âgées de 8 à 10 semaines . (D) Images représentatives de la rate et des ganglions lymphatiques périphériques de souris Foxp3Cre (à gauche) et Foxp3Cre;miR-142fl/fl (à droite). (E) Coloration hématoxyline-éosine de coupes de tissus du foie, des poumons, de l’estomac et du côlon de souris Foxp3Cre et Foxp3Cre;miR-142fl/fl. On observe une accumulation massive de leucocytes dans les tissus Foxp3Cre;miR-142fl/fl. Barre d’échelle = 50 μm. Source : https://journals.plos.org/plosbiology/article?id=10.1371/journal.pbio.3001552
Les lymphocytes Treg développés dans le thymus (tTreg) expriment le facteur de transcription Helios. Ils y sont sélectionnés selon leur forte avidité de leur TCR pour des antigènes du soi. Les lymphocytes tTreg subissent une différenciation supplémentaire en lymphocytes Treg effecteurs entièrement suppressifs en réponse aux signaux du récepteur de l’antigène des lymphocytes T (TCR) et des cytokines. Les lymphocytes Treg périphériques (pTreg) proviennent de lymphocytes T conventionnels CD4+Foxp3− naïfs à la périphérie lors de la stimulation antigénique avec une combinaison appropriée de cytokines telles que IL-2 et TGFβ. Les pTreg sont principalement présents dans l’intestin, notamment en raison de l’expression abondante de TGFβ et d’acide rétinoïque, et sont considérés comme particulièrement importants dans l’établissement de la tolérance au microbiote au niveau des sites muqueux. Une sous-population de pTreg est essentielle pour une bonne tolérance du placenta chez les mammifères placentaires. Le gène FoxD3 est activé par un enhancer particulier appelé CNS1 dans cette population (Samstein et al., 2012).
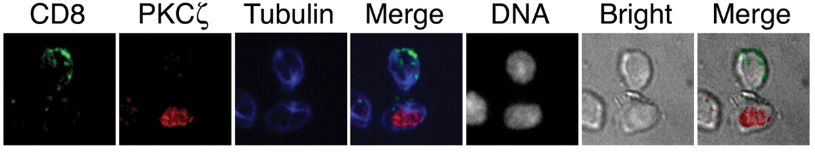
Les lymphocytes T CD8 répondent aux antigènes présentés sur les complexes protéiques du CMH de classe I et se différencient en lymphocytes T cytotoxiques (CTL) qui expriment des protéines cytolytiques (perforines, granzymes…) et interviennent directement dans l’élimination des cellules infectées par le virus et des cellules tumorales. Lors de la première division suivant la présentation de l’antigène, une division asymétrique permet de former un précurseur de CTL et un précurseur de lymphocytes T mémoire (Chang et al., 2007).
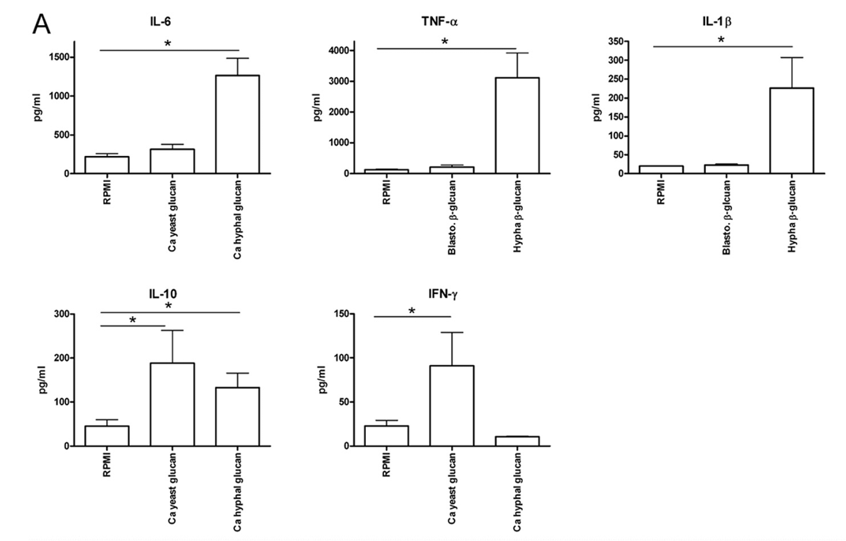
Les cellules dendritiques (CD) reconnaissent différentes morphologies de pathogènes comme C. albicans et différencient les sous-ensembles de cellules T auxiliaires (TH) adaptés au contexte pour orchestrer les réponses immunitaires (d’Ostiani et al., 2000; Kashem et al., 2015). Différentes morphologies de C. albicans stimulent différents récepteurs de reconnaissance de formes (PRR) sur les CD (Gantner et al., 2005; Lowman et al., 2014; Mukaremera et al., 2017), et différents sous-ensembles de CD induisent des sous-ensembles spécifiques de cellules TH (Igyarto et al., 2011 ; Kashem et al., 2015).
Suite à l’expansion puis à la fin des réponses des lymphocytes T, un pool élargi de cellules mémoires est capable d’initier des réponses puissantes à une infection secondaire grâce à une accessibilité accrue à la chromatine, à une production rapide de cytokines et à un potentiel prolifératif (Mueller et al., 2013). Les populations de lymphocytes T CD8+ mémoire se reconnaissent rapidement lors de l’expansion clonale à la suite de l’activation du TCR car elles expriment fortement le récepteur à l’IL-7 (CD127) et faiblement KLRG1. C’est l’inverse des lymphocytes T CD8+ qui vont mourir après la fin de la réponse primaire et qui dépendent d’IL-15 ce qui est insuffisant pour leur survie à long terme (Kaech et al., 2003). Le choix entre lymphocytes T mémoire ou « éphémères » dépend de la quantité d’IL-12 reçue durant leur développement ce qui se traduit par une expression plus ou moins forte du facteur de transcription T-bet , codé par le gène Tbx21 (fortement exprimé dans les lymphocytes T éphémères et faiblement exprimé dans les lymphocytes T mémoire) (Joshi et al., 2007).
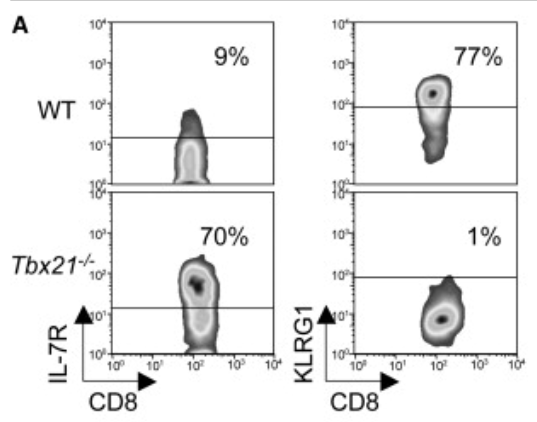
Les populations de lymphocytes T mémoire comprennent les lymphocytes T à mémoire effectrice (TEM) et à mémoire centrale (TCM) qui recirculent dans le sang et à travers les tissus (Masopust et Soerens, 2019). Les cellules T mémoire résidentes dans les tissus (TRM) se forment également dans de nombreux organes, notamment la peau, les poumons, les intestins, le foie et le cerveau (Mora-Buch et Bromley, 2020). Contrairement aux cellules TEM et TCM, les cellules TRM résident pendant de longues périodes, souvent de façon permanente, dans les tissus (Masopust et Soerens, 2019). Les cellules TRM expriment des marqueurs de surface distincts, dont CD69 et, dans des tissus tels que la peau, l’intégrine CD103 (ou intégrine αEβ7). Les cellules TRM diminuent l’expression du récepteur S1PR1 et du récepteur CCR7 qui sont nécessaires pour que les cellules sortent des tissus via les vaisseaux lymphatiques ce qui explique leur longue résidence dans les tissus (Casey et al., 2012; Mackay et al., 2013; Skon et al., 2013). Les cellules TRM peuvent fournir une protection supérieure par rapport au pool circulant de cellules T mémoire (Jiang et al., 2012; Shin et Iwasaki, 2012) et peuvent favoriser un état antiviral par production rapide de cytokines et de chimiokines qui recrutent des cellules immunitaires dans la circulation (Ariotti et al., 2014; Schenkel et al., 2014). La formation et le maintien des cellules TRM dans les tissus nécessitent une combinaison de signaux, notamment l’interleukine-15 (IL-15) et le facteur de croissance TGF-β (Hirai et al., 2021 ; Schenkel et al., 2016 ; Zhang et Bevan, 2013).
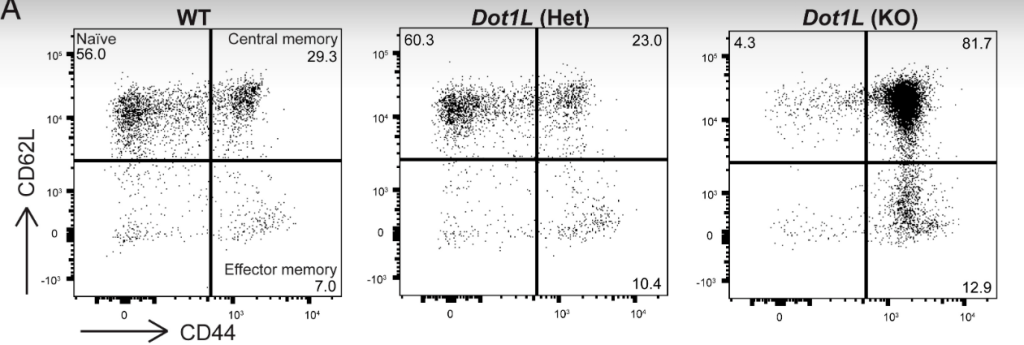
A l’inverse, des facteurs contrôlant la chromatine inhibent cette différenciation en lymphocytes T mémoire pour ne pas qu’elle se fasse trop précocement, avant la rencontre avec l’antigène. L’histone méthyltransférase DOT1L qui permet la triple méthylation de H3K79 (une marque épigénétique d’activation de la transcription) est nécessaire à ce contrôle (Kwesi-Maliepaard et al., 2020).
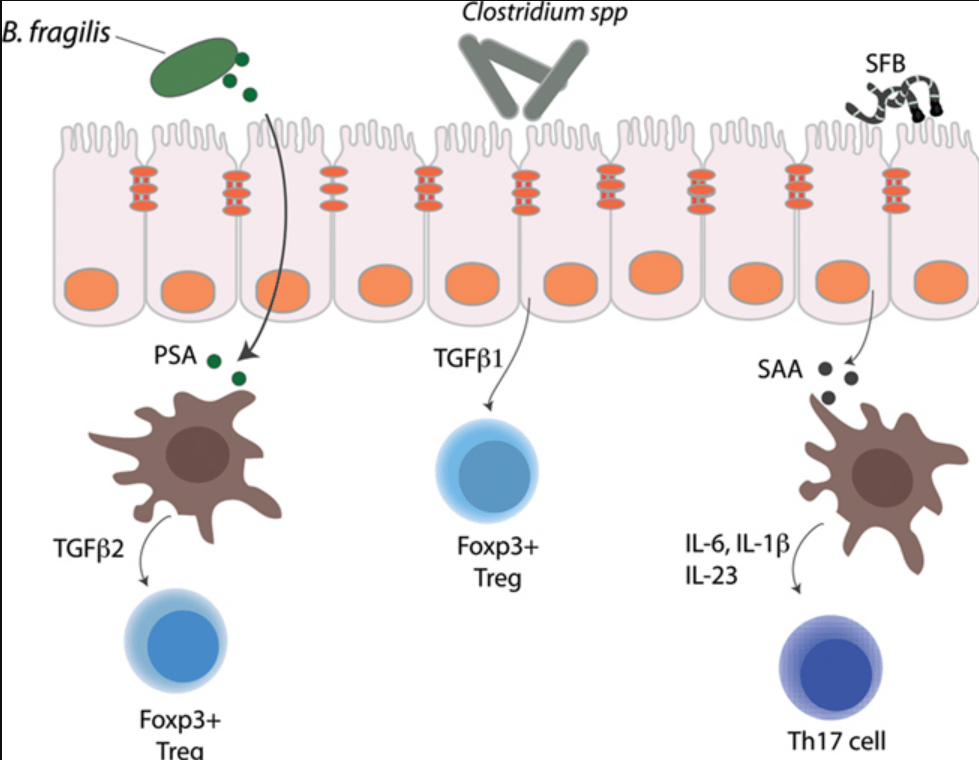
Le développement des lymphocytes T à proximité de l’intestin peut être influencé par le microbiote intestinal (Smith et Garrett, 2011). Bacteroides fragilis est un symbiote Gram négatif qui habite le tractus intestinal inférieur et colonise environ la moitié des humains. La monocolonisation des souris sans bactéries (GF) avec B. fragilis induit une expansion globale des lymphocytes T CD4 et une augmentation du nombre de cellules Th1 à des niveaux similaires à ceux des souris élevées normalement. L’effet de B. fragilis est entièrement dépendant d’un polysaccharide capsulaire zwitterionique, le polysaccharide A (PSA) (Mazmanian et al., 2005). L’exposition au PSA in vivo et in vitro est suffisante pour induire l’expansion des populations Th1 et la production de cytokines et les souris GF colonisées par B. fragilis dépourvues de PSA ne réussissent pas à corriger leur déséquilibre Th1/Th2. Les acides gras à courte chaîne telles l’acétate, le butyrate et le propionate produits par le métabolisme des microbiotes influence également le développement du système immunitaire intestinal.
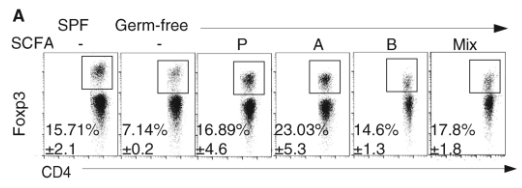
Trois acides gras à chaîne courte, l’acétate, le propionate et le butyrate (qui sont les principaux sous-produits générés par la fermentation bactérienne de polysaccharides d’origine végétale (tels que la cellulose) par le microbiote intestinal) régulent l’homéostasie des lymphocytes Treg dans le colon. Le nombre de Treg et leur sécrétion d’IL-10 est augmentée après un traitement in vitro avec les trois acides gras à chaîne courte ou après un traitement in vivo après que les bactéries Gram+ aient été préalablement détruites par un traitement antibiotique. L’effet des acides gras sur les lymphocytes Treg est médiée par le récepteur GPCR43 (Smith et al., 2013).
L’homéostasie du fer est un régulateur clé de l’immunité innée et adaptative et joue un rôle important dans les processus inflammatoires (Pereira et al., 2019). De nombreux types de cellules, notamment les macrophages et les cellules T, importent du fer pour soutenir leur développement et leurs fonctions effectrices. La privation de fer altère généralement l’activation des lymphocytes T, la sécrétion des cytokines et la prolifération (Wang et al., 2018; Yarosz et al. 2020). Par conséquent, la réduction des taux systémiques de fer est une approche fréquente et efficace pour traiter l’auto-immunité médiée par les lymphocytes T, par exemple pour les patients atteints de sclérose en plaques (Weigel et al., 2014).
Les lymphocytes B
Les lymphocytes B sont responsables de l’immunité humorale et de la production des anticorps. Ils présentent à leur membrane plasmique des récepteurs BCR spécifiques d’un antigène. Chaque lymphocyte B, produit dans la moelle osseuse, est spécifique à un antigène. La diversité énorme de ce répertoire à l’échelle d’un individu ne peut être codé directement par le génome mais résulte de recombinaisons génétiques dans chaque clone de lymphocytes B qui fait jouer une combinaison d’éléments génétiques. Ces recombinaisons sont qualifiées de somatiques pour les distinguer des recombinaisons dans les cellules germinales lors de la méiose.
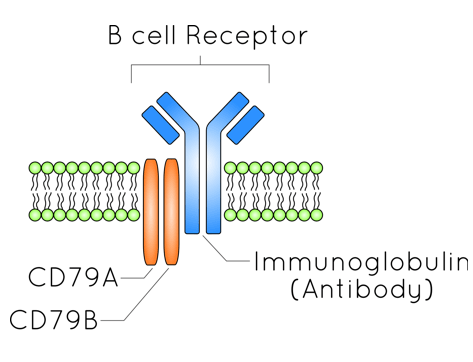
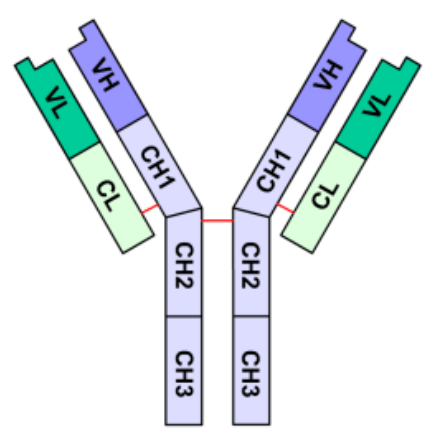
Les séquences codant le segment variable (V), le segment de diversité (D) et le segment de jonction (J) au sein de la région variable des anticorps sont représentées en de multiples exemplaires dans le génome et des réarrangements génomiques permettent de former une combinaison unique à chaque clone de lymphocyte au cours de leur maturation.
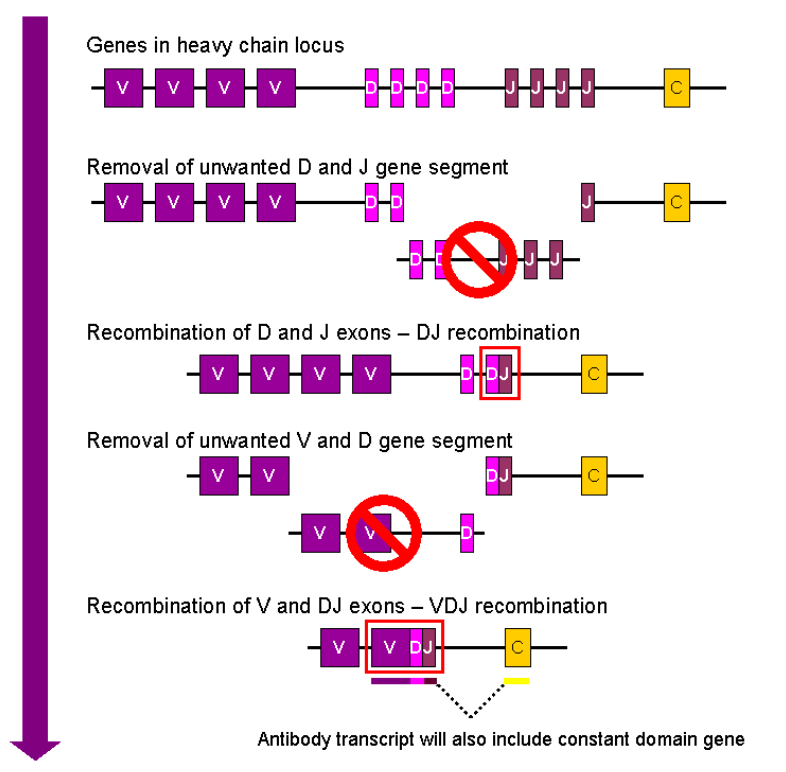
Les premières étapes de la recombinaison VDJ sont pris en charge par les recombinases RAG1 et RAG2 qui sont spécifiques des lymphocytes. Elles reconnaissent des séquences spécifiques à la fin de chaque segment V appelées RSS pour Recombination Signal Sequence.
Une fois qu’une recombinaison aboutit à la production d’une protéine fonctionnelle, le processus est arrêté sur l’autre chromosome homologue. Un seul allèle fonctionnel est donc présent par clone de lymphocytes et donc un seul antigène pourra être reconnu (malgré la diploïdie). C’est le phénomène d’exclusion allélique.
La différenciation des lymphocytes B est initiée par les facteurs de transcription E2A (un facteur de transcription hélice-boucle-hélice) et EBF, en l’absence desquels les cellules B sont arrêtées à un stade antérieur aux réarrangements DJ. Ensemble, ces gènes induisent la transcription de nombreux gènes spécifiques aux lymphocytes B, notamment celui codant Pax5. À partir du stade pro-lymphocyte B, Pax5 active l’expression de gènes tels que CD19 et blnk tout en inhibant l’expression des gènes « inappropriés » pour les lymphocytes B tels que M-CSFR (c-fms) et Notch-1. PU.1 est un facteur de transcription important pour le lignage des lymphocytes B et égalemement des macrophages car les souris déficientes dans ce gène codant cette protéine n’ont pas les deux lignées. Ce facteur de transcription est exprimé à des niveaux plus faibles dans les cellules B que dans les macrophages (DeKoter et Singh, 2000), et il a été impliqué dans les décisions de lignée lymphocyte B/Macrophage, car de faibles niveaux de PU.1 exprimés dans les précurseurs hépatiques fœtaux PU.1−/+ favorisent la différenciation des lymphocytes B, tandis que des niveaux élevés favorisent la différenciation des macrophages (DeKoter et Singh, 2000).
En présence d’antigènes et suffisamment stimulés par d’autres signaux, les lymphocytes B sont activés, prolifèrent et donnent naissance à des plasmocytes producteurs d’anticorps et à des lymphocytes B mémoire.
La liaison d’un antigène à un récepteur BCR active une cascade de signalisation à plusieurs branches qui aboutit à des changements importants dans le métabolisme cellulaire, l’organisation du cytosquelette, la migration et l’adhésion, la progression du cycle cellulaire et, finalement, cela aboutit à la différenciation en une cellule effectrice sécrétant des anticorps et un lymphocyte B mémoire (Treanor et al., 2012).
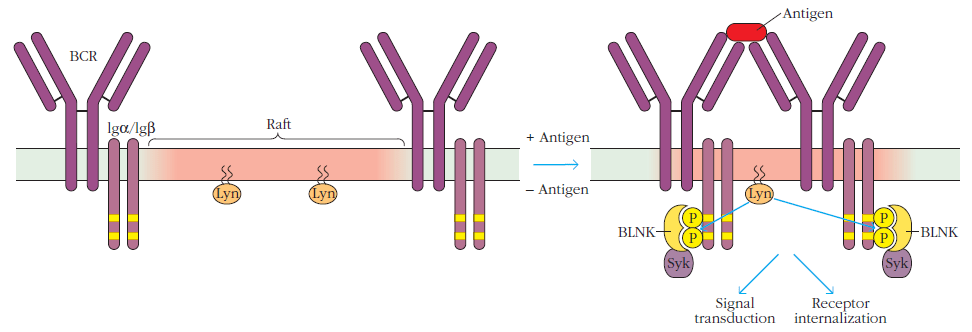
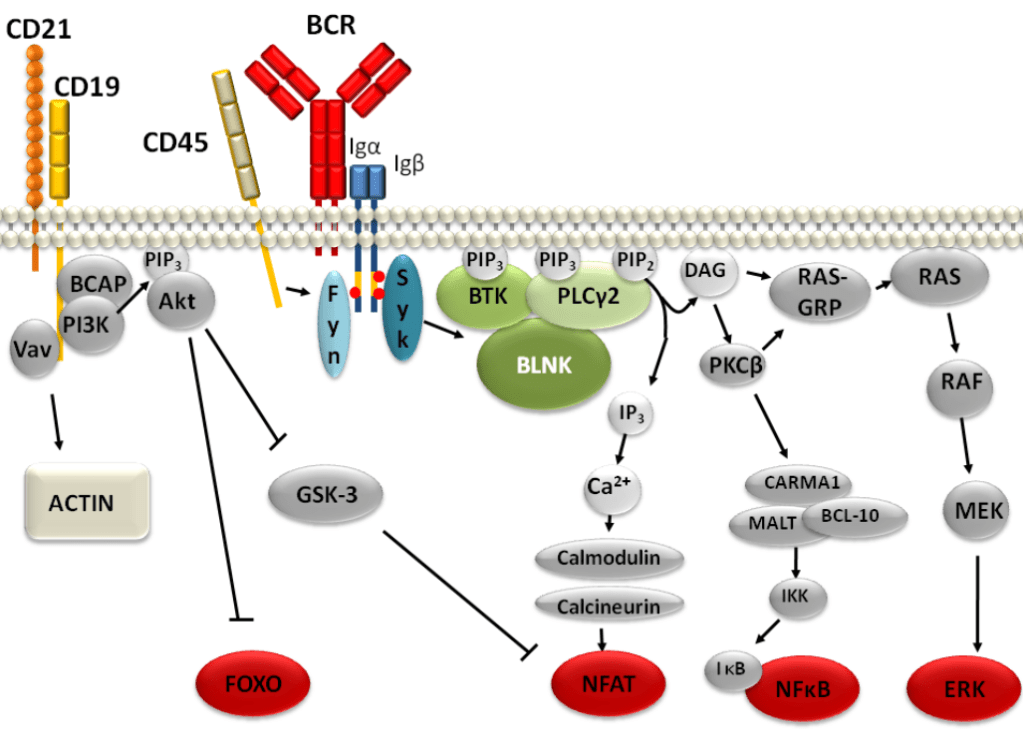
Signalons que le virus d’Epstein-Barr (qui infecte 95% de la population et qui peut causer la mononucléose) et qui reste dormant dans les lymphocytes B mémoire stimule la survie de ces lymphocytes grâce à la protéine d’origine virale LMP2A qui mime un BCR activé et stimule les voies de signalisation ERK/MAPK et PI3K (Merchant et al., 2001, Portis et al., 2004, Fish et al., 2020). LMP2A bloque cependant les autres voies activées par BCR.
Une signalisation BCR aberrante est associée à des dysfonctionnements des lymphocytes B. Par exemple, une signalisation BCR excessive est une caractéristique des maladies auto-immunes telles que la polyarthrite rhumatoïde ou le lupus érythémateux disséminé (Kristyanto et al., 2020, Lipsky, 2001). L’activation chronique de la signalisation BCR est également associée à diverses tumeurs malignes dérivées des lymphocytes B.
Dans la moelle osseuse, l’édition des récepteurs et la suppression clonale empêchent les cellules B immatures exprimant les récepteurs des cellules B (BCR) réactifs aux auto-antigènes locaux et systémiques de poursuivre leur développement. Cela constitue le point de contrôle central de la tolérance (Nemazee, 2017). L’étendue réduite des antigènes contre lesquels les cellules B en développement sont testées dans la moelle osseuse conduit à la survie et à la libération vers la périphérie de proportions élevées (≈20%) de cellules B matures, autoréactives et naïves (Wardemann et al., 2003). L’absence d’interaction avec des lymphocytes T auxiliaires apparentés et/ou la suppression par les lymphocytes T régulatrices FOXP3 + CD4 + (Treg) empêche l’activation de ces lymphocytes B naïves auto-réactives à la périphérie. Ce processus est connu sous le nom de « modèle à deux signaux » (Bretscher et Cohn, 1970). La fréquence des lymphocytes B naïfs autoréactifs est aussi limitée par des mécanismes cellulaires intrinsèques induits par l’exposition des lymphocytes B aux autoantigènes conduisant à une non-réactivité fonctionnelle (anergie).
L’activation des lymphocytes B naïfs avec un antigène apparenté combiné aux signaux des lymphocytes folliculaires auxiliaires (Tfh) CD4+ conduit au développement de plasmablastes qui sécrètent des anticorps, de cellules mémoire et de cellules B du centre germinatif (GC).
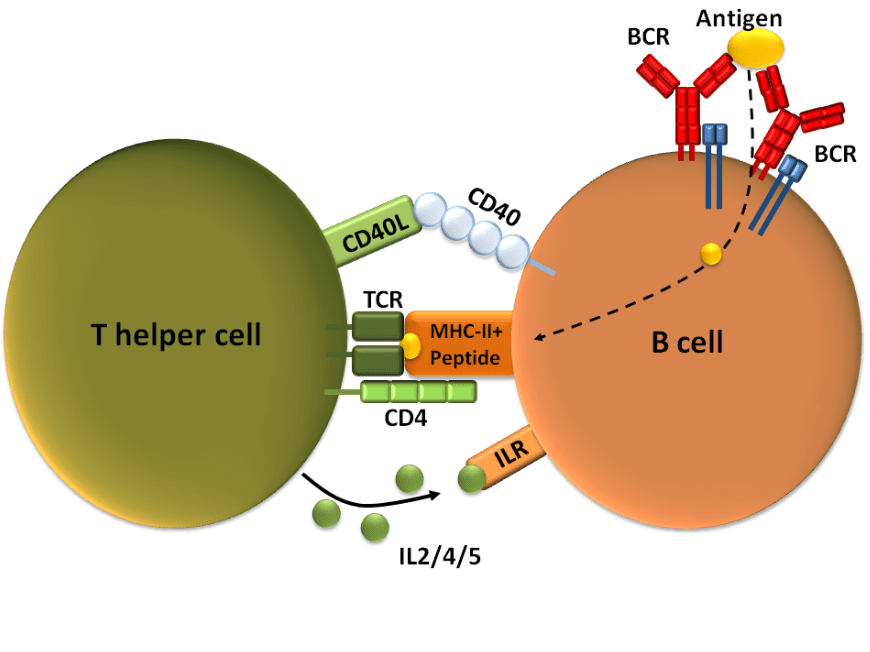
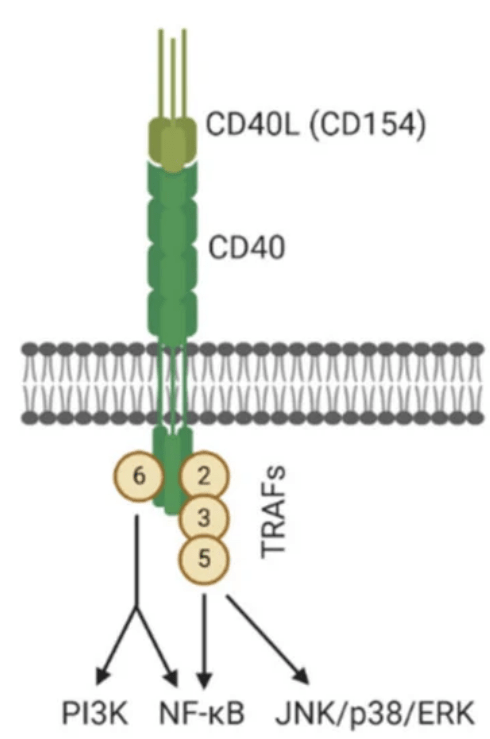
En règle générale, la première vague d’anticorps déclenchée contre un agent pathogène se compose d’immunoglobulines produites par les plasmablastes, des cellules à courte durée de vie. Il n’y a dans ce cas pas eu d’hypermutations somatiques et les immunoglobulines sont de faible affinité pour les antigènes (Elsner et Shlomchik, 2020). Les immunoglobulines M (IgM) et les cellules mémoire à longue durée de vie à commutation de classe apparaissent également aux premiers stades de la réponse (Good-Jacobson et Tarlinton, 2012; Weisel et al., 2016; Pritchard et Pepper, 2018). En parallèle, les lymphocytes B du centre germinatif se différencient en des sous-ensembles de lymphocytes B à prolifération rapide et forment des amas de cellules au centre du follicule ganglionnaire 5 à 7 jours après l’exposition à la stimulation immunitaire.
Les centres germinatifs (GC) de la rate, des ganglions lymphatiques ou des plaques de Peyer (dans la paroi intestinale) sont des lieux essentiels dans la production de plasmocytes (les lymphocytes B producteurs d’anticorps à haute affinité et à longue durée de vie) et de lymphocytes B mémoire qui peuvent ensuite rester des années voire des décennies en quiescence avant d’être stimulés par une nouvelle rencontre avec l’antigène (cela constitue alors la réponse immunitaire secondaire) (Victora et Nussenzweig, 2022).
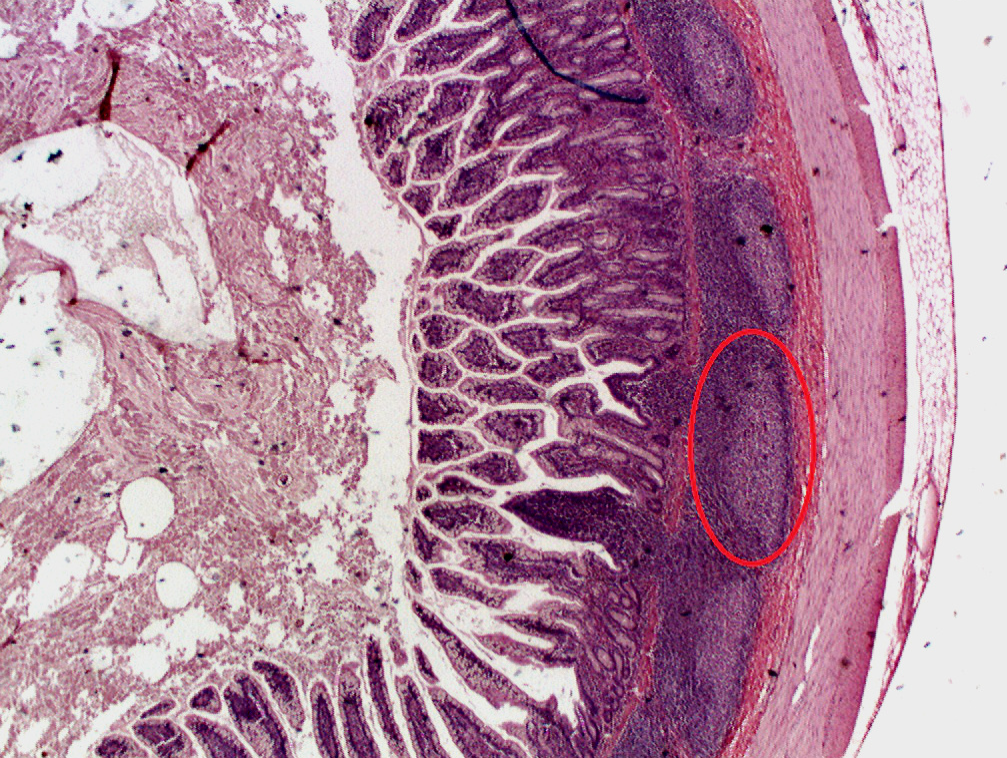
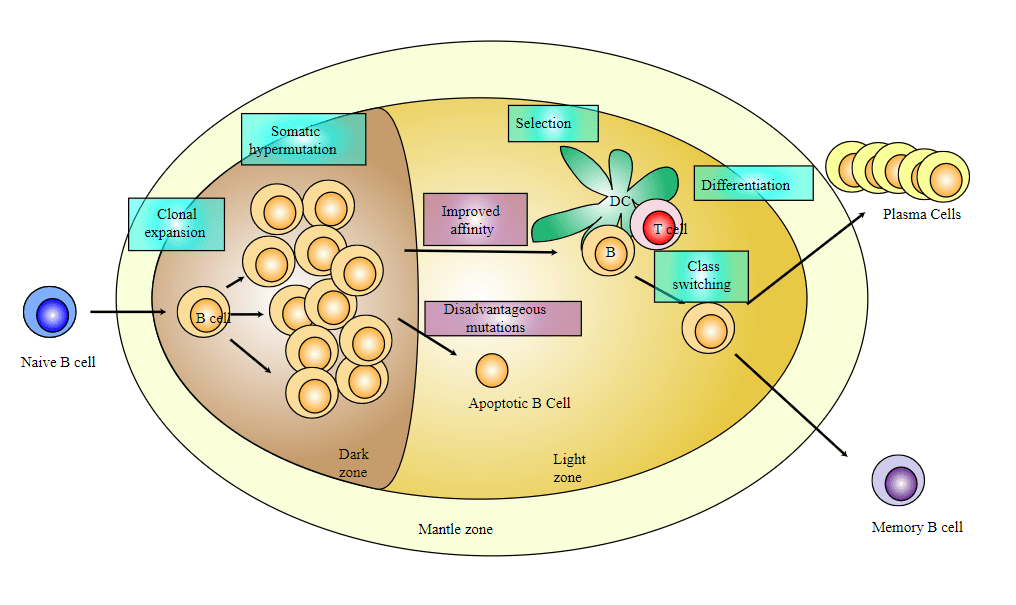
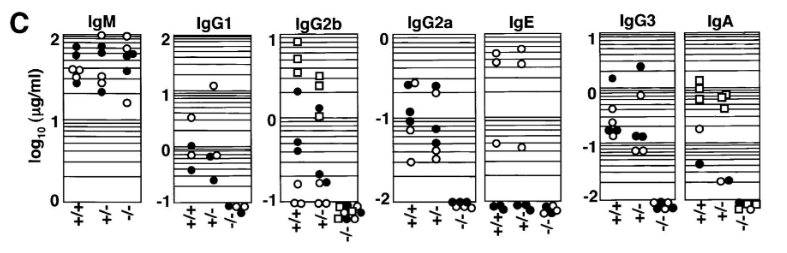
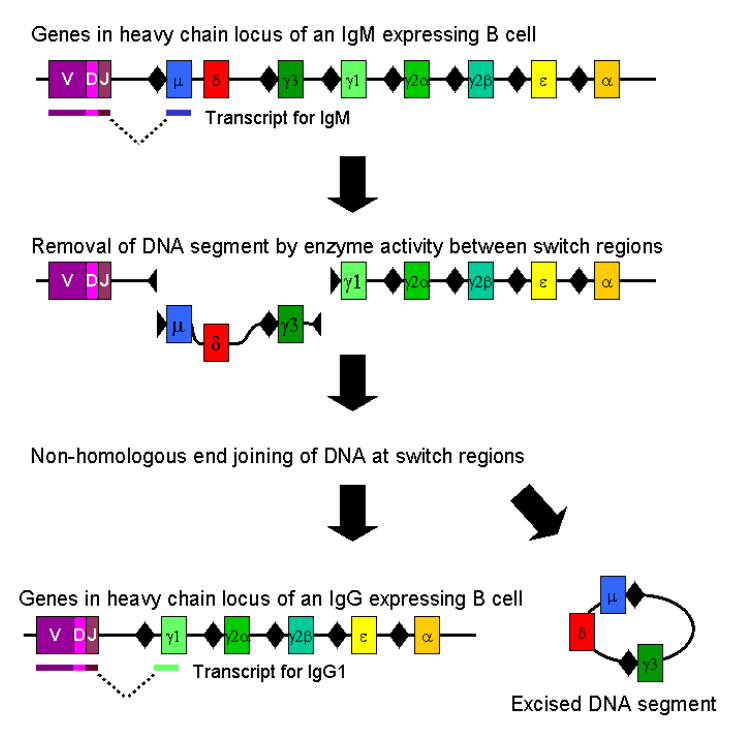
La maturation d’affinité des lymphocytes B se produit par l’acquisition aléatoire d’hypermutations somatiques dans leurs BCR. L’enzyme cytidine désaminase (AID) induite par l’activation régule ce processus (Muramatsu et al., 2000; Revy et al., 2000). Indépendamment de son activité mutationnelle, AID est également essentielle pour la commutation de classe d’immunoglobuline par recombinaison (CSR) (Shinkura et al., 2004). En effet, les lymphocytes B expriment d’abord des immunoglobulines (Ig) de type M liées à la membrane, mais d’autres types d’Ig sont plus efficaces pour neutraliser les pathogènes, notamment des formes secrétées. Il existe en tout 5 classes principales d’Ig chez les Mammifères : IgA, IgD, IgE, IgG et IgM, chacune avec des propriétés particulières. Il s’agit alors de changer de types d’Ig sans changer le site de reconnaissance spécifique de l’antigène.
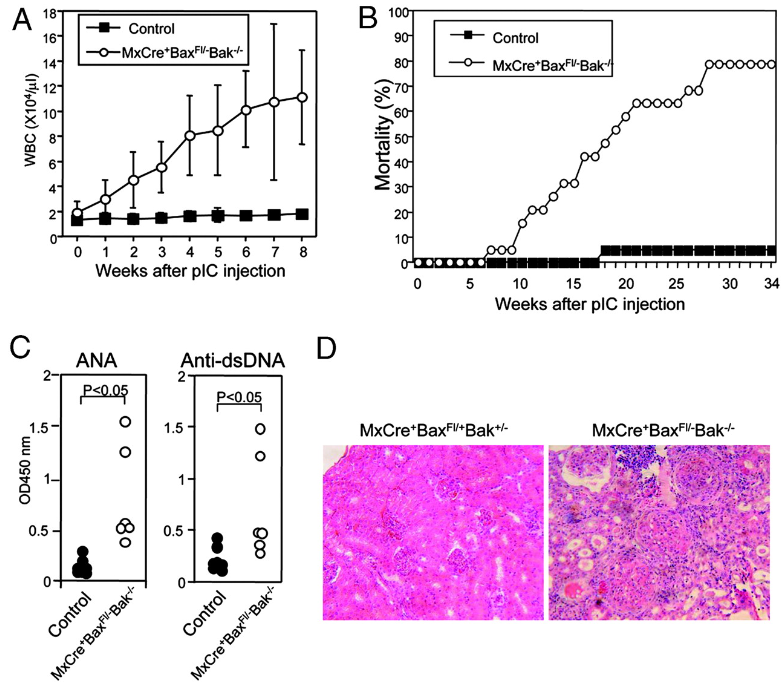
Les hypermutations somatiques peuvent entraîner une baisse de l’affinité pour l’antigène et cela aboutit à des lymphocytes B qui ne vont plus être stimulés et qui meurent par apoptose. Il peut aussi y avoir émergence d’une auto-réactivité (Tiller et al., 2007), qui est contrôlée par apoptose par un point de contrôle de tolérance périphérique supplémentaire qui évite la sélection de cellules auto-réactives. L’inhibition de l’apoptose dépendante de Bax et Bak conduit à une auto-immunité avec développement d’auto-anticorps (Takeuchi et al., 2005).
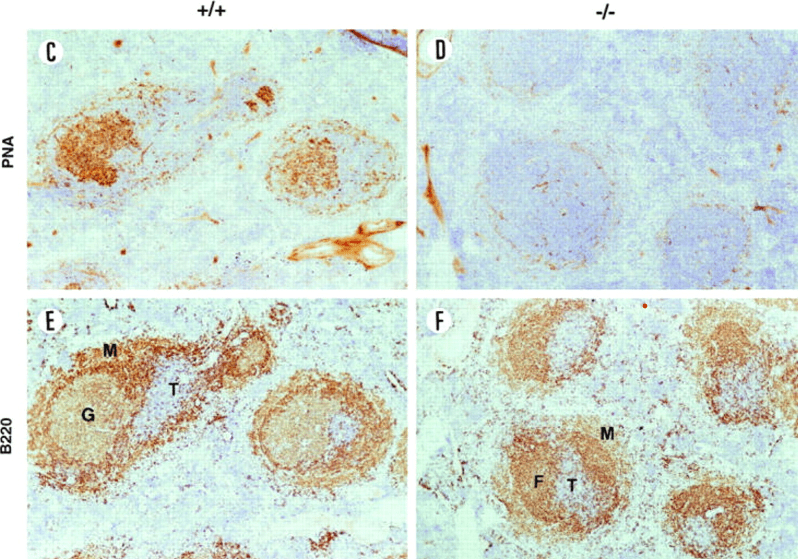
Enfin, la sélection des cellules B avec des BCR de haute affinité nécessite une migration alternée de la zone sombre (DZ) vers la zone claire (LZ) du centre germinatif régulée par une série de processus cellulaires dépendants de l’actine (chimiotactisme, endocytose des BCR, formation de synapses immunitaires, recyclage du complexe majeur d’histocompatibilité (CMH) de classe II). L’importance de ces processus est mise en évidence par le nombre croissant de déficiences génétiques liées à l’actine associées à une sélection défectueuse des lymphocytes B dans les centres germinatifs (He et Westerberg, 2019).

Parmi ces troubles figure le syndrome de Wiskott-Aldrich (WAS), une maladie rare liée à l’X présentant une thrombocytopénie et une susceptibilité variable à l’eczéma, aux infections récurrentes, à l’auto-immunité et au cancer (Candotti, 2018). Le WAS est causé par une déficience génétique de la protéine WAS (WASp), le membre fondateur d’une famille de facteurs favorisant la nucléation de l’actine qui traduisent les signaux de surface en polymérisation de l’actine via le complexe Arp2/3 lié à l’actine (Kelly et al., 2006).
La contribution spécifique des lymphocytes B à l’auto-immunité dans WAS a été étudiée avec des modèles murins knock-out conditionnels précoces dans lesquels le gène WASp est supprimé dans les précurseurs des lymphocytes B de la moelle osseuse (Recher et al., 2012). Ces expériences ont montré que les défauts intrinsèques des lymphocytes B déficientes en WASp entraînent le développement d’auto-anticorps et d’une auto-immunité qui sont en corrélation avec une fréquence plus élevée de développement incontrôlé dans les centres germinatifs (Recher et al., 2012; Becker-Herman et al., 2011).
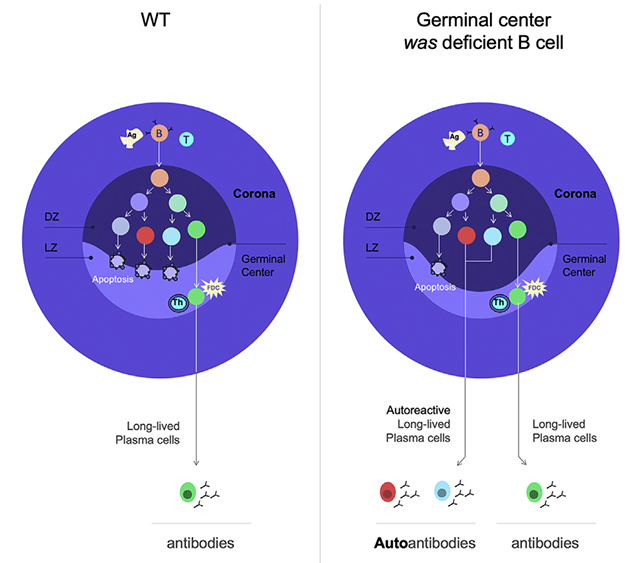
Les cellules B défectueuses en WASp acquièrent une auto-réactivité lors de la réaction du centre germinal. Source : https://www.cell.com/cell-reports/fulltext/S2211-1247(22)00207-8
BCL6 est un facteur de transcription clé dans le développement des lymphocytes B dans les centres germinatifs (Fukuda et al., 1997). EWSR1 est un facteur de transcription qui peut ralentir la prolifération et la maturation des lymphocytes B et la production des anticorps de type IgG en inhibant l’expression de BCL6 (Li et al., 2023). EWSR1 joue ainsi un rôle de modulateur de la réponse immunitaire : il est normalement inactif car associé dans un complexe avec TRAF3. Lorsque le lymphocyte B est activé, TRAF3 est dégradé et EWSR1 peut rentrer dans le noyau et diminuer l’expression de BCL6.
Les structures du centre germinatif persistent pendant plusieurs semaines à plusieurs mois, selon la nature de l’agent pathogène ou de la vaccination, et génèrent une mémoire de longue durée et des plasmocytes qui portent généralement des immunoglobulines issues des hypermutations somatiques et de haute affinité pour les antigènes (Victora et Nussenzweig, 2012). La régulation de la dichotomie développementale entre les cellules B des centres germinatifs et les cellules sécrétant des anticorps est très étudiée (Tellier et Nutt, 2019).
Les lymphocytes B peuvent maturer et proliférer indépendamment des lymphocytes Th. Dans ce cas, un acteur essentiel est le récepteur TACI qui est un membre de la superfamille des récepteurs du TNF qui lie les ligands BAFF et APRIL (un ligand induisant la prolifération) (Bodmer et al., 2002, Mackay et Schneider, 2009). Il est exprimé par les lymphocytes B humains activés, les lymphocytes B de la zone marginale, les lymphocytes B à mémoire commutée et les plasmocytes. Après la liaison des ligands, le domaine intracellulaire de TACI interagit avec des molécules de signalisation qui aboutissent à activer NFAT et NF-kB. Cela induit une recombinaison et une différenciation par commutation de classe dans les plasmocytes (Salzer et al., 2005). Des mutations pertes de fonction dans le gène codant TACI chez des patients humains provoquent des immunodéficiences, tandis qu’une surexpression du ligand BAFF est à l’origine de certaines de lupus érythémateux systémique, une maladie auto-immune (Stohl et al., 2003). TACI peut aussi être clivé par ADAM10, libérant une forme de récepteur leurre soluble (sTACI) qui peut neutraliser les ligands BAFF et APRIL (Hoffmann et al., 2015). Le nombre élevé de lymphocytes B chez les souris Taci-/- peut ainsi s’expliquer par le manque d’activité de leurre sTACI (von Bülow et al., 2001). Ainsi, en régulant la disponibilité et la force des signaux de survie induits par BAFF, TACI peut contrôler la taille des populations de lymphocytes B.
FOCUS SUR LA SYNAPSE IMMUNITAIRE
Les synapses immunitaires peuvent mettre en jeu des lymphocytes B ou des lymphocytes T. Ici, nous nous concentrons sur celles impliquant des lymphocytes B.
L’interaction du récepteur des cellules B (BCR) avec l’antigène apparenté présenté par une cellule présentatrice d’antigène (CPA) déclenche des changements importants dans la physiologie des cellules B qui favorisent leur activation, la formation de la synapse immunitaire (SI) et les fonctions effectrices des cellules B (Harwood et Batista, 2011). La SI permet l’échange d’informations entre les deux cellules par le biais d’événements exocytaires et endocytaires étroitement régulés (Griffiths et al., 2010). La signalisation et le trafic au niveau de la SI nécessitent des réarrangements profonds des microfilaments d’actine et des microtubules. L’actine contrôle l’organisation des microclusters contenant des récepteurs d’antigènes ce qui permet la coordination entre le trafic et la signalisation et aide en outre à générer les forces mécaniques qui dépendent de la myosine II (Treanor et al., 2011; Kumari et al., 2019; Bolger-Munro et al., 2019).
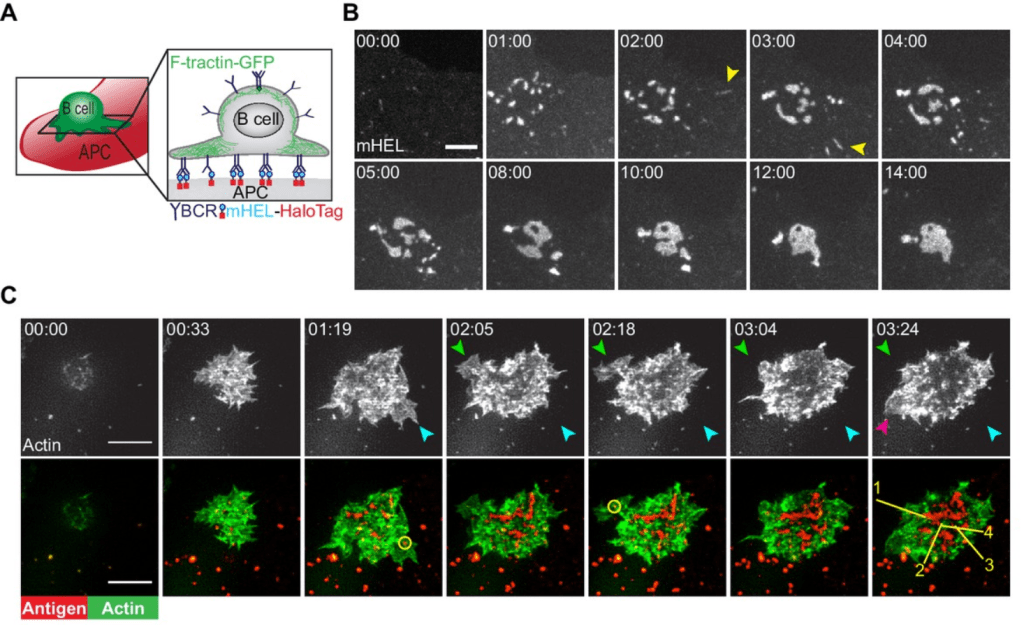
La SI active un assemblage dynamique des microfilaments initié par la formation d’un réseau d’actine ramifié dépendant du complexe Arp2/3 au bord externe de la SI (Wang et Hammer, 2020; Song et al., 2014). Ce réseau d’actine de type lamellipode entraîne l’étalement de la cellule B sur la surface recouverte d’antigène, favorisant ainsi les interactions BCR/antigène. Un flux centripète ou rétrograde d’actine entraîne ensuite une clusterisation des complexes BCR/ antigène vers le centre de la SI (Mattila et al. , 2016). Ce processus de centralisation de l’antigène est nécessaire pour une signalisation BCR robuste et est considéré comme une condition préalable à l’internalisation de l’antigène par les cellules B folliculaires (Yuseff et al., 2013; Yuseff et Lennon-Duménil, 2015). L’intégrine des lymphocytes B, LFA-1, qui lie la molécule d’adhésion ICAM-1 présente à la surface des APC sert de co-signal de stimulation (Carrasco et al., 2004).
Quant à eux, les microtubules contrôlent le recrutement des vésicules au niveau de la synapse immunitaire. Cela repose sur la réorientation du centrosome, conduisant à la rupture de la symétrie des lymphocytes et à l’acquisition d’un état cellulaire polarisé (Yuseff et al., 2013).
Les cellules présentatrices d’antigène (APC) telles que les lymphocytes B expriment CD74 qui fonctionne de manière intracellulaire comme un chaperon pour les molécules du complexe majeur d’histocompatibilité (MHC) de classe II (Stumptner-Cuvelette et Benaroch, 2002). Une petite proportion de CD74 subit des modifications post-traductionnelles par l’ajout de sulfate de chondroïtine (CD74-CS), et cette forme de CD74 est dirigée vers la membrane plasmique (Naujokas et al., 1993). Les ligands naturels du CD74 sont des membres de la superfamille des cytokines du facteur inhibiteur de la migration des macrophages (MIF) (Leng et al., 2003), qui se lient au CD74 pour induire la formation d’un complexe avec CD44. Ce complexe de récepteurs est essentiel pour l’initiation d’une cascade de signalisation nécessaire à la régulation du maintien des lymphocytes B (Gore et al., 2008; Shi et al., 2006) via l’activation de la voie PI3K/AKT. Le complexe est internalisé dans les compartiments endocytaires où il est clivé, libérant le fragment de domaine intracellulaire CD74 (CD74-ICD). CD74-ICD se transloque dans le noyau, où il induit la phosphorylation du domaine d’activation p65 du facteur nucléaire κB (NF-κB) et, avec son co-activateur, augmente l’expression de TAp63.
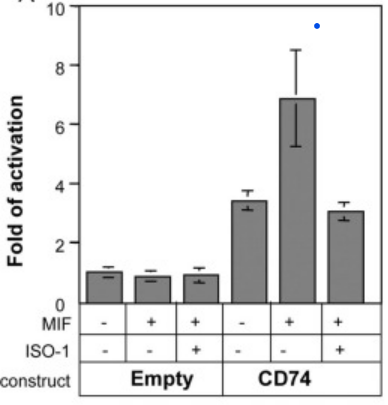
Ces événements cellulaires induisent une augmentation des niveaux d’expression de BCL-2 (protéine anti-apoptotique) et entraînent une régulation transcriptionnelle des gènes qui contrôlent la prolifération et la survie des cellules B (Gore et al., 2008; Lantner et al., 2007; Starlets et al., 2006).
Les leucémies et les myélomes
La leucémie est le terme désignant les tumeurs des cellules sanguines. Il existe de nombreux types de leucémie, qui sont classés comme aigus ou chroniques, et selon le type de cellules anormales produites, et selon l’âge d’apparitions des symptômes (enfant ou adulte). En général, la leucémie se caractérise par une surproduction de globules blancs immatures. Ces cellules ne peuvent pas remplir leurs fonctions normales, et le patient devient très sensible aux infections. Comme une plus grande proportion de cellules et de nutriments sont utilisés par les cellules tumorales, la production des autres cellules sanguines diminue entraînant un déséquilibre dans l’hématopoïèse. Une anémie sévère est une conséquence de la diminution de la production de globules rouges, et la tendance à l’hémorragie est le résultat
de la diminution du nombre de plaquettes.
La leucémie myéloïde aiguë (LMA) est la leucémie aiguë la plus courante chez l’adulte et survient de plus en plus avec l’âge avec des conséquences dévastatrices. La LMA est initiée et entretenue par un petit nombre de cellules souches leucémiques (LSC) qui s’auto-renouvellent. La thérapie conventionnelle peut détruire la majeure partie des cellules leucémiques, mais ne parvient pas à éliminer les LSC, qui peuvent initier à nouveau une tumeur après une période de latence. Les chercheurs souhaitent donc identifier et cibler des molécules-clés qui régulent spécifiquement l’auto-renouvellement des cellules souches des LMA.
Les myélomes dits multiples sont causés par une prolifération incontrôlée des lymphocytes B produisant des anticorps (les plasmocytes). Ils ne sont classiquement pas considérés comme faisant partie des leucémies, car les cellules proliférantes gardent des caractères partiellement différenciés. On peut observer une immunoglobulémie élevée d’anticorps monoclonaux correspondant au clone dont l’amplification n’est plus contrôlée. Par rétrocontrôle, la production des autres cellules sanguines est partiellement inhibée, pouvant causer des anémies et une protection immunitaire moins efficace contre des antigènes non reconnus par le clone affecté. Ces cellules tumorales secrètent aussi des molécules (notamment IL6) qui stimulent les ostéoclastes qui déminéralisent la matrice extracellulaire osseuse qui provoque des douleurs et des fragilités osseuses, ainsi qu’une hypercalcémie. L’exposition à des radiations ou à des pesticides comme le chlordecone (utilisé pour protéger les bananes dans les Antilles) est un facteur à risque important. Des études épigénétiques ont montré que les cellules tumorales ont un profil rappelant les cellules souches indifférenciées plutôt que des cellules différenciées telles que des plasmocytes normaux (Agirre et al., 2015). Les patients ont souvent des translocations impliquant des fragments du chromosome 14.
QUELQUES EQUIPES FRANCOPHONES QUI TRAVAILLENT SUR LE SUJET :
Approches quantitatives en immuno-hématologie – Institut Curie (Paris)
Biologie des leucémies de l’enfant – Institut Gustave Roussy (Villejuif)
Cellules souches et biologie des macrophages – Centre d’Immunologie de Marseille-Luminy
Cancer et âge (sur les leucémies) – Institut d’Oncologie de Bordeaux
- Adhérences cellule-cellule
- Arabidopsis thaliana
- Axe antéro-postérieur chez la drosophile
- Biomécanique du développement
- Caenorhabditis elegans
- Concepts principaux
- Contrôle de la traduction
- Contrôle de la transcription
- Contrôle génétique et épigénétique
- Croissance du tube pollinique et double fécondation chez les Angiospermes
- Croissance et guidage axonal
- Des modèles animaux moins classiques
- Développement de l’oeil des Vertébrés
- Développement et évolution
- Et l’Humain ?
- Exercices sur l’ovogenèse, la spermatogenèse et la fécondation
- Exercices sur le contrôle de l’expression des gènes
- Exercices sur le développement des bourgeons de membre
- Exercices sur le développement des muscles striés squelettiques
- Exercices sur le développement des végétaux et les hormones végétales
- Exercices sur les cycles et les divisions cellulaires
- Exercices sur les étapes du développement, les inductions embryonnaires et la mise en place des axes de polarité
- Exercices sur les matrices extracellulaires, le cytosquelette et les adhérences cellule-cellule
- Exercices sur les voies de signalisation
- Glossaire
- Glossaire des termes liés à la génétique
- Glossaire des termes liés au cytosquelette, la matrice extracellulaire, l’adhérence et la migration cellulaire
- Histoire de la biologie cellulaire et de la biologie du développement
- L’acide rétinoïque
- L’apoptose
- L’autophagie
- L’organogenèse
- L’ovogénèse prépare le développement embryonnaire
- La drosophile
- La fécondation
- La formation des somites
- La gastrulation
- La gastrulation (version allégée)
- La métamorphose chez les Hexapodes et les Amphibiens
- La neurogénèse chez les mammifères adultes
- La neurulation
- La poule
- La signalisation calcique
- La souris
- La superfamille TGFβ et ses voies de signalisation
- La voie de signalisation de l’auxine et ses rôles
- La voie de signalisation Hedgehog
- La voie de signalisation Hippo et ses composants YAP/TAZ
- La voie de signalisation Notch
- Le clivage
- Le cytosquelette
- Le destin des cellules et les réseaux de régulation génique
- Le développement des bourgeons de membre
- Le développement des muscles striés squelettiques
- Le développement des organes génitaux et des cellules germinales
- Le développement du cortex
- Le méristème apical caulinaire en phase végétative et lors de la formation d’une fleur
- Le poisson zèbre
- Le xénope
- Les cellules des crêtes neurales
- Les cellules et les gènes en action dans le développement
- Les cellules souches
- Les cellules tumorales
- Les cycles et les divisions cellulaires
- Les étapes du développement
- Les étapes du développement embryonnaire d’Arabidopsis thaliana et leur contrôle
- Les inductions embryonnaires et les gradients de morphogène
- Les matrices extracellulaires animales
- Les organismes modèles
- Les outils pour étudier l’expression et la fonction des gènes
- Les parois des cellules végétales
- Les techniques et les outils pour la biologie cellulaire
- Les transitions épithélio-mésenchymateuses et les migrations cellulaires
- Les vésicules extracellulaires
- Les voies de signalisation
- Les voies de signalisation FGF
- Mise en place des axes chez les Vertébrés
- Structures et processus cellulaires
- Voies de signalisation WNT
