Niveaux de difficulté : * = embryon; ** = têtard; *** = mature
EXERCICE 1
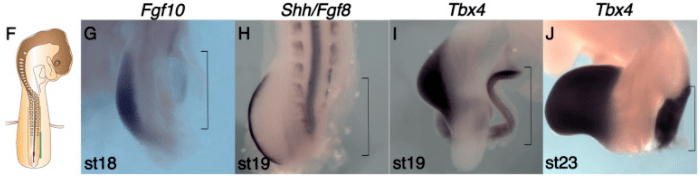
*1.1 Quel est l’objectif de la mise en place de la barrière ?
*1.2 Analysez et interprétez les résultats de cette expérience concernant la morphologie et les expressions de FGF10, FGF8 et Shh.
*1.3 Quelles informations complémentaires nous apporte les hybridations in situ avec la sonde Tbx4 ?
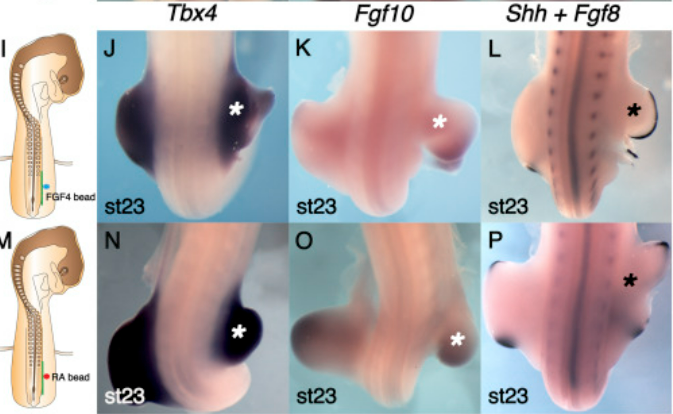
*1.4 Que peut-on conclure de ces expériences sur le rôle du FGF4 et de l’acide rétinoïque au cours du développement précoce du bourgeon de membre ? Est-ce que ce sont les inducteurs en provenance du mésoderme pré-somitique ?
EXERCICE 2

*2.1 Décrivez et proposez une explication pour le phénotype chez les mutants Eif3cXs-J/+.
**2.2 Décrivez et interprétez le phénotype des souris Eif3cXs-J/+;Ptch1+/-.
EXERCICE 3

*3.1 Interprétez le fait qu’à la fois radius et cubitus d’une part et tibia et péroné d’autre part sont affectés.
*3.2 Analysez les résultats de l’hybridation in situ. Expliquez l’origine du phénotype des mutants Ulnaless.
***3.3 Comment le génotype de la mutation peut expliquer ce que vous avez mis en évidence en 3.2 ?
EXERCICE 4

Des enfants naissent avec des pieds dit « fendus » (à droite en haut; à gauche, pied normal d’un enfant du même âge). Cela peut venir d’une mutation perte-de-fonction du gène Dlx5. On génère une souris avec la même mutation dans son gène Dlx5 et elle a également le pied fendu. On réalise une hybridation in situ au cours du développement de son bourgeon de membre avec une sonde reconnaissant l’ARNm de FGF8 (C; en B témoin avec le gène Dlx5 fonctionnel). Source : https://onlinelibrary.wiley.com/doi/10.1002/ajmg.a.31252
*4.1 Quelles informations apporte cette expérience pour expliquer l’origine du phénotype « pied fendu » ?
*4.2 Quelles hypothèses peut-on faire quant au rôle de Dlx5 au cours du développement du bourgeon de membre ?
REPONSES
1.1 Elle a pour objectif de bloquer les communications paracrines entre le mésoderme présomitique et les lames latérales. 1.2 En comparaison avec le côté témoin à gauche, le bourgeon de membre est très atrophié du côté où la barrière a été placée. L’expression de FGF10 est à peine activée et celle de FGF8 n’est pas activée alors que du côté sans la barrière, l’expression de ces gènes est assez importante. FGF8 est exprimé dans l’AER que ‘on voit bien formé au stade 19 du côté sans barrière et donc l’AER n’est pas formé du côté avec la barrière. Shh est légèrement exprimé du côté normal au stade 19 dans le mésenchyme postérieur (début de la formation de la ZPA). Il n’y a pas d’expression du côté avec la barrière. On en déduit que l’absence de communication paracrine entre le mésoderme présomitique et les lames latérales ont gravement compromis le début du développement du bourgeon de membre. 1.3 Au stade 19, Tbx4 est tout de même activé du côté avec la barrière mais plus faiblement et dans un volume plus petit que du côté témoin. Au stade 23, le marquage est plus large et il semble qu’un bourgeon de membre est en train de se développer avec retard (Tbx4 est un des gènes activés les plus précocement dans le bourgeon de membre postérieur, avant FGF8/10 et Shh). Il est possible que des voies de signalisation alternatives aient pu compenser l’absence des signaux en provenance du mésoderme présomitique. Il est aussi possible que la barrière ne limite plus bien le passage des signaux en provenance du mésoderme présomitique (qui a pu évoluer en somites) avec la croissance des tissus. 1.4 Avec les billes sécrétant FGF4 le bourgeon de membre produit parait plus gros au stade 23 (en comparaison avec la photo J de la figure précédente) et on observe une expression faible de FGF10 et une expression de FGF8 dans un AER. C’est un bourgeon de membre qui est néanmoins très en retard par rapport à celui du côté normal qui a éteint FGF10 et FGF8 qui sont exprimés au début de la croissance du bourgeon. Le bourgeon normal exprime Shh dans la partie postérieure ce qui n’est pas (encore ?) le cas du bourgeon du côté traité. On aurait aimé avoir pour comparaison les hybridations in situ FGF8/10 et Shh avec la barrière mais sans les billes. Avec les billes sécrétant l’acide rétinoïque, les expressions des gènes sont plus marquées et étendues et il y a un AER exprimant FGF8 et une ZPA exprimant Shh. L’acide rétinoïque semble avoir aussi un effet sur le bourgeon de membre à droite réactivant des gènes comme FGF8 et FGF10 ce qui indique que l’acide rétinoïque peut diffuser très largement et contourner la barrière. Les doses utilisées ne sont peut-être pas physiologiques. En tout cas, FGF4 et l’acide rétinoïque sont des candidats pour constituer le signal en provenance du mésoderme pré-somitique mais rien ne confirme que ce sont bien eux. Ils peuvent mimer l’action d’une autre molécule ou se trouver en aval dans la cascade de signalisation par rapport au signal envoyé par le mésoderme pré-somitique. Il faudrait faire des expériences de perte-de-fonction spécifique pour le savoir.
2.1 : Le squelette des membres antérieurs et postérieurs des mutants semblent globalement un peu plus fins/moins développés que chez le sauvage. A part cela, la régionalisation des doigts semble normale dans la patte postérieure tandis que dans la patte antérieure, le doigt 1 (le plus antérieur) est nettement plus allongé, avec plus de phalanges au lieu d’une. Il se met à ressembler à des doigts plus postérieurs. Cette postériorisation pourrait être due à une signalisation Shh plus importante, Shh étant un morphogène qui donne une identité plus postérieure pour de plus fortes concentrations. 2.2 : Avec la double mutation perte-de-fonction, mêmes les pattes postérieures présentent désormais une postériorisation du doigt 1 et il y a un doigt supplémentaire (polydactylie) qui est lui aussi postériorisé. Dans les pattes antérieures, la postériorisation du doigt 1 est encore plus marquée que dans le simple mutant et il y a aussi développement d’un doigt supplémentaire. Sachant que les souris Ptch1+/- ne présentent pas de phénotype notable au niveau des doigts, cela indique une interaction génétique importante entre eIF3c et la voie Shh dont fait partie Ptch1 en tant qu’inhibiteur. Ainsi, le facteur eIF3c serait requis pour inhiber la voie Shh et renforce l’effet de la mutation Ptch1 (et inversement la mutation de Ptch1 renforce l’effet de la mutation de eIF3c).
3.1 Toutes ces structures appartiennent au zeugopode sur l’axe proximo-distal et donc ainsi des régions équivalentes entre le membre antérieur et le membre postérieur sont affectées. 3.2 Chez le mutant Ulnaless, l’expression de Hoxd13 se propage dans des régions plus proximales que dans le cas normal. Les gènes des complexes Hox spécifient les différentes régions selon l’axe proximo-distal et Hoxd13 en particulier spécifie l’autopode et non le zeugopode. Ainsi l’expression ectopique de Hoxd13 dans ce qui devrait devenir le zeugopode perturbe son développement. 3.3 Le rapprochement de Hoxd13 d’une série d’enhancers peut modifier le contrôle de la transcription de ce gène, tout particulièrement si ces enhancers contrôlent l’expression dans des régions plus proximales que celles où Hoxd13 est normalement exprimé. On peut imaginer que le repliement de la chromatine peut se faire plus facilement à proximité entre les enhancers et le gène (qu’ils se retrouvent alors dans le même TAD ou domaine topologique d’activation).
4.1 On se rend compte que chez la souris mutante, l’expression de FGF8 est discontinue dans la région de l’AER avec une large portion centrale où l’expression est très faible à inexistante. Or on sait que FGF8 produit par l’AER est nécessaire à la croissance le long de l’axe proximo-distal. Chez le mutant, l’AER est comme coupé en deux et deux axes de croissance du bourgeon de membre vont ainsi se mettre en place ce qui peut expliquer que le pied est coupé en deux avec la partie médiane manquante. 4.2 Dlx5 semble nécessaire à une bonne expression de FGF8 dans l’AER, notamment dans la région médiane. Il doit donc contribuer directement ou indirectement à l’activation ou au maintien de l’expression de FGF8 dans cette partie de l’AER.
< Retour à la page sur le développement du bourgeon de membre
